Clear Sky Science · pt
Co-entrega da quimiocina CXCL9 e do ligante coestimulador TNFSF9 por células-tronco mesenquimais reprograma o microambiente imune para câncer de mama triplo-negativo
Por que essa nova abordagem para câncer de mama é importante
O câncer de mama triplo-negativo é uma das formas mais perigosas porque cresce rapidamente, se espalha precocemente e carece dos alvos hormonais comuns em que muitos medicamentos se baseiam. A imunoterapia acendeu esperanças, mas em muitos pacientes as células defensoras do organismo simplesmente não entram no tumor em número suficiente para fazer diferença. Este estudo explora uma estratégia inventiva: usar células vivas como “caminhões de entrega” guiados que levam sinais que potencializam o sistema imune diretamente a tumores de difícil tratamento, possivelmente tornando mais pacientes elegíveis para terapias imunológicas potentes.
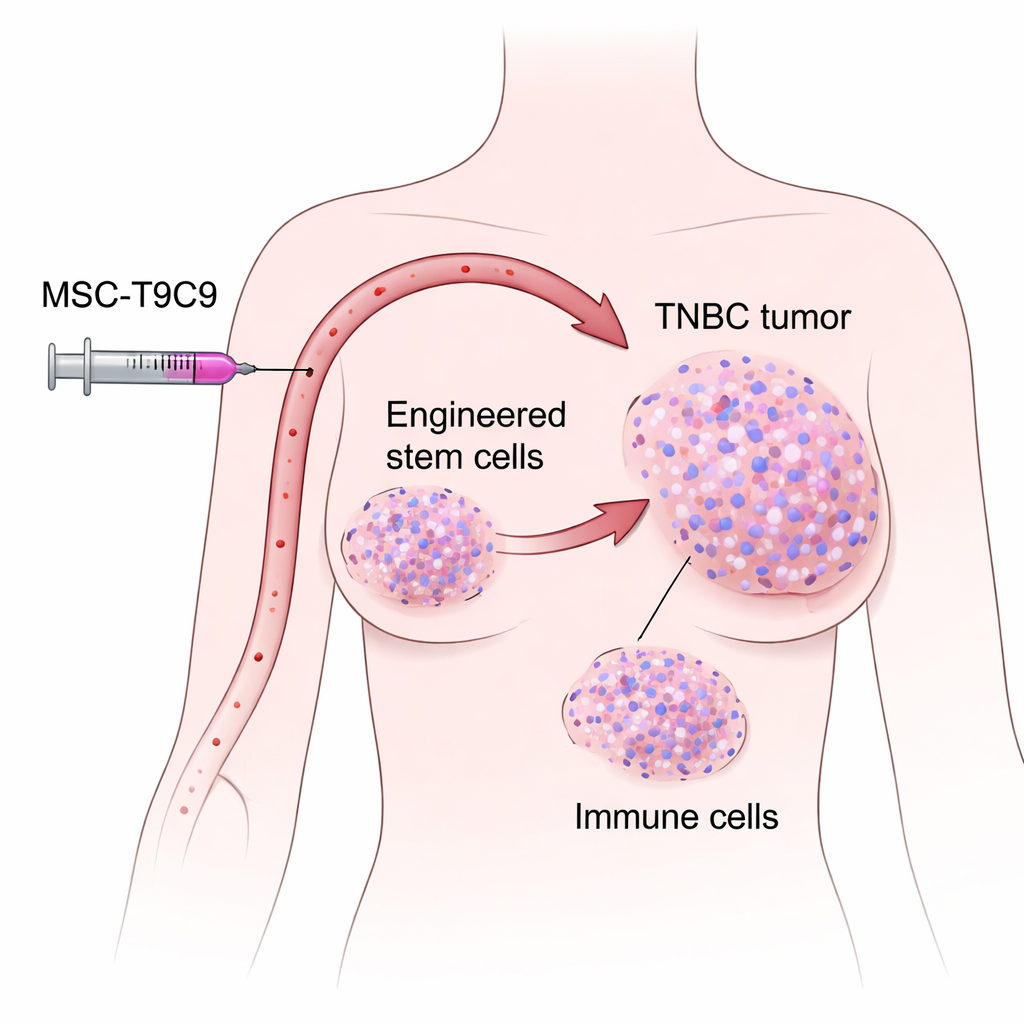
Um câncer difícil com ajuda imune insuficiente
Os tratamentos padrão para o câncer de mama triplo-negativo — cirurgia, quimioterapia e radioterapia — muitas vezes não impedem a recidiva, e a sobrevida média para doença avançada permanece abaixo de dois anos. Uma razão-chave é que muitos desses tumores são “frios”, ou seja, contêm poucas células imunes que combatem o câncer. Grandes bases de dados de pacientes mostraram que pessoas cujos tumores produzem naturalmente maiores quantidades de duas moléculas relacionadas à imunidade, CXCL9 e TNFSF9, tendem a viver mais e a ter mais células T e células natural killer (NK) dentro dos tumores. CXCL9 é um sinal químico que atrai células imunes aos tecidos, enquanto TNFSF9 funciona como um interruptor adicional que ajuda essas células a atacarem com mais força. O padrão sugeriu que aumentar ambos os sinais diretamente dentro dos tumores poderia inclinar a balança a favor do sistema imune.
Transformando células-tronco em caminhões de entrega inteligentes
Os pesquisadores se concentraram em células-tronco mesenquimais obtidas de cordões umbilicais humanos doados. Essas células têm uma propriedade útil: quando injetadas na corrente sanguínea de camundongos com tumores mamários, elas migram naturalmente para os locais tumorais e ali permanecem por dias, evitando em grande parte órgãos normais. A equipe geneticamente modificou essas células para liberar CXCL9 e exibir TNFSF9 em sua superfície, criando uma terapia celular de duplo propósito que chamam de MSC-T9C9. Testes em laboratório mostraram que as células modificadas liberavam altos níveis de CXCL9 e ativavam fortemente células T e NK de camundongo, sem alterar seu próprio comportamento de crescimento ou provocar tumores. Isso as tornou candidatas promissoras como amplificadores imunes direcionados.
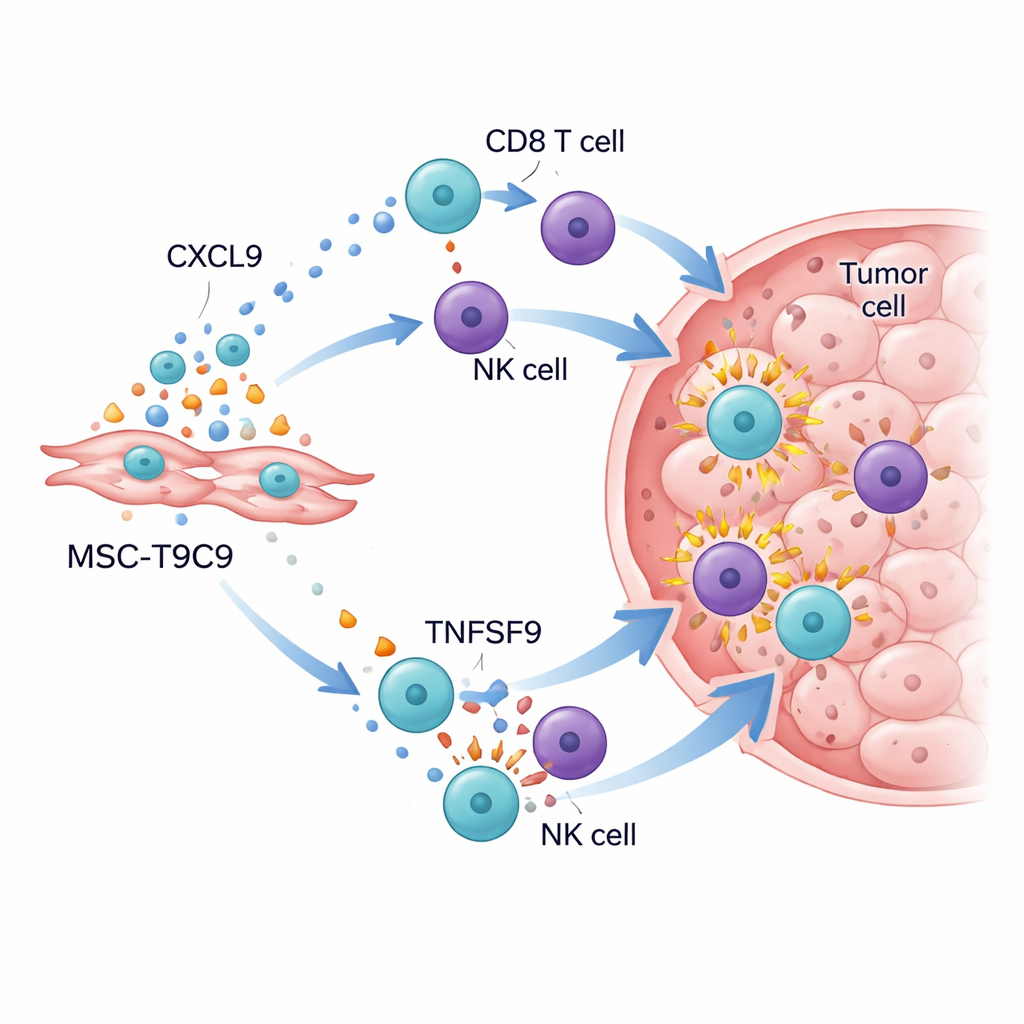
Despertando o campo de batalha imune do tumor
Quando as células modificadas foram administradas a camundongos portadores de tumores de mama triplo-negativos, os resultados foram impressionantes. Em camundongos com um sistema imune funcional, injeções repetidas de MSC-T9C9 retardaram fortemente o crescimento tumoral e aumentaram a morte das células cancerosas, enquanto células-tronco controle tiveram pouco efeito. Análises detalhadas dos tumores mostraram um aumento dramático no número de células T CD8 “assassinas” e células NK, junto com níveis mais altos de moléculas de ataque potentes como granzyme B, interferon-γ, fator de necrose tumoral-α e interleucina-2. Ao mesmo tempo, o microambiente tumoral mudou de um estado supressor: macrófagos inflamatórios benéficos aumentaram e, embora células T reguladoras ainda estivessem presentes, foram superadas pela nova onda de combatentes. Em camundongos imunodeficientes, onde células T e NK estão ausentes, MSC-T9C9 não retardou o crescimento tumoral, confirmando que seu benefício depende da mobilização das defesas do próprio organismo.
Preparando tumores para a terapia com checkpoint
Drogas imunoterápicas modernas, como anticorpos anti-PD-1, liberam os “freios” moleculares das células T, mas funcionam melhor quando já há células T suficientes dentro do tumor. O estudo descobriu que MSC-T9C9 não apenas atraiu mais células T CD8 para os tumores, como também as levou a um estado altamente ativo, porém sensível aos freios, marcado pelo receptor PD-1. Em um modelo de camundongo, a combinação de MSC-T9C9 com um anticorpo anti-PD-1 produziu a maior redução tumoral e a sobrevivência mais longa em comparação com cada tratamento isoladamente. Análises de conjuntos de dados de câncer humano apoiaram essa ideia: pacientes com níveis combinados mais altos de TNFSF9 e CXCL9 tinham maior probabilidade de se beneficiar de terapias que bloqueiam checkpoints, sugerindo que a mesma biologia pode se aplicar em pessoas.
Segurança e promessa futura
Qualquer tratamento que aumente a imunidade levanta preocupações sobre efeitos colaterais perigosos, como inflamação generalizada ou dano a órgãos. De forma encorajadora, camundongos que receberam MSC-T9C9 mantiveram peso e comportamento normais, não mostraram lesões óbvias em órgãos principais e apresentaram resultados normais em testes sanguíneos e de função hepática/renal. Importante, o surto de atividade imune ficou em grande parte confinado ao próprio tumor, e sinais inflamatórios na corrente sanguínea não aumentaram. Embora mais trabalho seja necessário antes de ensaios em humanos — incluindo testes em modelos mais realistas e cuidadosa determinação de dose — este estudo sugere que guiar células-tronco geneticamente modificadas aos tumores para atrair e ativar células imunes pode oferecer uma forma direcionada e mais segura de transformar cânceres de mama triplo-negativos “frios” em “quentes” que respondem melhor à imunoterapia.
Citação: Ye, P., Wen, Y., Liu, R. et al. Co-delivery of chemokine CXCL9 and costimulatory ligand TNFSF9 by mesenchymal stem cells reprograms the immune microenvironment for triple-negative breast cancer. npj Breast Cancer 12, 30 (2026). https://doi.org/10.1038/s41523-026-00893-5
Palavras-chave: câncer de mama triplo-negativo, imunoterapia, células-tronco mesenquimais, microambiente tumoral, bloqueio de checkpoints