Clear Sky Science · pt
Interleucina-1α derivada do hospedeiro promove imunossupressão tumoral ao reprogramar células mieloides associadas ao tumor
Por que esta pesquisa importa para pacientes com câncer
A imunoterapia transformou o tratamento de alguns cânceres, mas muitos tumores de mama ainda escapam do sistema imunológico. Este artigo explora um culpado menos conhecido: uma molécula de sinalização chamada interleucina‑1 alfa (IL‑1α) produzida não pelas próprias células cancerosas, mas por células normais do corpo. Os autores mostram que a IL‑1α derivada do hospedeiro pode silenciosamente transformar células imunes em aliadas do tumor, e que bloquear esse sinal em camundongos pode fazer com que tumores de mama encolham ou desapareçam. Entender essa mudança pode ajudar médicos a projetar tratamentos que tornem a imunoterapia mais eficaz para o câncer de mama.
Um influenciador oculto na vizinhança tumoral
Os cânceres não crescem isoladamente; eles vivem em uma “vizinhança” movimentada de células imunes, vasos sanguíneos e tecido conjuntivo conhecida como microambiente tumoral. Entre os moradores mais importantes estão as células mieloides, especialmente os macrófagos, que podem tanto atacar os tumores quanto protegê‑los. Textos clássicos dividem os macrófagos em M1 (que combatem tumores) e M2 (que os apoiam), mas tumores reais contêm muitos matizes intermediários. Os autores focalizaram a IL‑1α, uma molécula normalmente produzida por tecidos não cancerosos, para investigar se esse sinal do hospedeiro orienta as células mieloides que chegam para papéis úteis ou prejudiciais dentro dos tumores de mama.
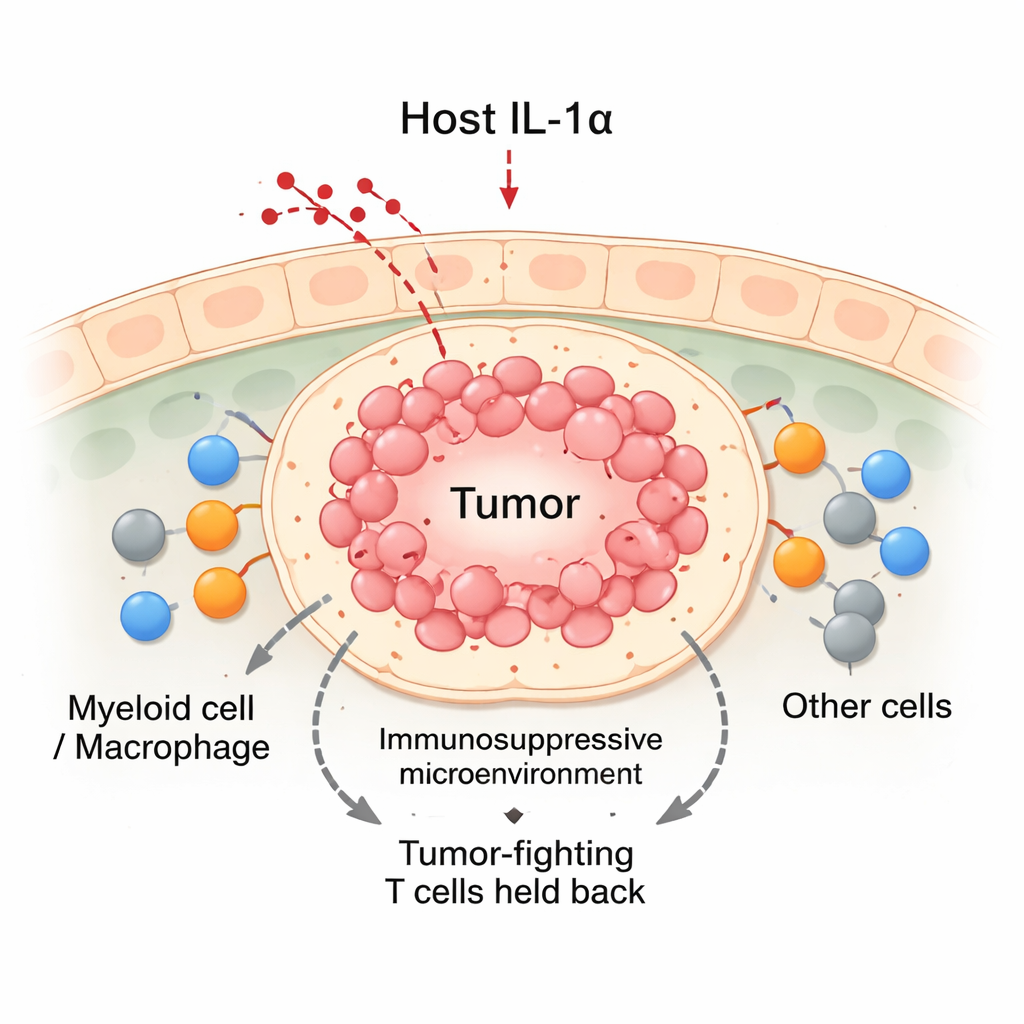
Desligar a IL‑1α inclina a balança contra os tumores
Usando modelos murinos de câncer de mama, a equipe comparou animais normais com outros geneticamente alterados para não produzir IL‑1α. Quando células de câncer de mama foram transplantadas nas glândulas mamárias, os tumores em camundongos normais cresceram de forma constante. Em contraste, tumores em camundongos deficientes em IL‑1α cresceram nas primeiras cerca de duas semanas e depois frequentemente regrediram. Esses tumores em regressão continham mais células imunológicas no geral, incluindo um aumento de células T CD8 “assassinas” e de células mieloides. Apesar de os camundongos sem IL‑1α apresentarem menos leucócitos circulantes no sangue, eles concentraram muito mais células imunes no local do tumor. Análises detalhadas mostraram que as células T CD8 infiltrantes nos tumores sem IL‑1α estavam mais ativas, produzindo níveis mais altos de moléculas citotóxicas e exibindo menos sinais de exaustão.
Como a IL‑1α remodela as células mieloides associadas ao tumor
Para entender o que a IL‑1α fazia a nível celular, os pesquisadores usaram sequenciamento de RNA de célula única para examinar milhares de células individuais dos tumores. Descobriram que apenas um pequeno subconjunto de macrófagos associados ao tumor — aqueles marcados por um receptor chamado CX3CR1 — produzia IL‑1α. Em camundongos normais, muitos monócitos que chegavam amadureciam nesses macrófagos positivos para CX3CR1, os quais estavam associados a um comportamento imunossupressor. Em camundongos sem IL‑1α, essa via de maturação foi interrompida. Em vez disso, as células mieloides tinham maior probabilidade de se tornar macrófagos inflamatórios positivos para iNOS, um perfil associado à atividade anti‑tumoral. Funcionalmente, as células mieloides de tumores deficientes em IL‑1α eram menos capazes de induzir “freios” como PD‑1 e CTLA‑4 nas células T, e mostraram menor capacidade de reduzir a proliferação de células T.
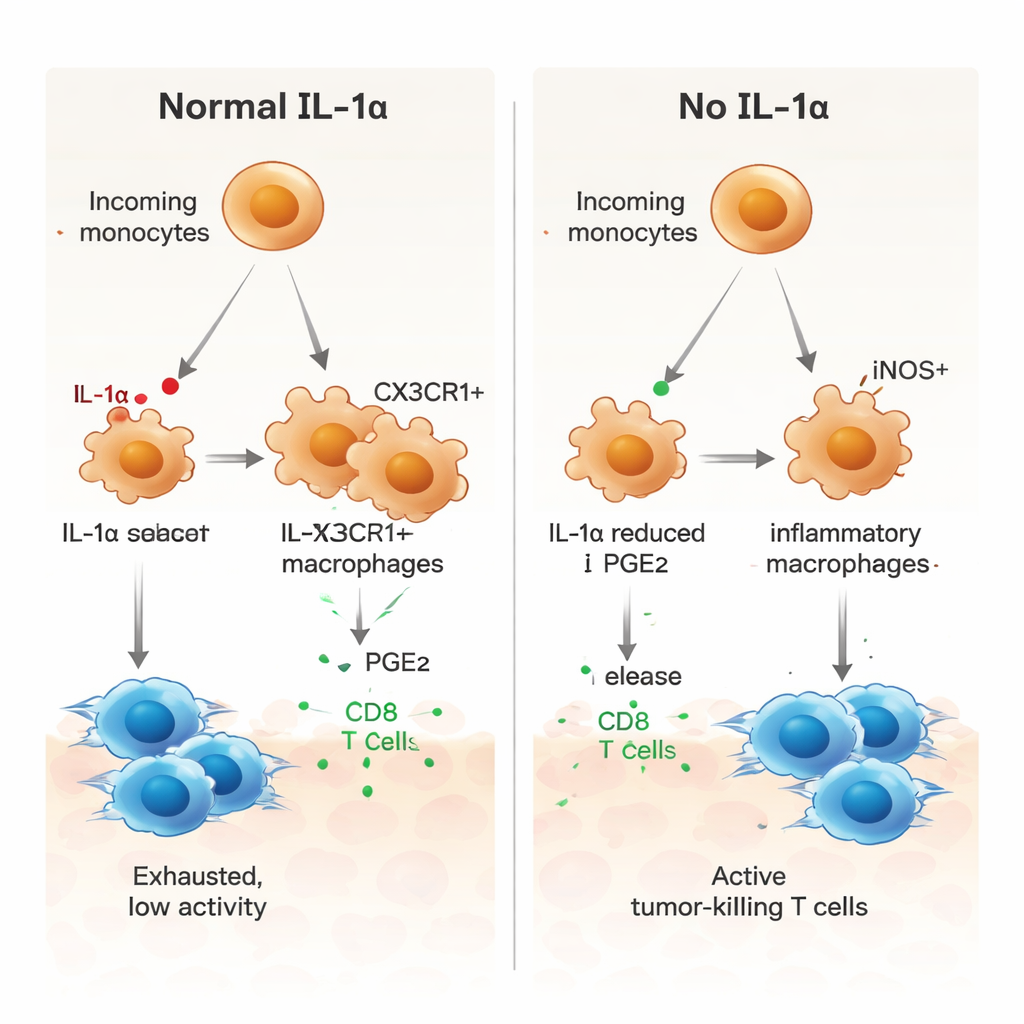
Um papel-chave para um mensageiro lipídico, a PGE2
Os autores então perguntaram como a IL‑1α direciona as células mieloides para um estado de apoio ao tumor. A análise de comunicação dos dados de célula única apontou para várias vias de sinalização, incluindo uma envolvendo a prostaglandina E2 (PGE2), um mediador lipídico conhecido por promover imunossupressão. Em tumores sem IL‑1α, os macrófagos expressavam níveis mais baixos de receptores para o fator de crescimento de macrófagos (M‑CSF), receptores de TGF‑β e um receptor de PGE2, e células do estroma próximas produziam menos das enzimas que geram PGE2. Em culturas de laboratório, macrófagos derivados da medula óssea de camundongos deficientes em IL‑1α exibiram um perfil mais inflamatório, com maior iNOS e menor CX3CR1. A adição de PGE2 reverteu essa mudança e restaurou um padrão mais supressor, enquanto bloquear PGE2 em macrófagos normais os empurrou para um estado pró‑inflamatório. Macrófagos sem IL‑1α também estimularam mais fortemente a proliferação de células T CD8 específicas ao tumor, um efeito atenuado quando PGE2 foi readicionado.
Ligando achados em camundongos à imunidade humana
Para verificar se seus dados murinos refletem a biologia humana, a equipe comparou assinaturas gênicas dos diferentes subconjuntos de macrófagos de camundongos com um amplo painel de células mieloides humanas direcionadas a vários estados em laboratório. Agregados de macrófagos de tumores em camundongos normais assemelharam‑se a células humanas levadas a estados semelhantes a M2, de amortecimento imune, por moléculas como IL‑10, IL‑4 e glucocorticoides. Em contraste, os mesmos agregados de tumores deficientes em IL‑1α corresponderam a células humanas em condições mais inflamatórias e menos supressoras. Notavelmente, padrões gênicos ligados à sinalização de PGE2 estavam enriquecidos em macrófagos dependentes de IL‑1α, mas ausentes quando IL‑1α faltava, reforçando a ideia de que IL‑1α e PGE2 atuam juntos para construir um nicho imunossupressor.
O que isso pode significar para terapias futuras do câncer de mama
Em termos simples, este estudo sugere que uma molécula derivada do hospedeiro, IL‑1α, pode silenciosamente instruir certos macrófagos a proteger o tumor e manter as células T assassinas sob controle, em parte por meio da sinalização da PGE2. Quando a IL‑1α é removida em camundongos, os macrófagos mudam para um estado mais inflamatório e atacam o tumor, as células T CD8 tornam‑se mais ativas, e tumores de mama transplantados são frequentemente rejeitados. Como as imunoterapias atuais já visam reenergizar células T exauridas, combiná‑las com abordagens que bloqueiem a IL‑1α ou sua via downstream da PGE2 poderia inclinar ainda mais o microambiente tumoral a favor do sistema imune do paciente. Embora sejam necessários mais estudos para testar segurança e eficácia em humanos, esses achados destacam a IL‑1α como um novo alvo promissor para tornar o câncer de mama mais vulnerável ao ataque imune.
Citação: Keerthi Raja, M.R., Gupta, G., Atkinson, G. et al. Host-derived interleukin-1α drives tumor immunosuppression by reprogramming tumor-associated myeloid cells. npj Breast Cancer 12, 26 (2026). https://doi.org/10.1038/s41523-026-00890-8
Palavras-chave: imunoterapia do câncer de mama, microambiente tumoral, macrófagos, interleucina-1 alfa, prostaglandina E2