Clear Sky Science · pt
Eliminação direcionada de infecções mastíticas por Staphylococcus aureus com sistemas sintéticos de entrega CRISPR-Cas baseados em fagos
Combate a uma infecção cara na produção de laticínios
O leite de vacas e outros animais de fazenda pode ser comprometido por uma dolorosa infecção mamária chamada mastite, frequentemente causada pela bactéria Staphylococcus aureus. Tratar essas infecções geralmente exige cursos longos de antibióticos, que são caros, estressantes para os animais e contribuem para o problema crescente da resistência aos antibióticos. Este estudo explora uma abordagem radicalmente diferente: transformar um parasita natural semelhante a vírus de bactérias em uma arma de precisão que pode cortar seletivamente o DNA bacteriano e eliminar infecções sem disseminar genes de resistência.
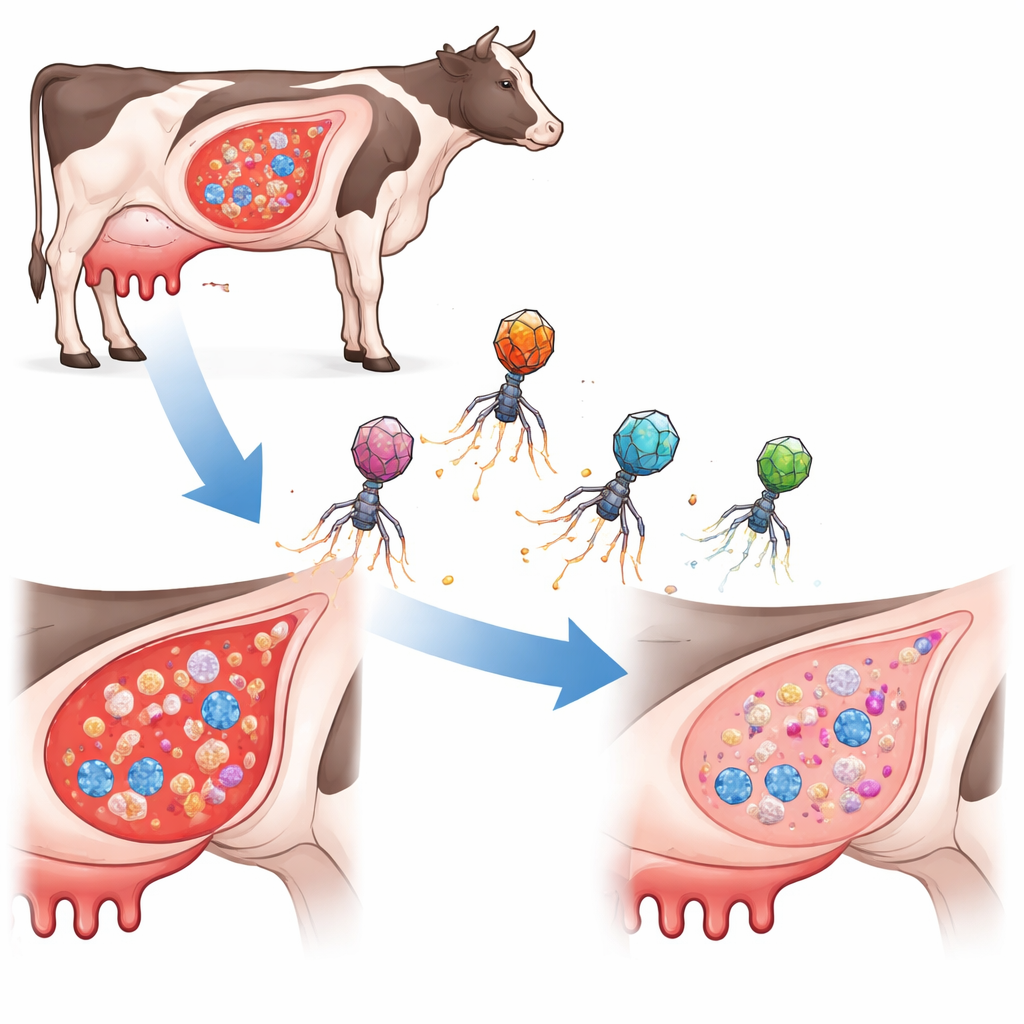
Um novo tipo de caçador bacteriano direcionado
Em vez de usar antibióticos tradicionais ou bacteriófagos comuns (vírus que infectam bactérias), os pesquisadores projetaram pequenos elementos portadores de DNA conhecidos como ilhas cromossômicas indutíveis por fagos. Na natureza, essas ilhas "peganham carona" dentro de capsídeos fagais para pular entre células bacterianas. Aqui, a equipe as reconstruiu como “ePICIs” que carregam a ferramenta de edição genética CRISPR‑Cas9 mais pequenas sequências guia direcionadas a três RNAs regulatórios pequenos, mas importantes, em S. aureus. Quando um ePICI entra em uma célula alvo, Cas9 é produzido e corta o cromossomo bacteriano no sítio escolhido, matando a célula de dentro. Crucialmente, essas partículas engenheiradas não se replicam por conta própria, o que limita sua dispersão e reduz o risco de mover acidentalmente genes nocivos.
Como o escudo bacteriano muda a batalha
S. aureus frequentemente sobrevive ao tratamento formando biofilmes — comunidades pegajosas onde as células ficam embebidas em uma matriz produzida por elas mesmas. A equipe comparou dois tipos comuns de matriz: uma construída principalmente a partir de uma proteína chamada Bap, e outra feita de um polímero de açúcar conhecido como PIA/PNAG. Em testes de laboratório, biofilmes ricos em Bap protegeram fortemente as bactérias contra os ePICIs e contra um fago auxiliar padrão, atuando como uma armadura densa que bloqueava a infecção. Em contraste, biofilmes baseados no polímero de açúcar tornaram as bactérias mais fáceis de matar, provavelmente porque enzimas nas cápsides virais conseguem degradar esses açúcares e ajudar as partículas a alcançar seus alvos.
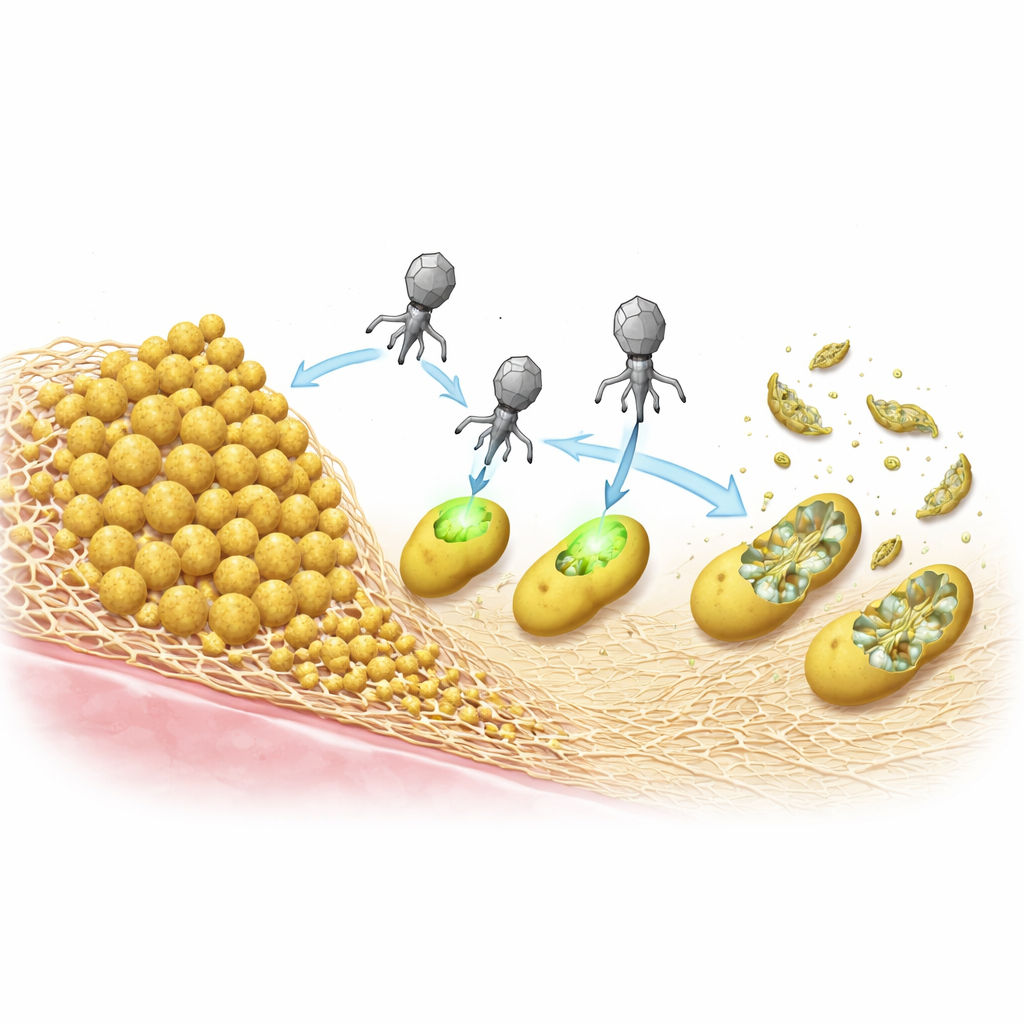
Matar bactérias sem integrar seu DNA
Uma vez dentro da célula, os ePICIs podem integrar‑se ao cromossomo bacteriano, mas os pesquisadores investigaram se essa etapa é realmente necessária para matar. Eles criaram uma versão que não poderia mais integrar e mostraram que, desde que a partícula fosse produzida corretamente na linhagem de origem, ela era tão letal para S. aureus quanto a original. Isso significa que o sistema CRISPR pode ser expresso diretamente a partir do DNA circular entrante, cumprir sua função e então ser perdido à medida que a célula morre. Essa ação sem integração reduz ainda mais as chances de transferência gênica não intencional e diferencia essas partículas da terapia clássica com fagos, que depende da replicação viral e da lise celular em massa para se propagar.
Do prato de Petri às glândulas mamárias infectadas
Como linhagens produtoras de Bap são comuns na mastite em lactentes, a equipe testou seu construto de melhor desempenho, chamado ePICIrsaE, em um modelo de camundongo que imita infecção da glândula mamária. No leite e em culturas de laboratório, biofilmes ricos em Bap claramente reduziram a atividade do ePICI. Ainda assim, dentro da glândula mamária, doses repetidas de ePICIrsaE reduziram drasticamente o número de bactérias para todas as linhagens testadas, incluindo as que produziam Bap. Seu desempenho foi comparável ao da vancomicina, um poderoso antibiótico de último recurso. Os resultados sugerem que condições em tecido vivo — como menor produção de Bap, a presença de bactérias livres em suspensão ou componentes úteis do leite — permitem que as partículas engenheiradas atuem muito melhor do que em biofilmes estáticos de laboratório.
O que isso pode significar para fazendas e além
O estudo mostra que sistemas CRISPR embalados em fagos e não replicantes podem eliminar seletivamente S. aureus em uma infecção difícil associada a biofilme sem se espalhar ou romper um grande número de células de uma só vez. Embora sejam necessárias doses altas de partículas e a escala de camundongos para vacas será desafiadora, essas partículas oferecem uma alternativa promissora e controlável aos antibióticos para infecções localizadas, como a mastite. Mais amplamente, o trabalho destaca que tratamentos que parecem desapontadores em testes laboratoriais simples ainda podem ter sucesso no ambiente complexo de um animal, e abre a porta para bibliotecas de ePICIs personalizadas ajustadas a diferentes bactérias, cápsides virais e sequências guia.
Citação: Garmendia-Antoñana, N., Dorado-Morales, P., Gil, C. et al. Targeted elimination of Staphylococcus aureus mastitis infections with synthetic phage-based CRISPR-Cas delivery systems. npj Biofilms Microbiomes 12, 67 (2026). https://doi.org/10.1038/s41522-026-00931-x
Palavras-chave: mastite bovina, Staphylococcus aureus, terapia CRISPR, tratamento baseado em fagos, infecções por biofilme