Clear Sky Science · pt
Caracterização metabólica em tempo real e alta resolução de bactérias vivas usando imagem metabólica óptica sem marcadores
Observando Germes Reagir em Tempo Real
Bactérias estão por toda parte em nossa superfície e no nosso interior, silenciosamente moldando nossa saúde. Elas ajudam a digerir alimentos, protegem a pele e, às vezes, causam infecções persistentes que resistem a antibióticos. Este estudo apresenta um método para observar bactérias vivas reagindo ao estresse e a medicamentos em tempo real, ao nível de células individuais, sem adicionar corantes ou marcadores. Essa capacidade pode, no futuro, ajudar médicos a escolher o tratamento certo mais rapidamente e auxiliar cientistas a entender por que algumas infecções são tão difíceis de curar.
A luz como janela para a vida bacteriana
Em vez de adicionar corantes ou etiquetas genéticas, os pesquisadores se apoiam no fato de que bactérias emitem um brilho muito tênue de forma natural quando certas moléculas internas são excitadas por luz laser. Duas dessas moléculas, conhecidas como NAD(P)H e FAD, são peças centrais no processo pelo qual as células transformam alimento em energia. Usando microscopia a laser rápida e de alta resolução, a equipe pode medir tanto o brilho quanto o pequeno atraso temporal desse brilho, revelando o quão ativo está o metabolismo de uma célula. Como o método é sem marcadores e não destrutivo, as mesmas bactérias vivas podem ser acompanhadas por segundos e minutos enquanto o ambiente muda. 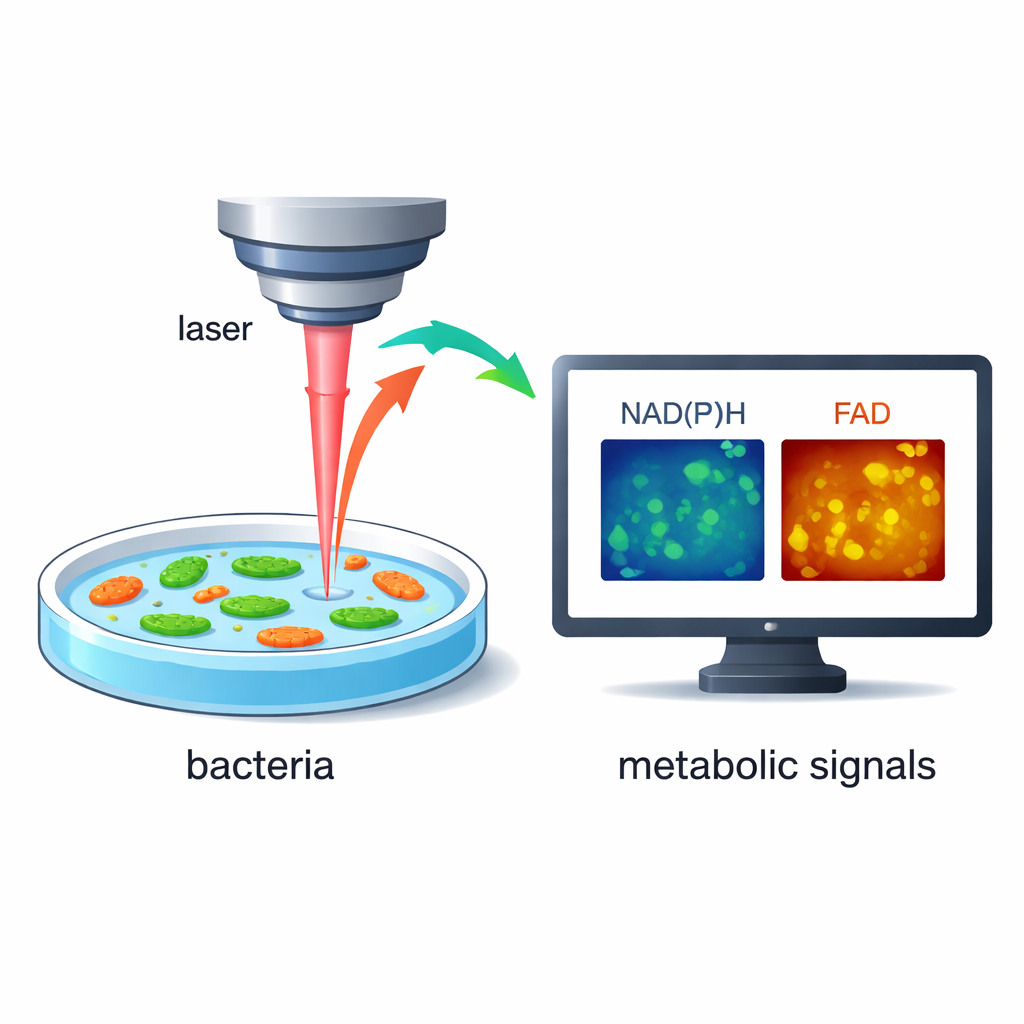
Vendo diferenças entre bactérias individuais
A maioria dos testes de laboratório padrão agrupa milhões de bactérias e reporta apenas uma resposta média. Aqui, os autores mostram que seu método de imageamento pode identificar células únicas de Staphylococcus aureus em cultura líquida e analisar cada uma separadamente, mesmo em altas densidades celulares. Quando compararam duas colônias de S. aureus cultivadas nas mesmas condições, um sinal chave (do FAD) diferiu entre as colônias, e também houve uma dispersão de valores dentro de cada colônia. Isso significa que bactérias geneticamente semelhantes no mesmo frasco podem apresentar estados metabólicos muito diferentes — uma diversidade oculta que testes em larga escala podem perder, mas que pode influenciar como infecções respondem ao tratamento.
Observando antibióticos agirem em segundos
A equipe então acompanhou células individuais de S. aureus enquanto eram expostas a vários tratamentos antibacterianos, incluindo antibióticos comuns e água sanitária doméstica. Usando seu sistema de imageamento rápido, capturaram mudanças desde o momento em que a solução do fármaco tocou as células até os 30 minutos seguintes. Tratamentos fortes causaram queda nos sinais de NAD(P)H e aumento nos sinais de FAD, frequentemente em questão de segundos, refletindo a paralisação da produção de energia e uma mudança para um estado celular mais oxidado. O tempo exato e o padrão dessas mudanças dependiam do tipo e da dose do fármaco: por exemplo, antibióticos que bloqueiam proteínas e os que atacam a parede celular produziram uma queda breve seguida de recuperação parcial, enquanto a água sanitária provocou uma mudança acentuada e sustentada. Essas “assinaturas de luz” distintas sugerem que a técnica consegue detectar não apenas se as células estão estressadas ou morrendo, mas também como estão sendo danificadas. 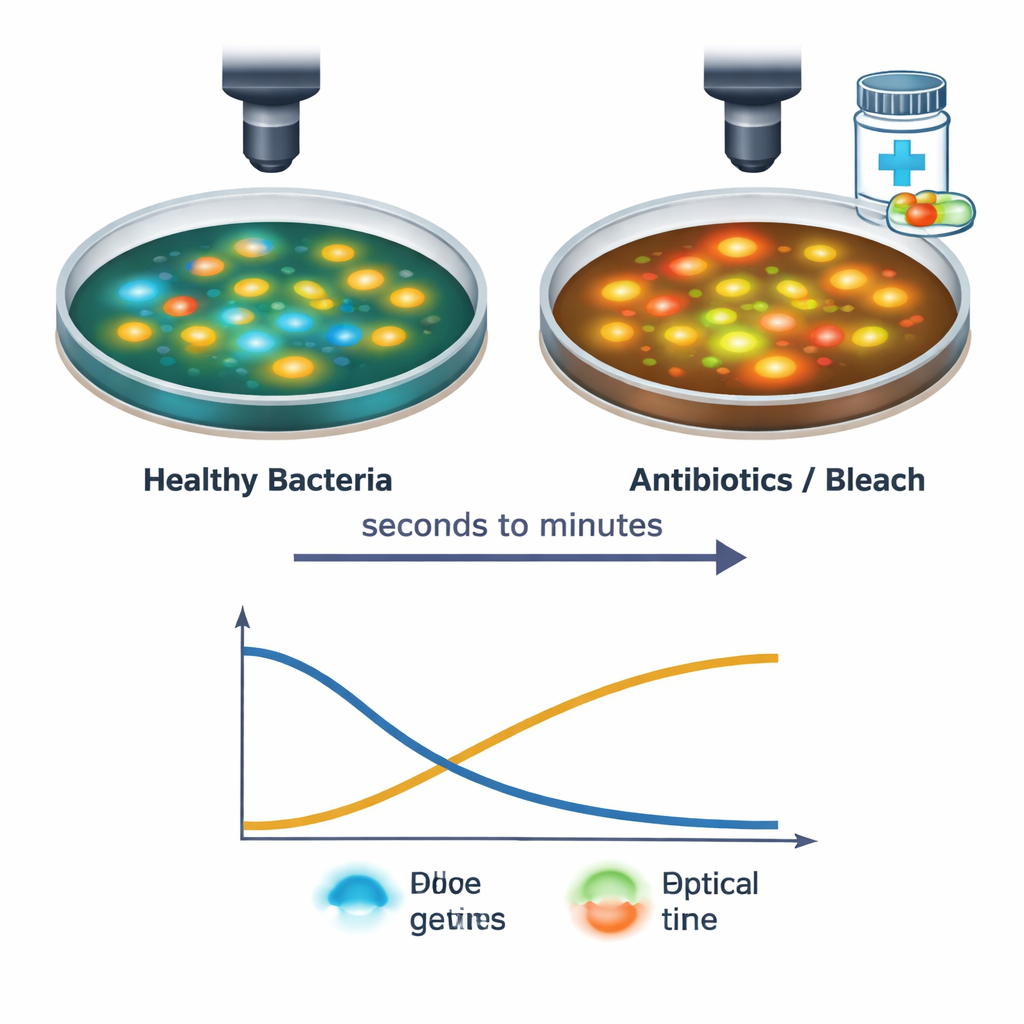
Espiando o mundo oculto dos biofilmes
Bactérias raramente vivem sozinhas na natureza; em vez disso, constroem comunidades viscosas e protetoras chamadas biofilmes em superfícies que vão de implantes médicos a dentes. Nessas camadas densas, algumas células podem estar altamente ativas enquanto outras permanecem dormentes, uma mistura que ajuda a comunidade a sobreviver a antibióticos. Usando imagens grandes montadas em mosaico, os pesquisadores mapearam a paisagem metabólica dentro de biofilmes de S. aureus e a compararam com células livres em suspensão. Eles encontraram bolsões brilhantes e metabolicamente ativos cercados por regiões menos ativas e mostraram que, em várias espécies, bactérias em biofilmes tendiam a apresentar um perfil metabólico mais oxidado do que suas contrapartes livres. Sinais ópticos adicionais sugeriram excesso de lipídios e proteínas, compatíveis com o material tipo cola que mantém os biofilmes unidos.
Por que isso importa para a medicina futura
Em conjunto, esses resultados mostram que a imageamento metabólico óptico sem marcadores pode fornecer instantâneos rápidos, detalhados e não invasivos de como bactérias vivem, se adaptam e morrem. Para o leitor leigo, a mensagem chave é que os cientistas agora podem “escutar” o uso de energia bacteriana em tempo real, sem perturbar as células, usando apenas luz cuidadosamente ajustada. A longo prazo, esse tipo de tecnologia pode ajudar a identificar bactérias difíceis de cultivar, localizar bolsões de células tolerantes a fármacos dentro de biofilmes ou testar rapidamente como a infecção de um paciente responde a diferentes antibióticos. Isso poderia apoiar tratamentos mais rápidos e personalizados e aprofundar nossa compreensão dos mundos microbianos invisíveis que afetam nossa saúde todos os dias.
Citação: Sorrells, J.E., Yang, L., Iyer, R.R. et al. Real-time, high-resolution metabolic characterization of live bacteria using label-free optical metabolic imaging. npj Biofilms Microbiomes 12, 55 (2026). https://doi.org/10.1038/s41522-026-00920-0
Palavras-chave: metabolismo bacteriano, imageamento óptico, biofilmes, resposta a antibióticos, microbioma