Clear Sky Science · pt
Terapia antibiótica potencializada por enzimas reduz biofilmes a níveis indetectáveis em um modelo de infecção associada a implantes
Por que infecções persistentes em implantes são importantes
Substituições de quadril e joelho transformam vidas, mas quando bactérias colonizam esses implantes metálicos elas podem formar comunidades viscosas chamadas biofilmes. Esses biofilmes funcionam como cidades fortificadas que protegem os microrganismos tanto do sistema imunológico quanto dos antibióticos, levando a infecções dolorosas e de longa duração que são muito difíceis de curar. Este estudo explora um novo tratamento em duas frentes que primeiro ajuda a desmantelar as defesas do biofilme e depois banha a área com altas doses de antibióticos — uma abordagem que pode, no futuro, ajudar a salvar mais implantes em vez de substituí‑los.
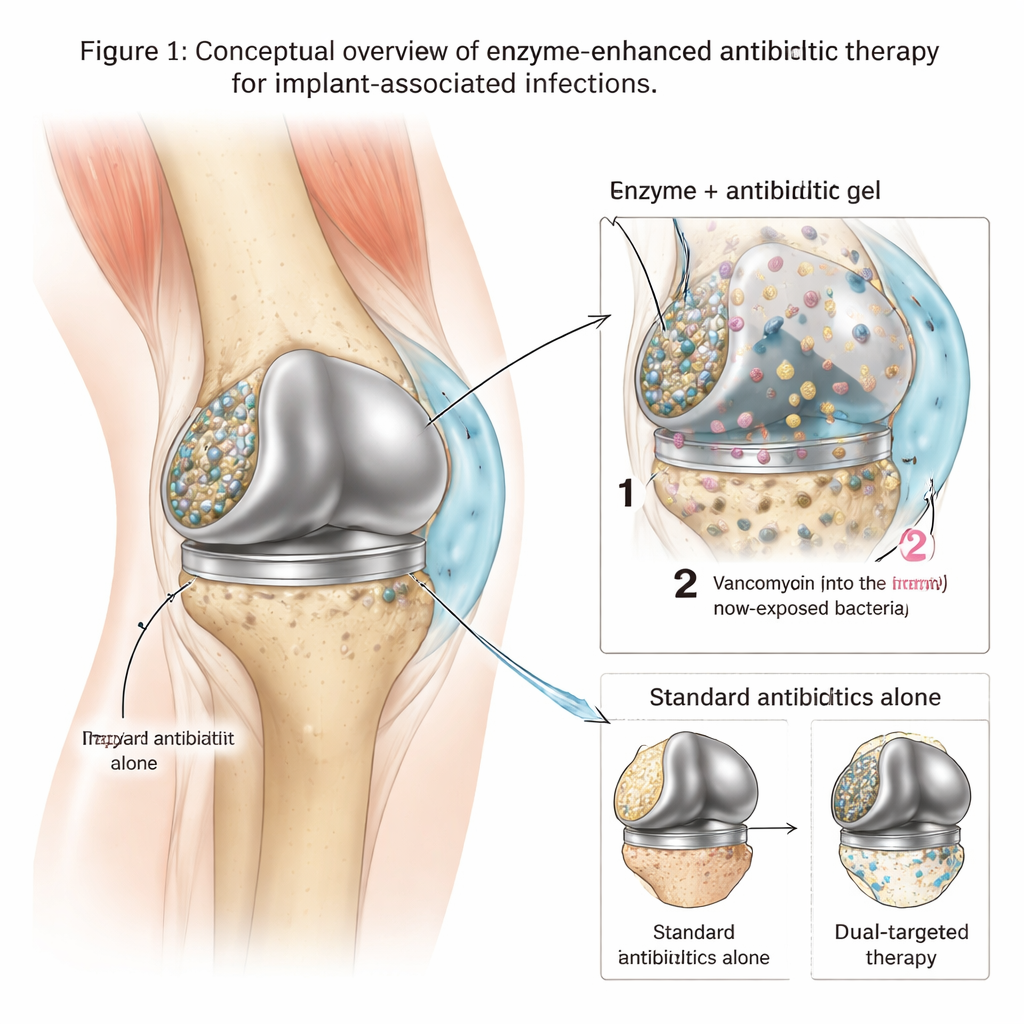
As fortalezas ocultas nos implantes metálicos
Quando bactérias como Staphylococcus aureus resistente à meticilina (MRSA) se aderem a uma articulação artificial, elas rapidamente constroem uma matriz pegajosa de DNA, açúcares e outras moléculas sobre a superfície metálica. Dentro desse biofilme protegido, as bactérias crescem devagar, mudam seu comportamento e podem tolerar níveis de antibiótico centenas ou até milhares de vezes maiores do que aqueles que matam microrganismos em suspensão. Como resultado, tratamentos padrão — mesmo com fármacos potentes como a vancomicina — frequentemente não conseguem eliminar completamente a infecção, obrigando pacientes a cirurgias repetidas ou à substituição total do implante. Os médicos precisam de ferramentas que não apenas matem as bactérias, mas também abram a fortaleza protetora para que os medicamentos possam alcançá‑las.
Um gel inteligente que libera enzimas e antibióticos
Os pesquisadores desenvolveram um tratamento local baseado em um hidrogel termossensível feito a partir de um composto chamado poloxâmero 407. Esse gel é líquido quando frio, facilitando a injeção ao redor de um implante, mas rapidamente se transforma em um sólido macio à temperatura corporal, ajudando‑o a permanecer no lugar. Nesse gel, a equipe carregou dois ingredientes-chave: um antibiótico potente (vancomicina) e um coquetel de três enzimas que cortam os principais componentes da matriz do biofilme. Em testes de laboratório, ajustaram o gel para que as enzimas sejam liberadas primeiro — afrouxando e afinando o biofilme — enquanto a vancomicina é liberada mais lentamente ao longo de vários dias, mantendo níveis locais de medicamento muito altos exatamente onde as bactérias vivem.
De placas de laboratório a cobaias
Para verificar se a estratégia realmente funcionava, a equipe testou primeiro em biofilmes cultivados em pedaços de titânio no laboratório e depois em um modelo com porquinhos-da-índia que imita implantes infectados. In vitro, duas aplicações do gel enzimático‑antibiótico, com 48 horas de intervalo, reduziram o número de bactérias vivas nas superfícies metálicas em mais de 100.000 vezes e quase eliminaram a massa do biofilme. Nos animais, os pesquisadores colocaram cirurgicamente caixas perfuradas contendo esferas de titânio sob a pele, infectaram‑nas com MRSA e então trataram com diferentes combinações de antibióticos sistêmicos e géis locais. O regime mais eficaz combinou: (1) o gel local contendo tanto as enzimas quanto a vancomicina, administrado duas vezes, e (2) tratamento sistêmico com vancomicina mais um segundo antibiótico, rifampicina, que é especialmente eficaz em penetrar biofilmes.
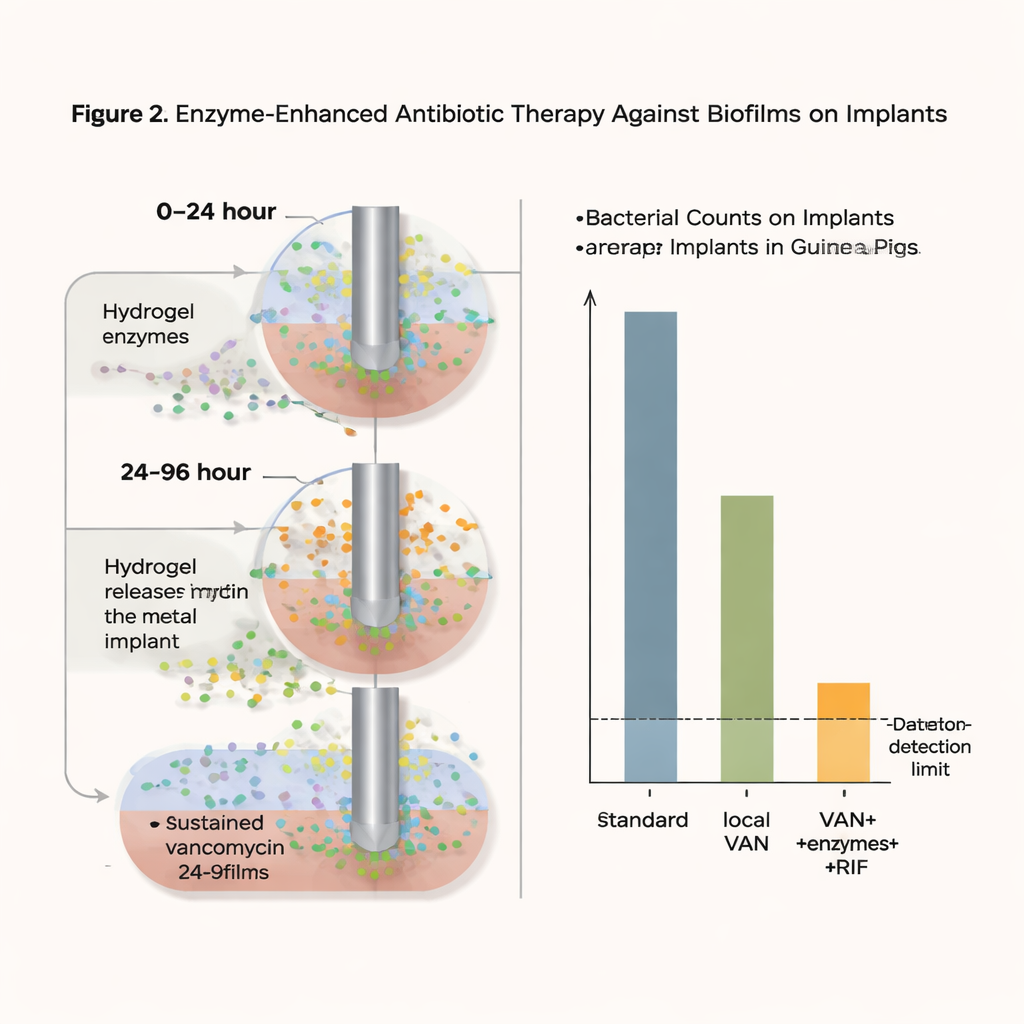
O que a nova abordagem alcançou
Com essa estratégia intensiva, mas localizada, as contagens bacterianas no material do implante caíram até o limite de detecção — efetivamente “sem bactérias recuperáveis” neste modelo — em 75% das caixas tratadas um dia após o término da terapia, e em 37,5% mesmo cinco dias depois. Importante, não foi observada elevação na resistência à vancomicina, e os altos níveis locais de vancomicina parecem ter prevenido o surgimento de cepas resistentes à rifampicina. Testes de segurança usando células em cultura e um modelo de pele humana reconstruída não encontraram sinais de toxicidade ou irritação pelas formulações do gel. Embora um leve recrescimento bacteriano ainda tenha ocorrido em alguns casos e o período de tratamento tenha sido mais curto do que o que os pacientes normalmente recebem, os resultados mostram que combinar enzimas que desestruturam biofilmes com liberação local sustentada de antibiótico pode diminuir dramaticamente infecções que de outra forma seriam persistentes.
O que isso pode significar para os pacientes
Para pessoas enfrentando infecções relacionadas a implantes, este trabalho aponta para um futuro em que cirurgiões possam injetar um gel inteligente ao redor de uma articulação infectada, em vez de remover ou substituir imediatamente o dispositivo. Ao primeiro enfraquecer o escudo do biofilme e depois inundar a área com doses altas e sustentadas de antibióticos — apoiadas por tratamento sistêmico — essa estratégia de alvo duplo visa reduzir as populações bacterianas a níveis indetectáveis e diminuir o risco de resistência. Embora sejam necessários mais estudos, tratamentos mais prolongados e ensaios em humanos, a abordagem oferece um plano promissor para transformar algumas das infecções ortopédicas mais persistentes em problemas mais gerenciáveis e potencialmente curáveis.
Citação: Buzisa Mbuku, R., Poilvache, H., Maigret, L. et al. Enzymes-enhanced antibiotic therapy reduces biofilms to undetectable levels in an implant-associated infection model. npj Biofilms Microbiomes 12, 44 (2026). https://doi.org/10.1038/s41522-026-00910-2
Palavras-chave: infecção por biofilme, implantes ortopédicos, vancomicina, terapia enzimática, rifampicina