Clear Sky Science · pt
Uma exploração teórica de protocolos para tratar infecções de articulações protéticas com combinações de antibióticos e bacteriófagos
Por que as infecções em implantes articulares importam
Substituições de quadril e joelho transformaram a vida de milhões, permitindo que as pessoas caminhem sem dor. Mas quando bactérias colonizam essas articulações artificiais, elas podem formar comunidades viscosas chamadas biofilmes que aderem firmemente a superfícies de metal e plástico. Uma vez estabelecido, um biofilme costuma resistir às doses normais de antibióticos e às defesas imunológicas do corpo, às vezes forçando os pacientes a se submeterem a novas cirurgias. Este estudo investiga se acrescentar vírus que atacam especificamente bactérias — chamados bacteriófagos, ou fagos — aos antibióticos padrão pode oferecer uma forma melhor de tratar essas infecções persistentes.
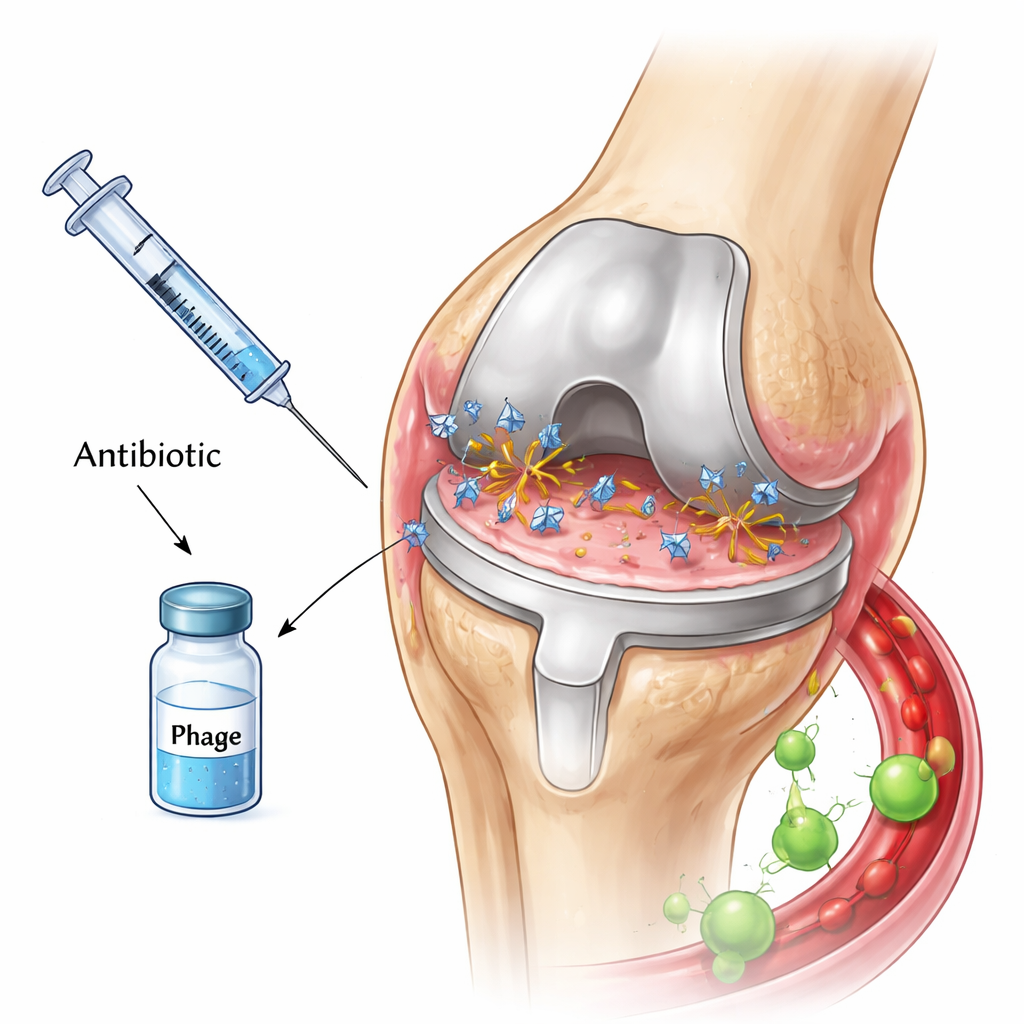
Vírus minúsculos que caçam bactérias
Os fagos são predadores naturais de bactérias. Eles se prendem à célula bacteriana, injetam seu material genético, transformam a célula em uma fábrica de vírus e, por fim, a rompem, liberando uma enxurrada de novos fagos. Alguns fagos também carregam enzimas que podem degradar o material pegajoso que envolve os biofilmes, potencialmente abrindo camadas protetoras que protegem as bactérias dos medicamentos. Por causa dessas características, muitos pesquisadores esperam que combinar fagos com antibióticos possa fornecer um golpe duplo poderoso contra infecções de articulações protéticas, especialmente quando as bactérias se tornam resistentes aos fármacos.
Construindo infecções dentro de um computador
Em vez de ir diretamente a experimentos em animais ou ensaios clínicos, os autores primeiro construíram um modelo matemático e computacional detalhado de uma infecção em articulação protética. Seu sistema virtual tinha duas zonas principais: bactérias em suspensão nos fluidos do corpo e bactérias embutidas em um biofilme na superfície do implante. O modelo também acompanhou células imunes, nutrientes para o crescimento bacteriano, antibióticos e fagos, todos entrando e saindo da articulação. Ao alterar condições como dose do fármaco, cronograma e a presença de bactérias resistentes a antibióticos, eles puderam explorar muitas estratégias de tratamento que seriam difíceis, lentas ou caras de testar em pacientes reais.
Quando os remédios funcionam sozinhos e em conjunto
As simulações mostraram que nem o sistema imunológico nem os antibióticos, isoladamente, eliminavam facilmente infecções por biofilme. Os antibióticos reduziram fortemente as bactérias em suspensão, mas fizeram pouco efeito sobre a população no biofilme. Os fagos puderam inicialmente controlar a infecção de forma mais eficaz, mas introduziram ciclos de explosão e colapso: à medida que os fagos matavam bactérias, suas presas se tornavam escassas demais, fazendo com que os números de fagos caíssem e permitindo a recuperação bacteriana. Quando antibióticos e fagos foram administrados ao mesmo tempo, o antibiótico tendia a dominar o resultado, e a adição de fagos muitas vezes fez pouco mais do que o antibiótico já conseguia sozinho.
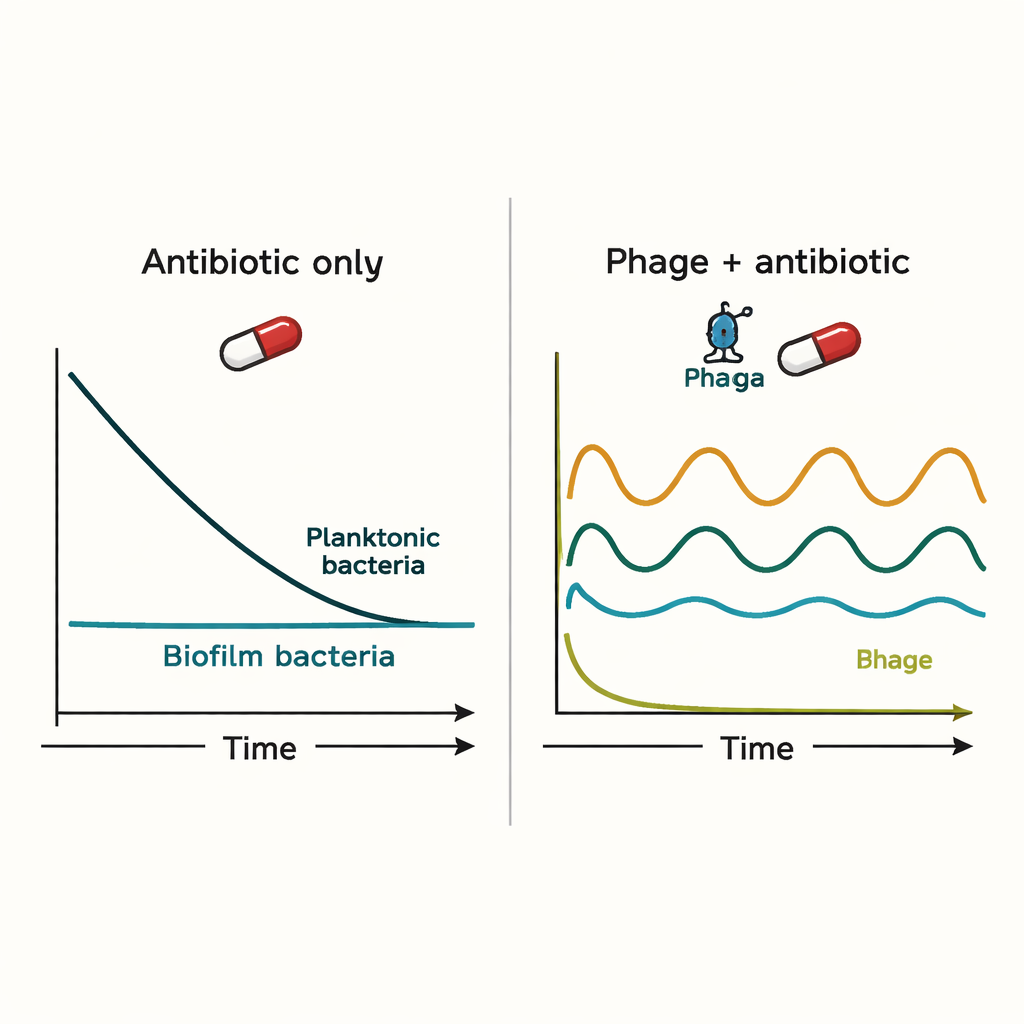
O papel especial do tempo e da resistência
O modelo ficou mais promissor quando incluíram bactérias resistentes a antibióticos. Os fagos puderam atacar essas células resistentes, às vezes eliminando-as completamente. Se o tratamento com fagos fosse iniciado primeiro e os antibióticos fossem adicionados algumas horas depois, a estratégia combinada reduziu as bactérias em suspensão por muitas ordens de magnitude e eliminou subpopulações resistentes nas simulações. Ainda assim, as bactérias associadas ao biofilme não foram completamente erradicadas; em vez disso, seus números foram mantidos em níveis mais baixos que poderiam ser mais fáceis de o sistema imunológico controlar. Isso sugere que os fagos podem ser mais úteis não como balas mágicas, mas como auxiliares que previnem a resistência e mantêm as infecções sob controle.
O que isso significa para pacientes e médicos
Para pessoas com um implante articular infectado, este trabalho oferece tanto cautela quanto promessa. O modelo sugere que simplesmente adicionar fagos aos antibióticos padrão provavelmente não curará por si só infecções profundas por biofilme. No entanto, os fagos ainda podem ser ferramentas valiosas: eles podem ajudar a eliminar bactérias resistentes a antibióticos e reduzir o número total de microrganismos o suficiente para que o corpo dê conta, especialmente se usados antes ou sincronizados com cuidado com os antibióticos. Os autores enfatizam que estas são previsões teóricas, não provas clínicas. A principal mensagem é que experimentos bem planejados — guiados por modelos como este — são necessários para descobrir quando a terapia com fagos pode realmente melhorar os desfechos de pacientes com infecções de articulações protéticas.
Citação: Levin, B.R., Gil-Gil, T., Berryhill, B.A. et al. A theoretical exploration of protocols for treating prosthetic joint infections with combinations of antibiotics and bacteriophage. npj Biofilms Microbiomes 12, 51 (2026). https://doi.org/10.1038/s41522-025-00908-2
Palavras-chave: infecção de articulação protética, biofilme, terapia com bacteriófagos, resistência a antibióticos, modelagem matemática