Clear Sky Science · pt
Estágios da formação de condensados biomoleculares na montagem pró-β-carboxissoma
Por que fábricas de carbono minúsculas importam
As cadeias alimentares da Terra dependem da fotossíntese, mas a enzima-chave que captura dióxido de carbono (CO2) do ar, a Rubisco, é lenta e facilmente confundida pelo oxigênio. As cianobactérias — microrganismos fotossintéticos microscópicos — resolveram esse problema há muito tempo construindo “micro-fábricas” proteicas chamadas carboxissomas, que aprisionam CO2 ao redor da Rubisco. Este estudo desvenda como um complexo adaptador crucial, composto por proteínas chamadas ApN e CM, se auto‑monta em etapas para ajudar a construir um carboxissoma funcional. Compreender essa coreografia pode orientar esforços para instalar sistemas semelhantes de aumento de CO2 em plantas cultivadas e elevar rendimentos.
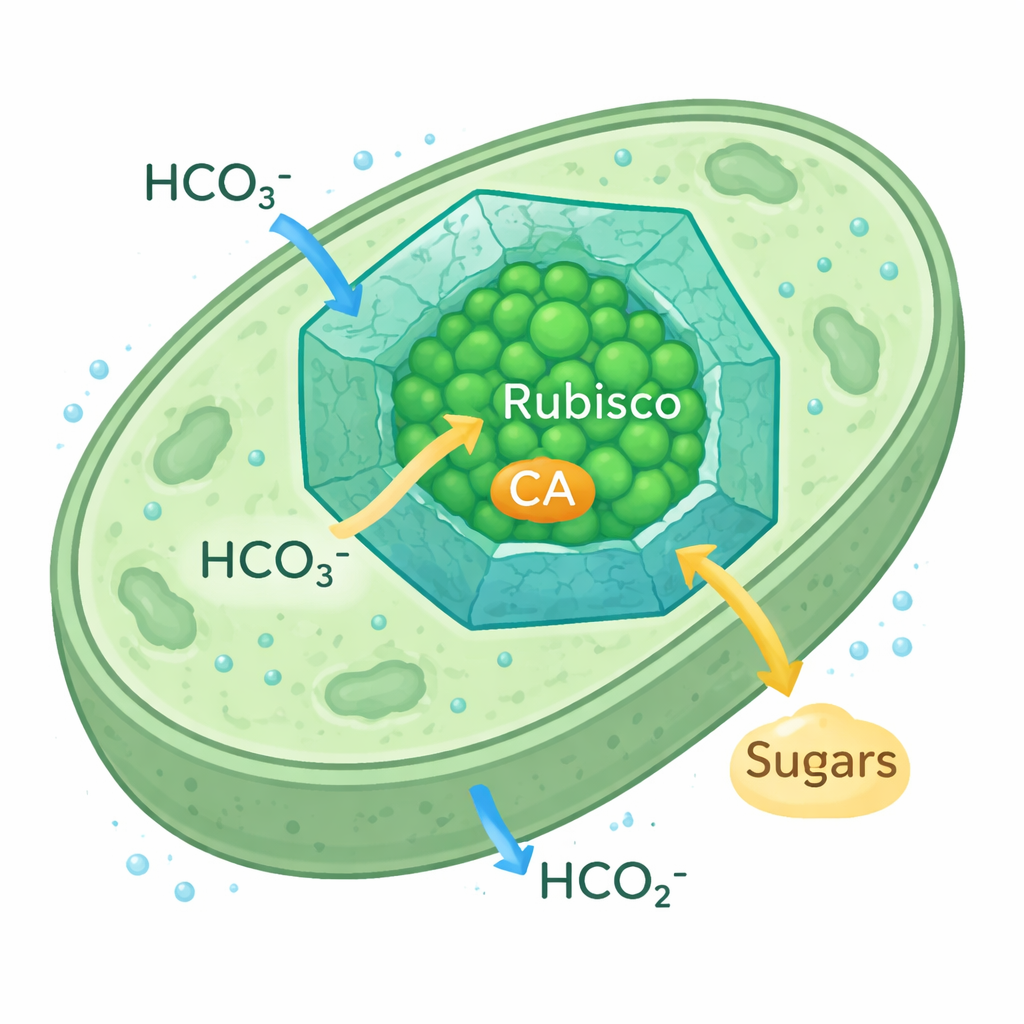
Como micróbios turbinaram a captura de carbono
Os carboxissomas de cianobactérias são minúsculos compartimentos proteicos icosaédricos que ficam dentro da célula. Sua casca proteica permite a entrada de íons bicarbonato enquanto reduz a fuga de CO2, criando uma bolha rica em CO2 ao redor da Rubisco e de sua enzima parceira, a anidrase carbônica (CA), que converte bicarbonato em CO2. Esse mecanismo de concentração de CO2 permite que as cianobactérias prosperem mesmo quando o CO2 ambiental é escasso. Como a forma de Rubisco usada nesses carboxissomas se assemelha à Rubisco de plantas, os pesquisadores os veem como um modelo realista para reengenharia de cloroplastos vegetais visando capturar carbono com mais eficiência.
A peça do quebra‑cabeça que se conecta à casca
Antes de a casca proteica rígida se formar, as cianobactérias primeiro constroem um condensado macio, com aparência de gotícula, chamado “pró‑carboxissoma”. Trabalhos anteriores mostraram que uma proteína andaime chamada CM reúne Rubisco e CA nessa gotícula. A peça que faltava era como a proteína adaptadora de casca ApN se integra a essa estrutura e depois se conecta às proteínas da casca. Os autores descobriram que quando ApN é produzida sozinha ela forma um feixe de quatro partes que ignora os outros componentes do carboxissoma. Nesse estado, ApN não pode ser incorporada às gotículas com Rubisco, CM e CA, sugerindo que uma forma diferente de ApN deve ser utilizada durante a montagem real do carboxissoma.
Adaptadores co‑construídos e um interruptor redox
Ao observar a organização genética nas cianobactérias, a equipe notou que apn fica diretamente após cm no mesmo operon, de modo que as duas proteínas geralmente são produzidas juntas. Imitando isso em bactérias, eles co‑expressaram ApN e CM a partir de um mesmo trecho de DNA. Nestas condições, ApN deixou de formar um tetrâmero independente. Em vez disso, três subunidades de ApN e uma subunidade de CM montaram‑se em um complexo adaptador específico de quatro partes, denominado (ApN)3:CM. Esse heterocomplexo ligava‑se prontamente à Rubisco, CA e CM e podia entrar em condensados. Modelagem estrutural e crio‑microscopia eletrônica mostraram que ApN e CM se encontram através de uma interface “língua‑e‑entalhe” finamente ajustada; quando resíduos-chave de ApN nessa interface eram mutados, o adaptador não se formava e as células falhavam em construir carboxissomas adequados.
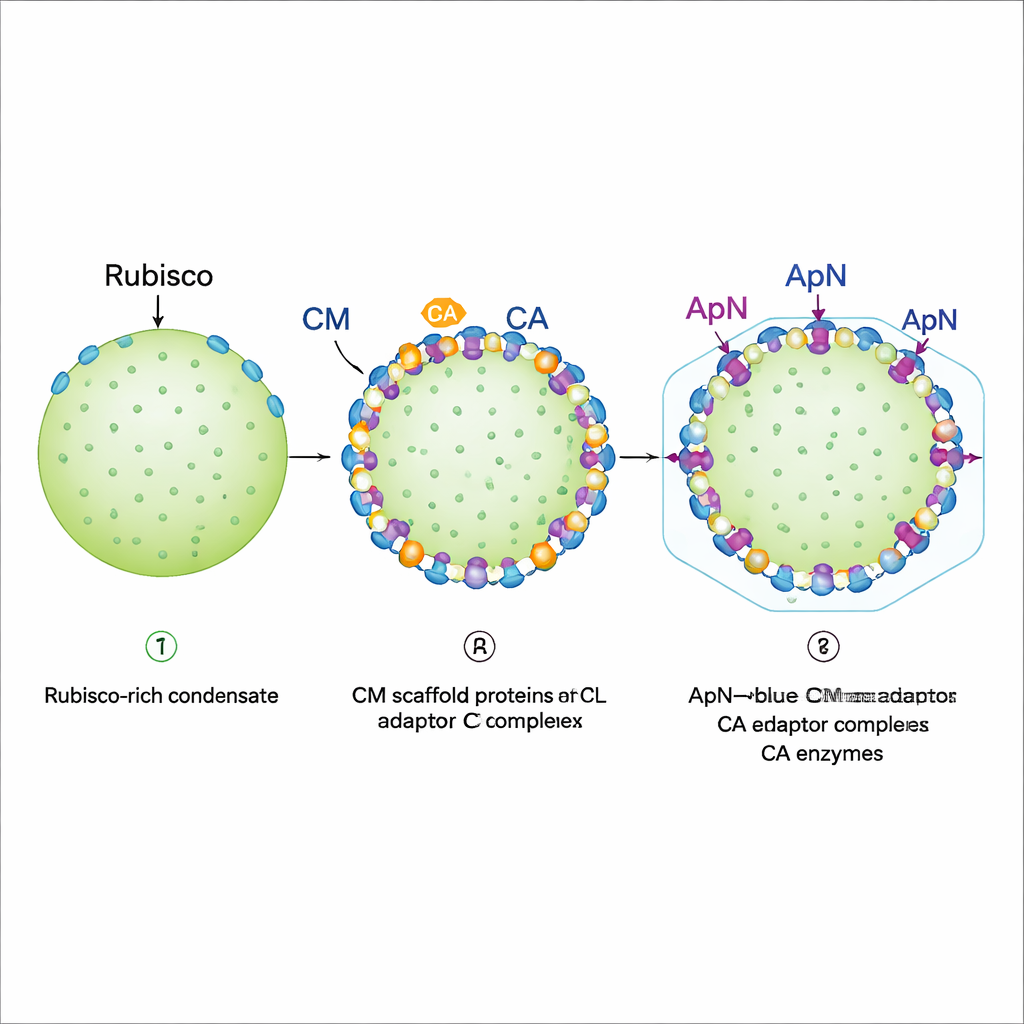
Posicionamento na borda e preparo para a casca
Imagens por fluorescência de gotículas reconstituídas revelaram um programa de montagem em etapas. Primeiro, Rubisco, CM de comprimento total e uma variante mais curta de CM formam um condensado denso que se comporta como um gel: Rubisco fica essencialmente preso no lugar. Em seguida, CA e o complexo (ApN)3:CM são adicionados. Ambos preferencialmente se assentam na borda externa da gotícula existente, desde que a CA chegue antes ou junto com (ApN)3:CM. Essa localização periférica é crucial porque a cauda de ApN carrega um “peptídeo de encapsulação” que se liga às proteínas da casca. Os autores também descobriram um interruptor redox incorporado: conforme o interior do carboxissoma em maturação se torna mais oxidante, duas cisteínas conservadas em ApN podem ser oxidadas, empurrando o adaptador de um tetrâmero (ApN)3:CM para um trimero (ApN)2:CM. Em células cianobacterianas vivas, alterar essas cisteínas retardou o crescimento e produziu carboxissomas sobredimensionados, mas ainda funcionais, ressaltando seu papel no ajuste fino da maturação.
Lições para construir culturas melhores
Para um não especialista, esses detalhes moleculares podem soar arcanos, mas resumem‑se a uma mensagem simples: tempo e parceria importam. O trabalho mostra que ApN deve ser co‑produzida com CM para evitar formar um aglomerado inútil por conta própria e, em vez disso, tornar‑se um adaptador que se posiciona na superfície do pró‑carboxissoma, pronto para recrutar a casca. Um passo sensível ao estado redox então ajuda a remodelar esse adaptador à medida que o compartimento se fecha e sua química interna muda. Para engenheiros de plantas que esperam transplantar a maquinaria cianobacteriana de concentração de CO2 para cultivos, o estudo destaca que não basta mover partes individuais; é preciso também respeitar a ordem, as proporções e os gatilhos químicos que orientam a montagem do carboxissoma na natureza.
Citação: Zang, K., Hong, X., Nguyen, N.D. et al. Stages of biomolecular condensate formation in pro-β-carboxysome assembly. Nat. Plants 12, 447–464 (2026). https://doi.org/10.1038/s41477-026-02227-6
Palavras-chave: montagem do carboxissoma, Mecanismo de concentração de CO2 em cianobactérias, condensados de Rubisco, condensados biomoleculares, fotossíntese sintética