Clear Sky Science · pt
Interação entre a acetilação O de ácido siálico no Golgi dependente e independente de SLC33A1 na catálise por CASD1
Como pequenos ajustes de açúcares podem moldar a saúde e a doença
Nossas células são revestidas por cadeias de açúcares complexas que funcionam como carteirinhas moleculares, orientando a imunidade, o desenvolvimento e inclusive como vírus se ligam. Este estudo explora uma modificação sutil, porém poderosa, desses açúcares — a adição de pequenas “tampas” químicas chamadas grupos acetil a um açúcar terminal denominado ácido siálico — e revela uma máquina molecular surpreendente, em duas partes, que controla esse processo dentro do aparelho de Golgi da célula. Entender esse sistema oculto ajuda a explicar certos distúrbios neurológicos graves e oferece pistas sobre como as células regulam finamente suas superfícies em saúde e doença. 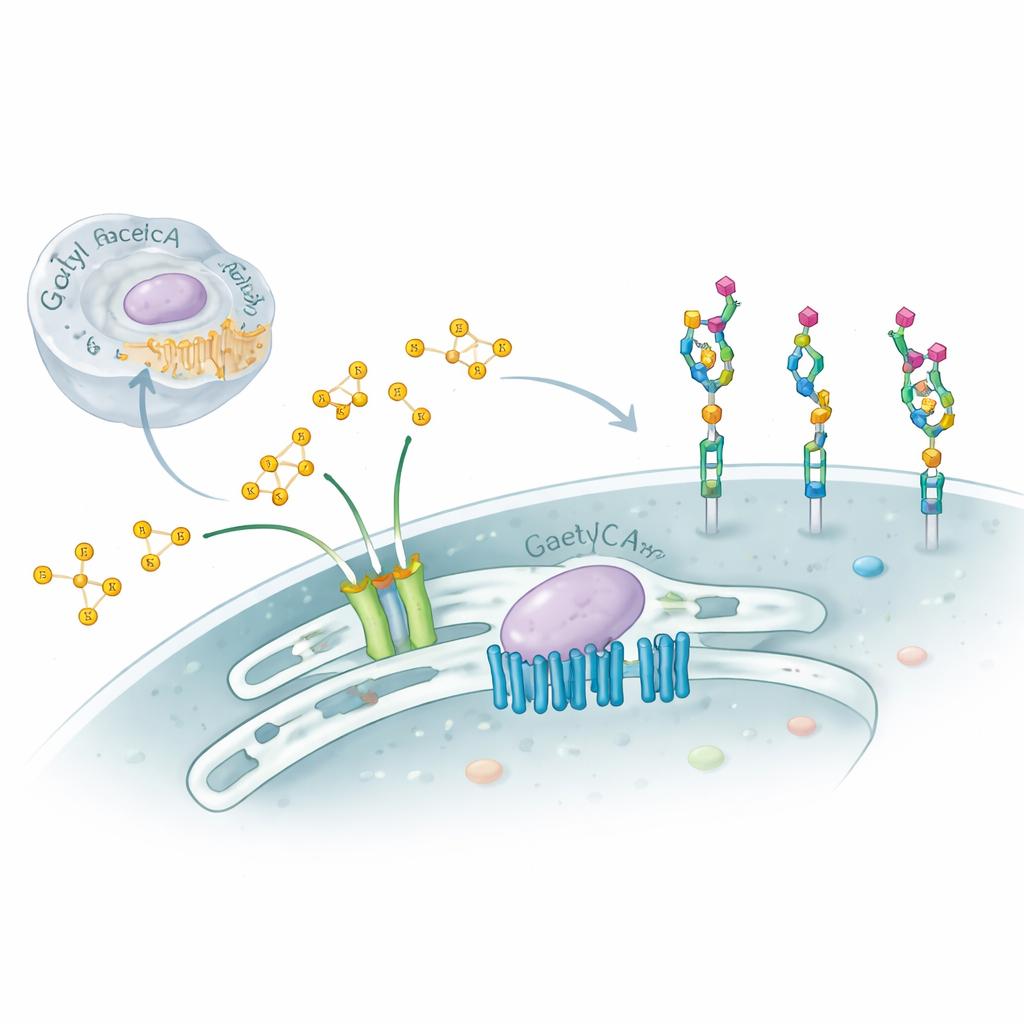
Os açúcares especiais na superfície celular
Os ácidos siálicos ficam nas pontas externas de muitos açúcares de superfície celular em proteínas e lipídios, particularmente em moléculas chamadas gangliosídeos no cérebro. Ao alterar levemente os ácidos siálicos — por exemplo, adicionando um ou dois grupos acetil em posições específicas — as células podem mascarar locais de reconhecimento existentes ou criar novos. Vírus como influenza C e alguns coronavírus buscam especificamente esses açúcares modificados, e gangliosídeos acetilados podem influenciar se neurônios sobrevivem ou morrem, assim como o crescimento de cânceres. No entanto, apesar de sua importância, o funcionamento interno das máquinas celulares que colocam esses grupos acetil no Golgi permaneceu pouco compreendido.
Um transportador e uma enzima atuam em conjunto
Os pesquisadores concentraram‑se em duas proteínas que residem no Golgi ou em suas proximidades: SLC33A1, um transportador que move acetil‑CoA (o principal doador de acetil da célula) através de membranas, e CASD1, uma enzima conhecida por transferir grupos acetil para ácidos siálicos. Usando edição gênica em linhagens celulares humanas e de hamster, eles removeram SLC33A1 e observaram o que aconteceu com gangliosídeos específicos. Células sem SLC33A1 ainda conseguiam produzir os gangliosídeos básicos GD3 e GD2, mas perderam completamente suas formas 9‑O‑acetiladas, uma modificação marcante ligada ao câncer e à função neural. Reintroduzir o SLC33A1 humano restaurou esses gangliosídeos acetilados, mostrando que SLC33A1 é um fornecedor crucial de acetil‑CoA para essa via. 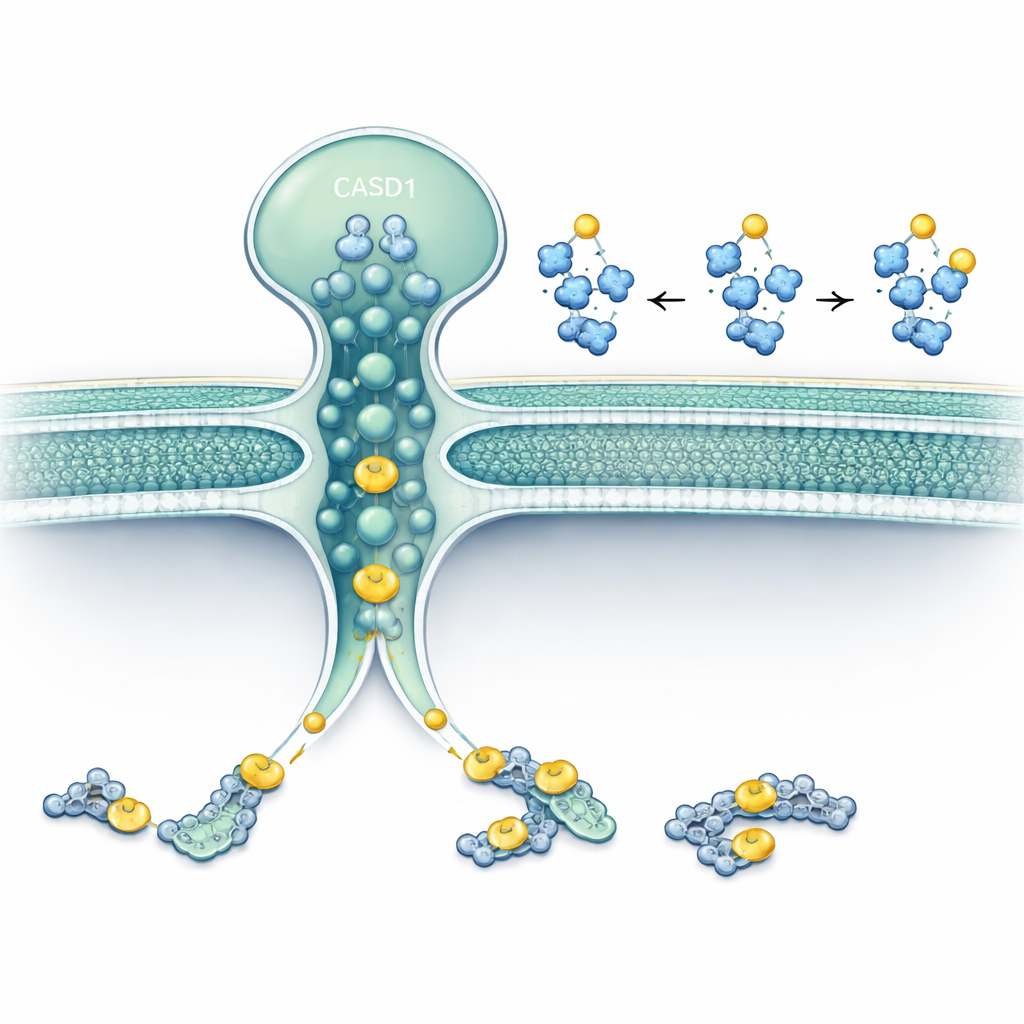
Mutations de pacientes revelam relevância médica
SLC33A1 tem sido implicado em várias condições neurológicas raras, incluindo um transtorno infantil grave (síndrome de Huppke–Brendel), uma forma de paraplegia espástica hereditária e ataxia cerebelar de início tardio. A equipe recriou quatro variantes de SLC33A1 derivadas de pacientes em células sem o transportador normal e testou se essas proteínas alteradas poderiam resgatar a acetilação dos gangliosídeos. Todas as quatro mostraram função reduzida, e as mutações de início infantil mais severas mal restauraram qualquer acetilação. Guiados por uma estrutura tridimensional recentemente resolvida de SLC33A1, os autores mapearam essas mutações na proteína e mostraram como provavelmente elas perturbam sua arquitetura ou sua capacidade de ligar acetil‑CoA. Isso sugere fortemente que a acetilação deficiente de gangliosídeos contribui para os sintomas neurológicos observados nos pacientes.
Um segundo sítio ativo oculto em CASD1
O trabalho também revelou uma reviravolta inesperada: CASD1 parece ser uma enzima de dupla finalidade. Sua porção conhecida no lúmen do Golgi usa acetil‑CoA fornecido por SLC33A1. Mas quando SLC33A1 foi derrubado, as células ainda conseguiam colocar um único grupo acetil em certos ácidos siálicos em algumas condições, embora não conseguissem adicionar o segundo grupo acetil necessário para padrões mais complexos. Usando predição estrutural avançada e simulações moleculares, os autores mostraram que a parte transmembrana de CASD1 se assemelha fortemente a uma acetiltransferase transmembrana conhecida de lisossomos. Eles identificaram aminoácidos chave nessa região que ligam acetil‑CoA do lado citosólico e transmitem seu grupo acetil através da membrana diretamente para o ácido siálico. Quando esses resíduos foram mutados, CASD1 perdeu essa segunda atividade tanto em ensaios in vitro quanto em células vivas.
DuAS rotas, um código de açúcar finamente ajustado
No conjunto, os dados apoiam um modelo de “dois sítios catalíticos”. Uma rota depende de SLC33A1 trazendo acetil‑CoA para o lúmen do Golgi, onde o domínio luminal de CASD1 adiciona um grupo acetil ao ácido siálico, permitindo padrões de acetilação simples e duplos. A outra rota está embutida no núcleo transmembrana de CASD1, que acessa diretamente o acetil‑CoA citosólico e ainda pode realizar um nível básico de acetilação mesmo quando SLC33A1 está ausente. Para um leigo, isso significa que uma única enzima, alimentada por duas fontes diferentes de acetil, escreve sutis “marcas de pontuação” nos açúcares da superfície celular. Quando o transportador ou qualquer parte da enzima está defeituosa, essas marcas ficam deslocadas ou ausentes, o que pode ajudar a explicar certas doenças do desenvolvimento e neurodegenerativas e destaca uma nova camada de regulação na maneira como nossas células moldam sua identidade externa.
Citação: Albers, M., Bosse, L., Schröter, L. et al. Interplay of SLC33A1-dependent and -independent Golgi sialic acid O-acetylation in CASD1 catalysis. Nat Commun 17, 3156 (2026). https://doi.org/10.1038/s41467-026-71333-y
Palavras-chave: ácido siálico, acetilação no Golgi, gangliosídeos, SLC33A1, CASD1