Clear Sky Science · pt
Dinâmica estrutural do midnolin-proteassoma durante a degradação de substratos independente de ubiquitina
Como as células eliminam o lixo às pressas
Dentro de cada célula, proteínas estão continuamente sendo sintetizadas e degradadas. Muitas recebem pequenas etiquetas chamadas ubiquitina antes de serem encaminhadas para a principal máquina de reciclagem da célula, o proteassoma. Mas algumas proteínas nucleares precisam ser removidas tão rapidamente que não há tempo para essa marcação. Este estudo revela como uma proteína auxiliar pouco conhecida, o midnolin, se encaixa diretamente no proteassoma para eliminar esses alvos urgentes, oferecendo pistas sobre como as células mantêm a atividade gênica sob controle estrito e rápido.
Um atalho para o triturador celular
O proteassoma 26S é um complexo em forma de barril que fragmenta proteínas em pedaços pequenos. Tradicionalmente, ele reconhece os alvos lendo cadeias de ubiquitina anexadas a eles. Trabalhos recentes revelaram uma rota alternativa: um caminho de “atalho” no qual o midnolin escolta certas proteínas nucleares — especialmente produtos de genes de resposta imediata que ligam e desligam genes rapidamente — diretamente ao proteassoma sem qualquer etiqueta de ubiquitina. Essas proteínas, como fatores de transcrição envolvidos em respostas ao estresse e inflamação, precisam aparecer e desaparecer em questão de minutos. O novo artigo combina microscopia crioeletrônica de alta resolução com experimentos bioquímicos para mapear, quase quadro a quadro, como o midnolin se prende ao proteassoma e posiciona sua carga para destruição.
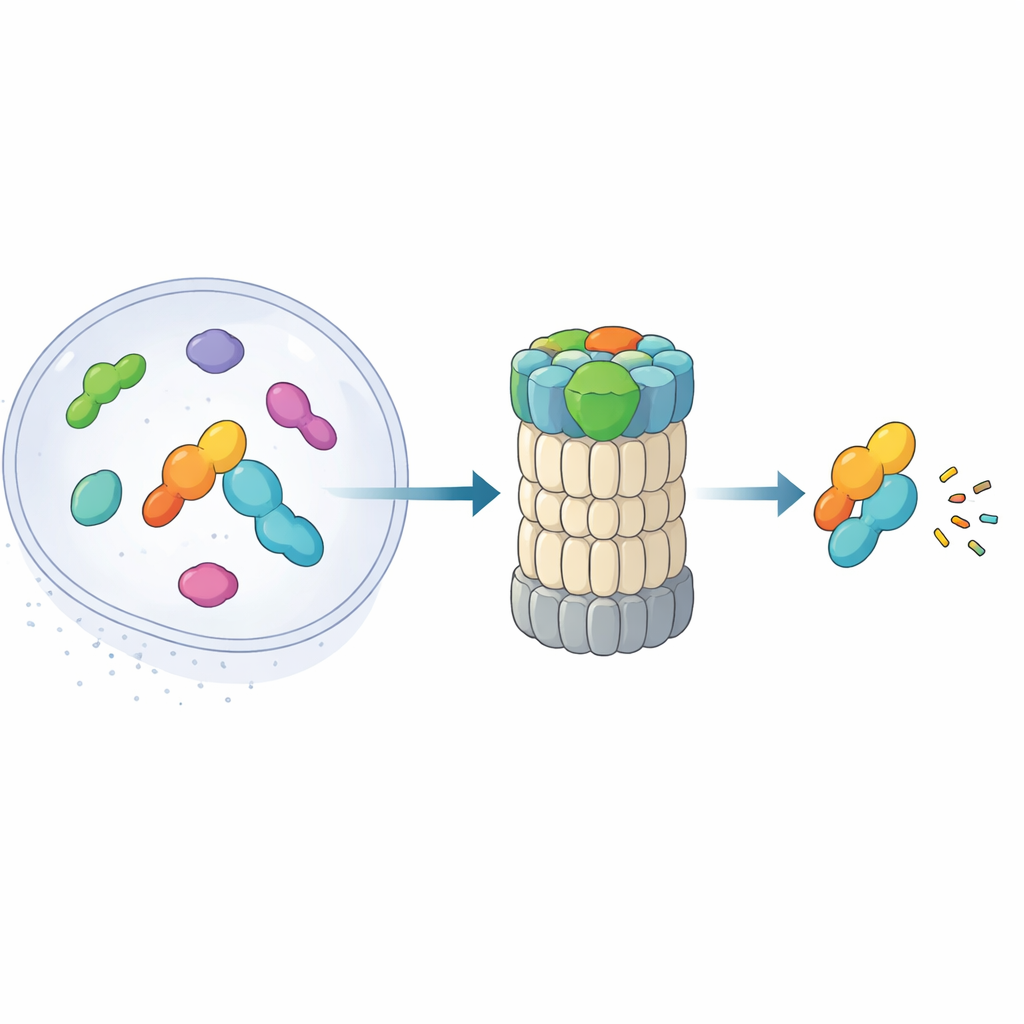
O ajudante em três partes que agarra e aponta os alvos
O midnolin funciona como uma ferramenta multifuncional com três módulos principais. Uma das extremidades, uma hélice C-terminal, se encaixa em um sítio de ancoragem de um componente do proteassoma chamado RPN1, fixando o midnolin à máquina de reciclagem. Uma região central, o “Catch”, reconhece e segura uma característica filamentosa específica (um degron) nas proteínas-alvo. Na extremidade oposta fica um domínio semelhante à ubiquitina. Surpreendentemente, esse domínio não serve principalmente para ligar o proteassoma, como ocorre em outras proteínas transportadoras. Em vez disso, os autores mostram que ele se apoia contra a RPN11, uma enzima que normalmente remove ubiquitina dos substratos. Aqui, a RPN11 atua mais como um andaime: ao envolver o segmento semelhante à ubiquitina do midnolin, ajuda a manter o domínio Catch e sua carga diretamente acima do estreito poro de entrada do proteassoma.
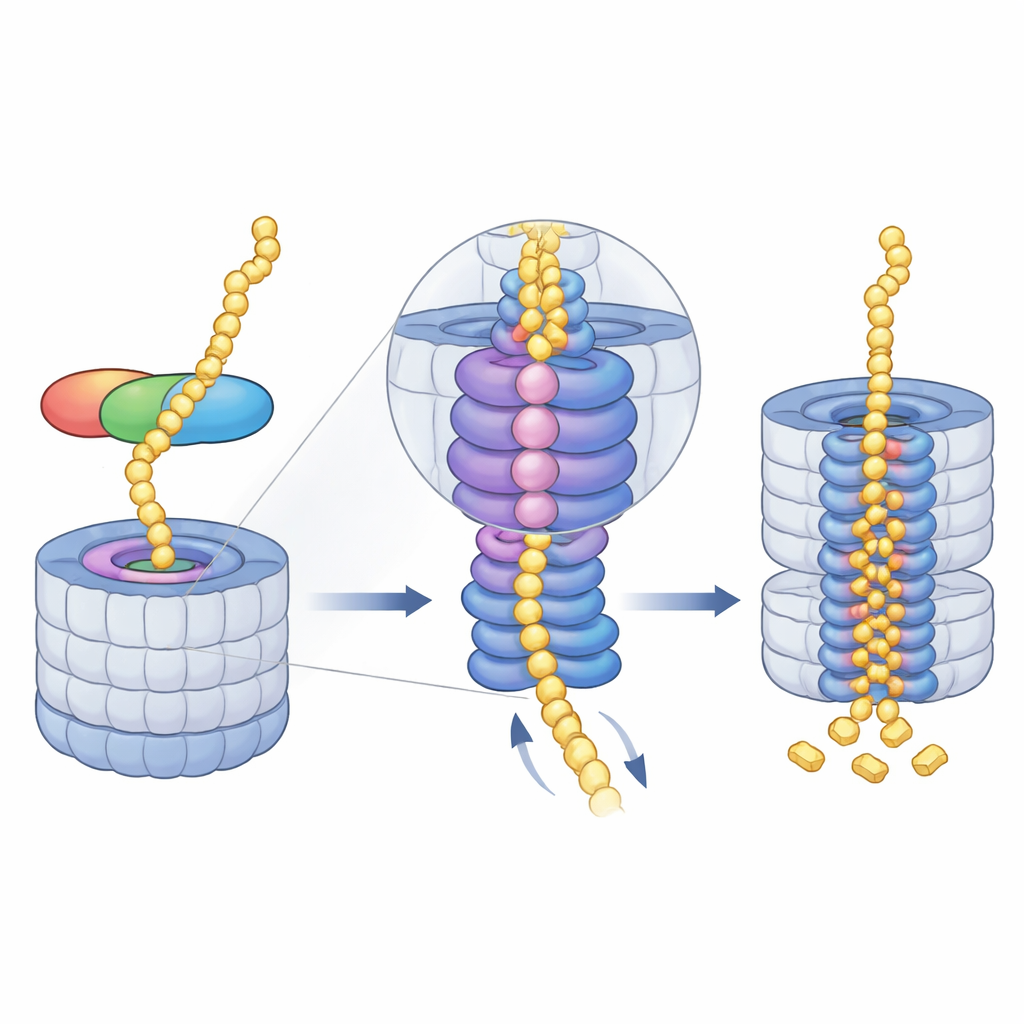
Guiando a proteína para o núcleo triturador
Uma vez que o midnolin esteja ancorado, o motor energético do proteassoma — um anel AAA+ ATPase — assume o controle. Esse anel fica logo abaixo do poro de entrada e puxa cadeias de proteínas desenoveladas para o núcleo, passo a passo. As imagens de crio-ME revelam uma série de posições em “escada espiral” adotadas pelas seis subunidades do motor enquanto elas agarram e transferem o substrato pelo canal central. Os autores capturaram quatro estágios consecutivos desse ciclo, todos com material ligado ao midnolin passando pelo poro, e até observaram como a liberação de um íon magnésio em uma subunidade coincide com um deslocamento para baixo de todo o anel. Isso sugere que o uso coordenado de ATP e a liberação de magnésio ajudam a catratar (ratchet) a proteína mais profundamente na câmara onde residem os sítios de clivagem.
Por que posicionamento e coexpressão importam
A equipe testou como cada módulo do midnolin contribui para a eficiência. A hélice de ancoragem sozinha pode ligar-se à RPN1, mas não melhora significativamente a atividade do proteassoma. Remover o domínio Catch deixa muitos proteassomas presos em um estado ocioso, sem substrato, mesmo que o midnolin ainda possa se anexar; substituir o Catch por um substrato permanentemente fundido também falha em restaurar a atividade completa. Essas descobertas indicam que o Catch faz mais do que apenas agarrar o alvo — ele também deve orientar a proteína com precisão na entrada do poro. Dados bioquímicos e transcriptômicos de tumores mostram ainda que o midnolin tende a ser produzido em conjunto com seus substratos. Quando coexpresso, o midnolin dobra-se melhor e forma complexos estáveis, criando um pacote “me degrade” pronto para ser entregue rapidamente ao proteassoma quando a célula precisa redefinir a expressão gênica.
Auto-limpeza e possibilidades médicas futuras
Depois que a proteína-alvo é puxada e fragmentada, o próprio midnolin não é poupado. Suas regiões não estruturadas podem ser conduzidas pelo motor e alimentadas na mesma câmara de destruição, garantindo que o auxiliar não se acumule desnecessariamente. Ao iluminar essa via sem ubiquitina para o proteassoma, o estudo amplia nossa compreensão de como as células gerenciam a vida útil das proteínas em cronogramas extremamente apertados. Também sugere novas estratégias terapêuticas: ao projetar moléculas baseadas em midnolin que prendam diretamente proteínas nucleares causadoras de doenças ao proteassoma, os pesquisadores podem um dia ser capazes de eliminar alvos “intratáveis”, incluindo certos oncogenes, de forma mais rápida e seletiva.
Citação: Zhu, C., Qin, L., Dai, Z. et al. Structural dynamics of the midnolin-proteasome during ubiquitin-independent substrate turnover. Nat Commun 17, 2800 (2026). https://doi.org/10.1038/s41467-026-71002-0
Palavras-chave: proteassoma, midnolin, degradação de proteínas, via independente de ubiquitina, genes de resposta imediata