Clear Sky Science · pt
A competência transcricional define o potencial de nucleação de heterocromatina de unidades MSR isoladas
Interruptores ocultos em nosso DNA
Os nossos genomas estão compactados dentro do núcleo celular em dois estados principais: regiões ativas que abrigam genes e trechos densamente empacotados que durante muito tempo foram considerados “matéria escura” genética. Este estudo parte de uma pergunta aparentemente simples: o que determina que um trecho de DNA se torne esse material fortemente compactado e silenciador de genes — conhecido como heterocromatina — em primeiro lugar? Ao dissecar uma classe específica de DNA repetitivo em camundongos, os autores revelam que nem todas as repetições são iguais: apenas aquelas capazes de suportar um tipo especial de transcrição conseguem acionar o interruptor que constrói e mantém esses bairros silenciosos do DNA.
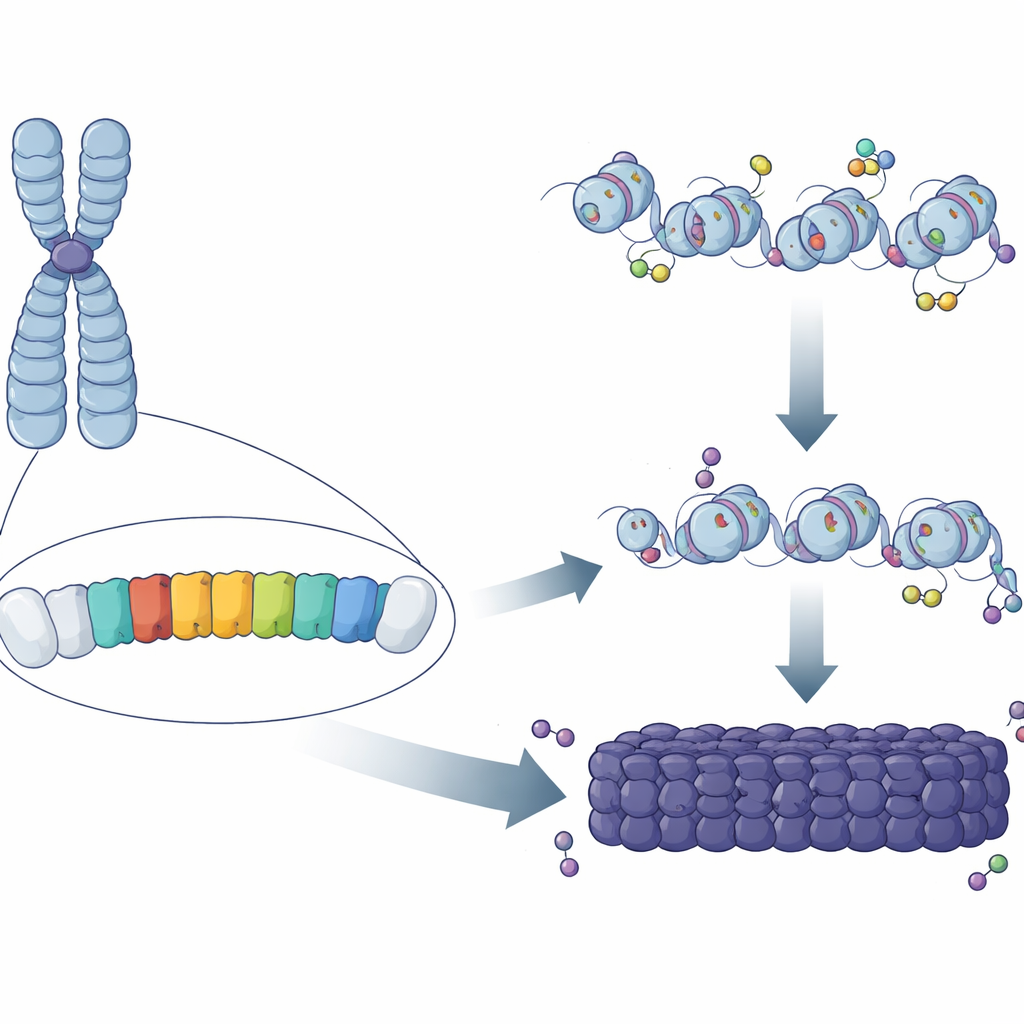
Padrões repetidos no genoma
Quase metade do DNA de mamíferos é composta por sequências repetidas, muitas delas agrupadas em regiões ao redor do centrômero. Em camundongos, um componente importante dessas regiões é o “major satellite repeat” (MSR), uma sequência curta rica em A/T copiada centenas de milhares de vezes. Trabalhos clássicos mostraram que essas regiões são revestidas por marcas químicas e proteínas que trancam o DNA num estado compacto e protetor. Mas permanecia misterioso por que algumas cópias de MSR se tornavam totalmente heterocromáticas enquanto outras, dispersas em outras partes do genoma, não. Os autores propuseram que pequenas diferenças na sequência ou no comportamento de unidades individuais de MSR poderiam determinar se elas conseguem semear, ou “nucleear”, um pedaço de heterocromatina.
Construindo um sítio-teste no genoma
Para testar essa ideia de forma limpa, a equipe projetou células-tronco embrionárias de camundongo contendo uma plataforma de inserção artificial em um trecho silencioso do cromossomo 2 — uma região sem genes ou repetições próximas e sem atividade detectável. Nesse sítio neutro, inseriram diferentes fragmentos de DNA: unidades MSR intactas, variantes MSR fortemente embaralhadas e elementos de controle como promotores virais ou trechos de elementos móveis. Isso lhes permitiu avaliar, unidade por unidade, quais sequências conseguem atrair as características marcantes da heterocromatina: uma marca química específica nas histonas (H3K9me3), ligação das proteínas HP1 e incorporação da histona ligadora H1, que em conjunto engrossam e estabilizam a cromatina local.
Apenas repetições prontas para transcrever semeiam cromatina silenciosa
Os resultados foram notavelmente seletivos. Uma única unidade MSR intacta inserida no sítio-teste não foi suficiente para alterar a cromatina. No entanto, três ou mais cópias tandem da sequência MSR intacta converteram a região circundante em uma “ilha” de heterocromatina, com H3K9me3 forte, HP1 e histona H1. Em contraste, trechos de comprimento equivalente compostos por MSR embaralhado, ou por outro tipo de repetição (região não traduzida 5' do LINE-1), não conseguiram produzir o mesmo efeito, mesmo podendo dirigir transcrição intensa. A diferença-chave foi que unidades MSR intactas em multicópia suportavam uma transcrição modesta e bidirecional que gerava pequenas moléculas de RNA não convencionais fortemente associadas à cromatina. Esse padrão, mais do que uma transcrição alta e semelhante à gênica, correlacionou-se com a capacidade de nucleação da heterocromatina.
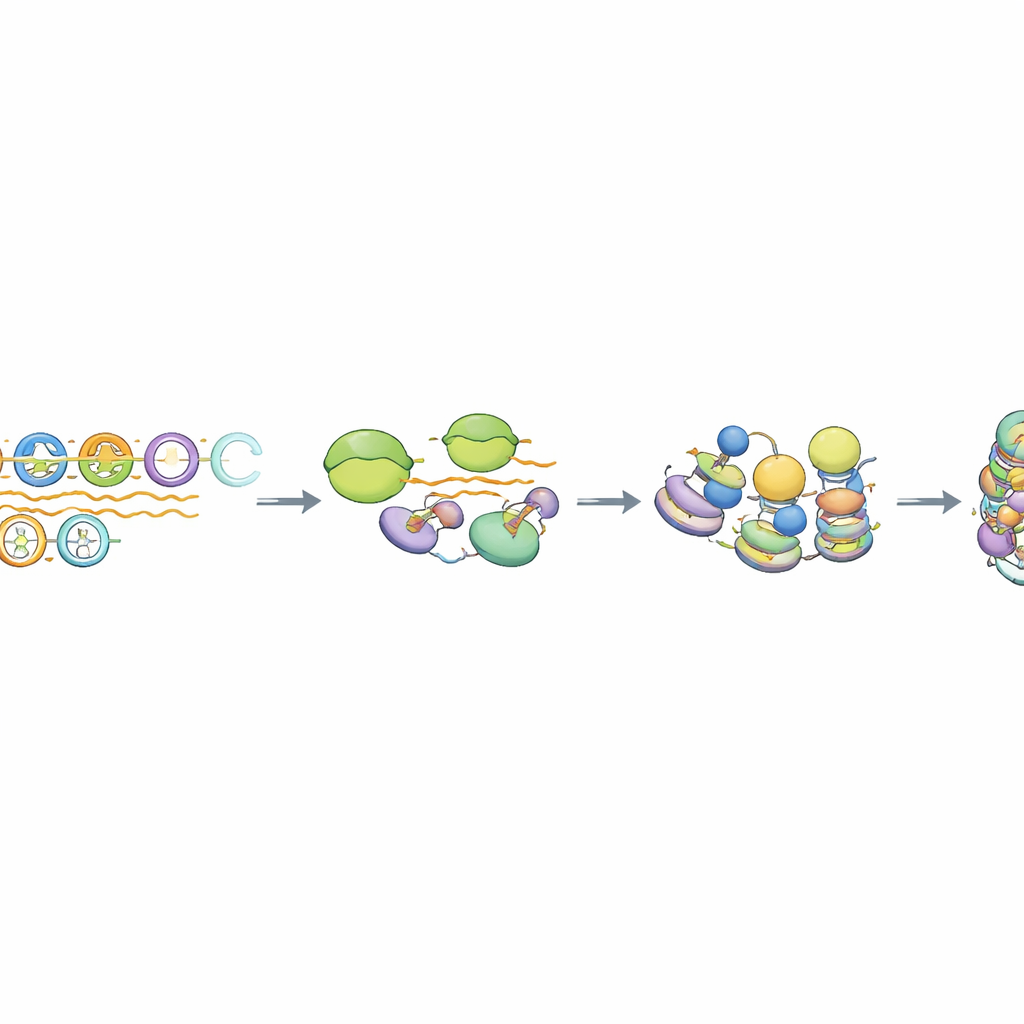
Um tipo especial de transcrição e processamento de RNA
Ao investigar mais a fundo, os autores descobriram que a RNA polimerase II, a enzima que normalmente produz RNA mensageiro, envolve-se brevemente com os arrays de MSR, mas não prossegue eficientemente em longos transcriptos. Os RNAs resultantes carecem de marcas típicas de mRNA, como a capa 5' protetora e longas caudas poli-A, e permanecem próximos ao DNA que os produziu. Uma máquina proteica chamada complexo Integrator, conhecida por aparar e terminar certos RNAs não codificantes, foi especificamente enriquecida em unidades MSR intactas. Quando a atividade de corte do Integrator foi reduzida, os níveis de RNA derivados de MSR aumentaram substancialmente, mas a marca repressive chave nas histonas persistiu enquanto a ligação de HP1 mudou de forma sutil. Análises em todo o genoma mostraram que apenas as ~10–15% cópias mais intactas de MSR se comportam dessa maneira, destacando um subconjunto de repetições “competentes” conectadas a essa via de silenciamento acoplada à transcrição.
DNA desespiralizado como imitação de promotor
A equipe também explorou como o próprio DNA MSR favorece essa transcrição incomum. Arrays MSR em multicópia, mas não cópias únicas ou duplas, mostraram sinais claros de DNA localmente desenrolado e de híbridos RNA:DNA, características estruturais frequentemente observadas perto de promotores ativos e em sítios de pausa. Essas configurações foram reforçadas quando as topoisomerases foram inibidas, e coincidiram com maior transcrição de MSR e características mais fortes de heterocromatina. Os autores propõem que três ou mais unidades MSR em tandem criem uma topologia física do DNA que imita um promotor, convidando a polimerase e fatores de transcrição a engajarem-se na medida certa para gerar pequenos RNAs que, juntamente com proteínas específicas, reforçam uma arquitetura de cromatina compacta.
Por que isso importa para a saúde do genoma
Para um observador leigo, este trabalho revela que partes do nosso DNA “lixo” atuam como interruptores cuidadosamente ajustados, usando uma combinação de forma do DNA, transcrição de baixo nível e processamento de RNA para construir a camada protetora do genoma. Apenas unidades MSR que podem suportar essa transcrição controlada e não mensageira podem disparar nova heterocromatina, enquanto elementos embaralhados ou excessivamente ativos não conseguem. Essa lógica baseada em DNA/RNA ajuda a explicar como as células distinguem entre regiões a serem mantidas silenciosas e aquelas que podem abrigar genes, e por que RNAs satélite mal regulados estão associados ao câncer e a problemas de desenvolvimento. Em essência, o estudo demonstra que o “fundo” repetitivo do genoma não é um enchimento passivo, mas um engenheiro ativo da arquitetura e da estabilidade nuclear.
Citação: Lo, YH., Shukeir, N., Erikson, G. et al. Transcriptional competence defines the heterochromatin nucleating potential of isolated MSR units. Nat Commun 17, 2653 (2026). https://doi.org/10.1038/s41467-026-70991-2
Palavras-chave: heterocromatina, DNA satélite, RNA não codificante, estrutura da cromatina, estabilidade do genoma