Clear Sky Science · pt
Canais de prótons governam a química do carbonato vesicular em células mineralizantes de um calcificador marinho
Como pequenos construtores moldam nosso planeta
Grande parte dos penhascos de calcário e dos recifes de coral da Terra é produzida por construtores microscópicos que extraem ingredientes dissolvidos da água do mar e os transformam em rocha sólida. Este estudo investiga o interior de um desses construtores — o estágio larval de um ouriço-do-mar — para fazer uma pergunta surpreendentemente básica: como suas células controlam a acidez enquanto constroem um esqueleto de carbonato de cálcio? A resposta revela um truque elétrico elegante que pode também explicar por que organismos marinhos formadores de conchas são tão vulneráveis a um oceano mais ácido.
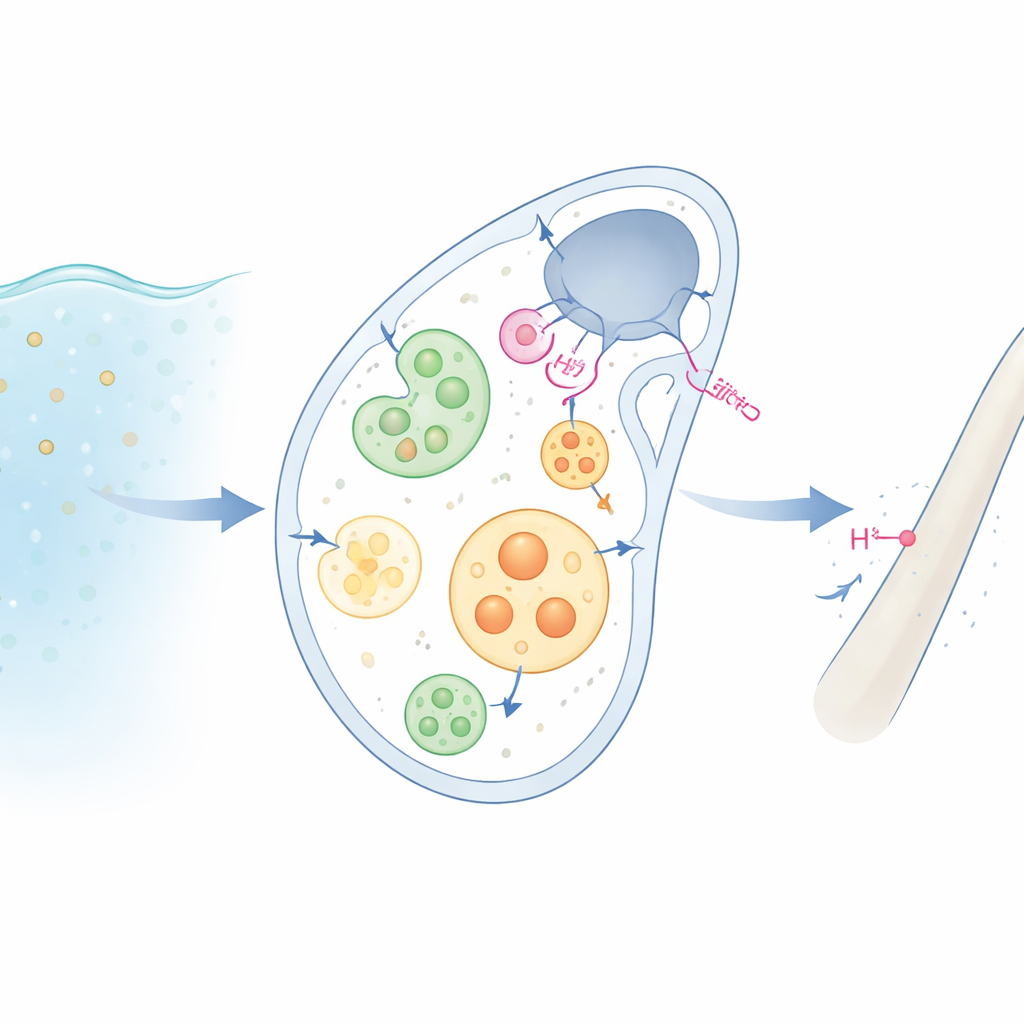
Da água do mar ao esqueleto
As larvas de ouriço-do-mar endurecem seus corpos com pequenos bastões de calcita feitos de carbonato de cálcio. Para isso, células especializadas “mineralizantes” primeiro aspiram água do mar, acondicionando-a em pequenas gotículas internas, ou vesículas. Dentro dessas vesículas, os ingredientes do mineral — cálcio, carbonato e outros íons — ficam concentrados em um precursor amorfo e vítreo que depois endurece em cristal. Mas toda vez que o carbonato de cálcio se forma, ácido extra (prótons) é gerado. Se esse ácido se acumulasse, ele dissolveria o próprio mineral que as células tentam produzir. Como as células evitam essa autodestruição tem sido um mistério de longa data.
Medindo a acidez dentro de gotículas em movimento
Os pesquisadores usaram imagens ao vivo e corantes fluorescentes sensíveis ao pH para observar a química dentro dessas vesículas em tempo real. Eles descobriram que quase metade das vesículas era fortemente alcalina — mais básica do que a água do mar normal — enquanto o restante era neutro ou ligeiramente ácido. Quando alteraram brevemente a acidez da água do mar circundante, tanto o interior das células quanto o das vesículas mudaram também, mostrando que os prótons podem mover-se relativamente livremente através dessas membranas. No entanto, as vesículas estavam parcialmente protegidas em comparação com o interior celular: responderam mais lentamente e de forma menos dramática, sugerindo uma “permeabilidade” controlada que ajuda a manter condições favoráveis à formação mineral.
Vazamentos elétricos que removem ácido
Para descobrir o que cria essa permeabilidade controlada, a equipe concentrou-se numa proteína canal de prótons chamada Otop2l, previamente ligada ao crescimento do esqueleto de ouriços-do-mar. Usando anticorpos, observaram que Otop2l está presente não apenas na membrana externa das células mineralizantes, mas também nas membranas de grandes vesículas internas. Quando reduziram os níveis de Otop2l com um bloqueador genético direcionado, tanto as células quanto suas vesículas tornaram-se menos responsivas às mudanças no pH externo, indicando que esse canal é uma rota principal para a saída de prótons. Registros elétricos em ovos de sapo e em células humanas geneticamente modificadas para produzir Otop2l mostraram que o canal se abre amplamente sob condições alcalinas e na presença de cálcio e magnésio — exatamente a situação nas vesículas calcificantes. Em essência, as células usam sua diferença natural de voltagem através da membrana, juntamente com Otop2l, para expulsar ácido sem gastar muita energia metabólica.
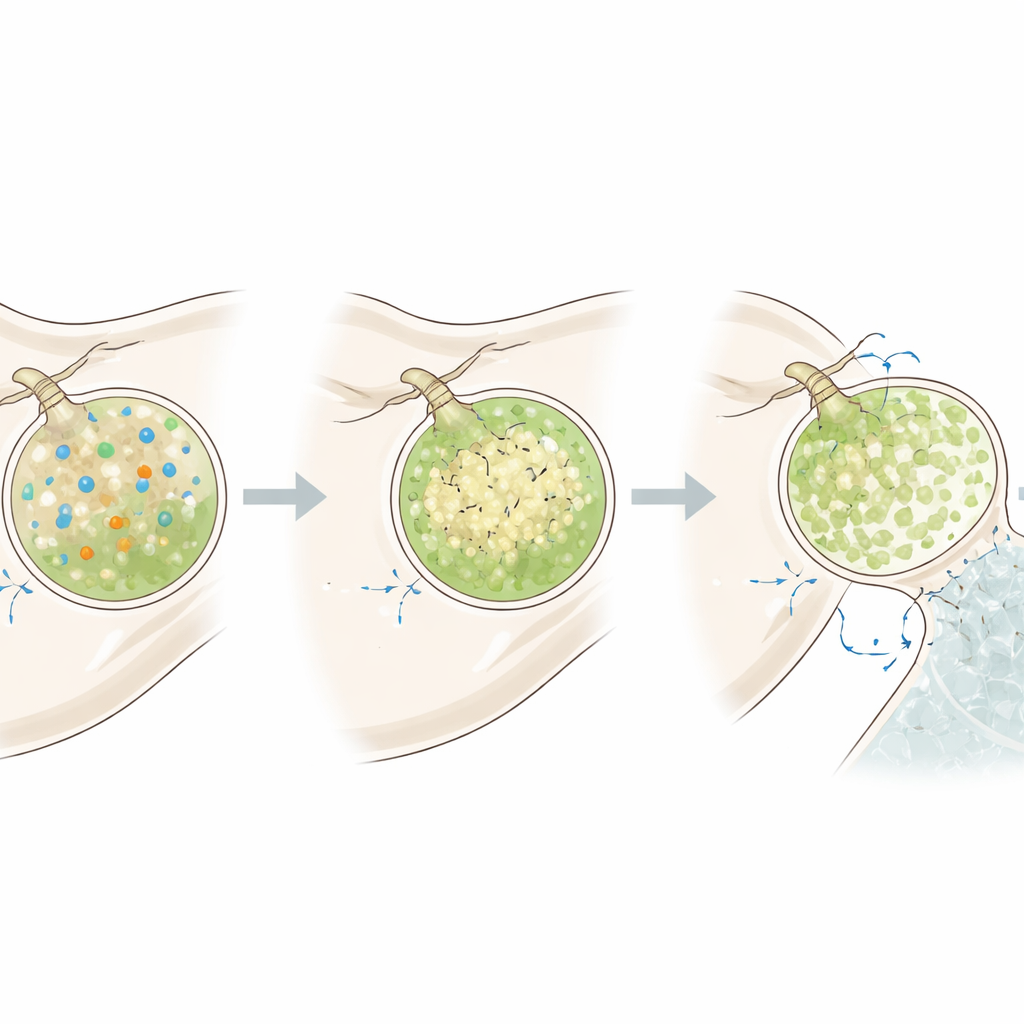
Vesículas se preparando para reparar
A equipe então investigou o que acontece quando as larvas precisam reconstruir o esqueleto após danos. Eles dissolveram os esqueletos larvais expondo-os brevemente a água do mar de baixo pH, depois os retornaram à água normal e seguiram as vesículas durante o recondicionamento. Durante essa fase de alta demanda, as células mineralizantes produziram mais vesículas no geral, com um forte aumento nas vesículas alcalinas e ricas em cálcio. Essas vesículas puderam recuperar seu pH elevado mais rapidamente após um pulso ácido, e o interior celular também tornou-se mais alcalino. Ainda assim, o potencial elétrico das células permaneceu semelhante, o que implica que elas se ajustam principalmente aumentando o suprimento de carbonato e a condutância de prótons, em vez de alterar profundamente seu estado elétrico.
Por que a acidificação dos oceanos importa
Juntos, os achados sustentam um modelo em que as células mineralizantes dos ouriços-do-mar operam um sistema “aberto”: elas continuamente endocitam água do mar, bombeiam carbono para as vesículas e dependem de canais de prótons e da voltagem da membrana para eliminar o excesso de ácido de volta ao oceano circundante. Esse arranjo é eficiente enquanto o pH externo permanecer dentro da faixa estreita e estável que caracterizou boa parte da história recente da Terra. Mas se a água do mar se tornar mais ácida — como está ocorrendo hoje com o aumento do dióxido de carbono — esse fluxo externo de prótons pode enfraquecer ou até reverter. O trabalho, portanto, oferece uma visão mecanicista do porquê muitos calcificadores marinhos têm dificuldades sob a acidificação dos oceanos: precisamente os canais que tornaram a biomineralização barata e robusta podem se tornar um passivo em um mar que muda rapidamente.
Citação: Jonusaite, S., Przibylla-Diop, C., Musinszki, M. et al. Proton channels govern vesicular carbonate chemistry in mineralizing cells of a marine calcifier. Nat Commun 17, 2578 (2026). https://doi.org/10.1038/s41467-026-70837-x
Palavras-chave: biomineralização, larvas de ouriço-do-mar, canais de prótons, acidificação dos oceanos, carbonato de cálcio