Clear Sky Science · pt
Receptores mecanossensoriais aptâmeros sintéticos permitem sensoriamento de forças específico por célula e controle temporal via circuitos de DNA
Ouvindo as Células por Meio de Puxões Suaves
Nossos corpos estão cheios de células que constantemente empurram e puxam seu entorno, usando forças diminutas para decidir quando crescer, mover-se ou mudar. Este estudo descreve uma nova maneira de escutar essas forças com dispositivos baseados em DNA que podem ser ajustados para tipos celulares específicos e ligados e desligados ao longo do tempo. Essa tecnologia poderia, um dia, ajudar engenheiros a orientar o crescimento de tecidos, entender como tumores se comportam ou projetar materiais inteligentes que reagem a células vivas em tempo real.
Usando DNA como um Pequeno Interruptor Mecânico
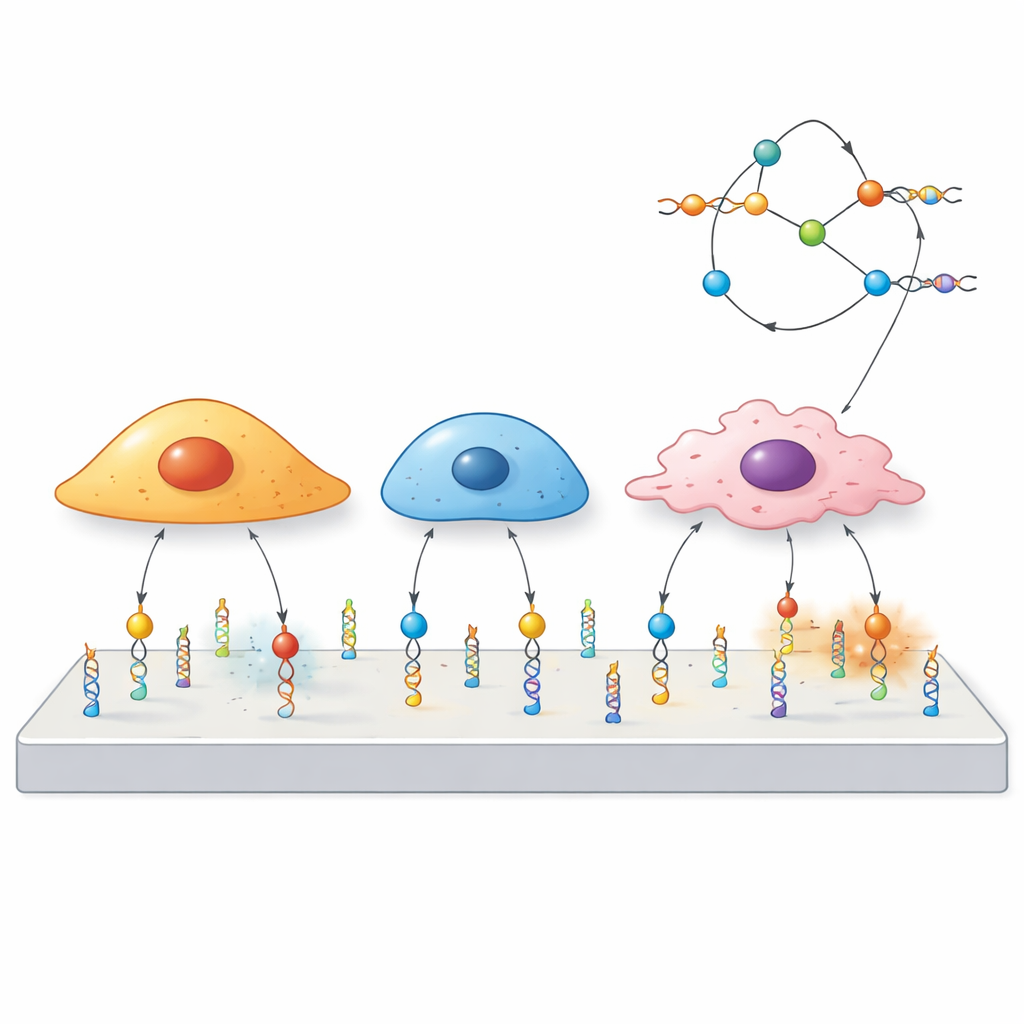
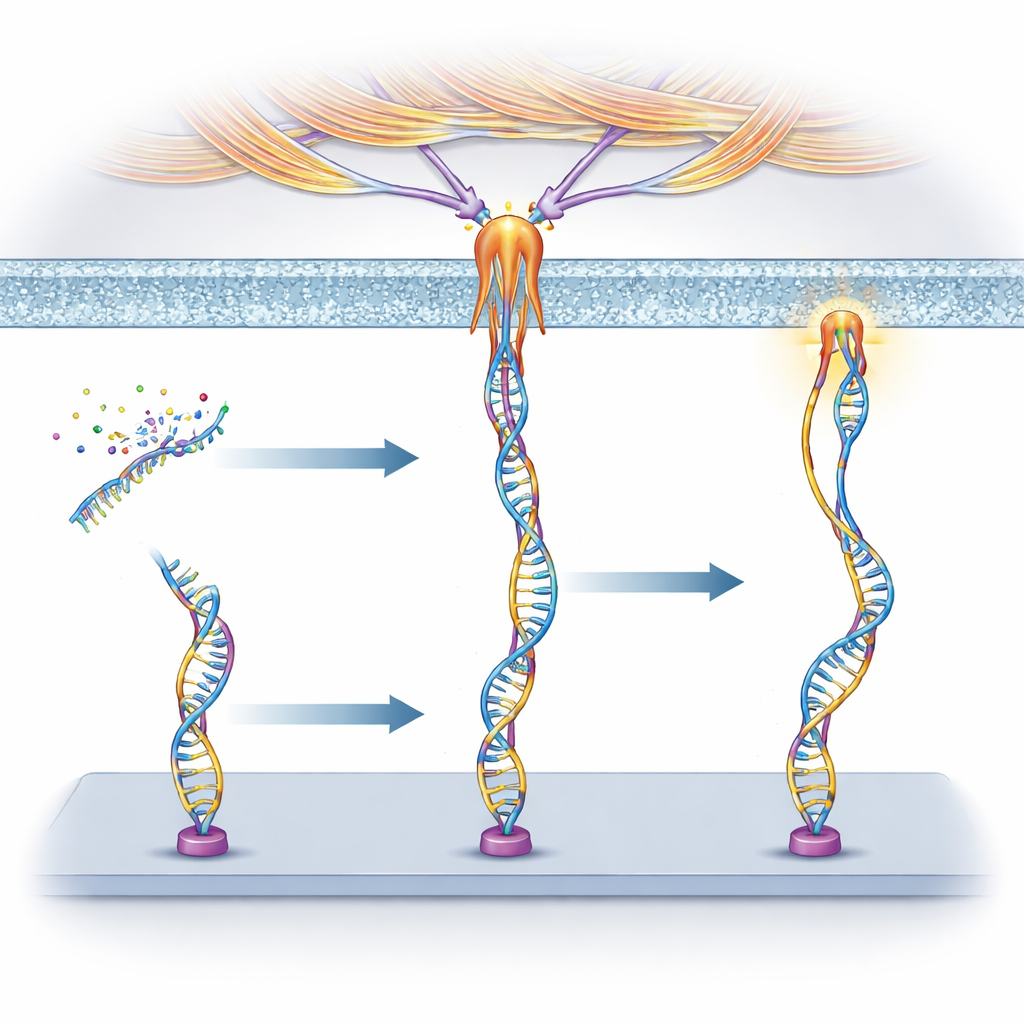
Os pesquisadores construíram “mecanoprobes” de DNA, a mesma molécula que carrega informação genética. Cada sonda tem três partes: uma sequência curta de DNA chamada aptâmero que se liga a uma proteína escolhida na superfície celular, um segmento pareado de DNA que atua como uma mola calibrada para romper sob uma certa força, e um corante fluorescente que acende quando essa mola se parte. Quando uma célula puxa o receptor ligado pelo aptâmero com força suficiente, o duplex de DNA abre e o sinal é ativado. Como aptâmeros diferentes se prendem a receptores distintos, a equipe pode decidir antecipadamente quais células ou proteínas serão capazes de disparar a sonda.
Encontrando Vias de Força Ocultas na Superfície Celular
A maioria dos sensores de força existentes foca em integrinas, proteínas conhecidas que ajudam as células a se agarrar ao entorno, mas que são encontradas em muitos tipos celulares, limitando a seletividade. Aqui, a equipe mirou em receptores “não canônicos” que normalmente não são vistos como mecânicos. Eles mostraram que um aptâmero chamado AS1411, que se liga à nucleolina — uma proteína comum em células cancerosas — só produziu sinal quando reconheceu especificamente seu alvo. Ao projetar sondas que exigiam forças mais fracas ou mais fortes para abrir, descobriram que a nucleolina transmite forças modestas em comparação com as integrinas e, por si só, não ajuda as células a se espalharem sobre uma superfície. Em contraste, outro aptâmero, Sgc8, que reconhece o receptor PTK7, pôde relatar forças mesmo quando as células mal aderiam, formando padrões em anel que sugeriam uma origem diferente do movimento.
Rastreando de Onde as Forças Vêm
Para entender o que puxava esses dispositivos de DNA, os pesquisadores usaram drogas que bloqueiam seletivamente diferentes processos celulares. Para a nucleolina, eles descobriram que suas forças dependiam fortemente da miosina, a mesma proteína motora que ajuda os músculos a contrair, e apareciam em locais onde a célula forma adesões focais — pontos de contato especiais usados para segurar e detectar rigidez. Isso sugere que a nucleolina está ligada indiretamente à maquinaria interna actina–miosina da célula e pode compartilhar suas forças contráteis. Para o PTK7, no entanto, bloquear um processo chamado macropinocitose — em que a célula revolta a membrana e engole fluido — reduziu muito os sinais. As forças surgiam principalmente do início do revolvimento da membrana impulsionado pelo crescimento de actina, não das etapas posteriores de selamento de vesículas, revelando uma via mecânica distinta.
Ajustando a Seletividade Celular com Precisão Molecular
Porque cada aptâmero reconhece um receptor de superfície particular, o mesmo arcabouço de DNA pode ser reprogramado simplesmente trocando um aptâmero por outro. A equipe demonstrou isso com sondas para três alvos diferentes — PTK7, mucina-1 e EpCAM — em um painel de linhas celulares cancerígenas com níveis altos ou baixos de cada proteína. Células ricas em um dado receptor produziram sinais fortes, enquanto aquelas com pouco receptor mal respondendo, mesmo quando misturadas no mesmo prato. Notavelmente, células que compartilhavam o mesmo receptor ainda podiam mostrar padrões espaciais diferentes de força, ressaltando que o fluxo de força através de um receptor depende não apenas de sua presença, mas também da fiação interna de cada tipo celular.
Programando Quando as Células Podem Puxar
Aproveitando o fato de que aptâmeros são feitos de DNA, os pesquisadores conectaram suas sondas a redes de reação de DNA que controlam se o aptâmero pode se ligar ou não. Fitilhas complementares “bloqueadoras” podem temporariamente esconder o aptâmero, e fitas “ativadoras” podem depois remover os bloqueadores por meio de uma reação de troca de fitas, restaurando a sensibilidade à força. Eles também projetaram um bloqueador à base de RNA que pode ser cortado por uma enzima chamada RNase H, e retardaram ainda mais esse corte com moléculas isca que competem pela enzima. Dessa forma, transformaram a mecanossensoriamento em um programa temporizado: as células só podiam gerar sinais após um atraso embutido ou dentro de janelas de tempo escolhidas.
Por Que Isso Importa para Materiais Vivos do Futuro
Em termos cotidianos, este trabalho transforma o DNA em uma trava mecânica inteligente que se abre apenas para certas células, apenas sob certas forças e apenas em momentos escolhidos. Ao revelar que receptores menos óbvios como nucleolina e PTK7 podem transportar informação mecânica por rotas muito diferentes dentro das células, amplia nossa visão de como as células “sentem” seu ambiente. Como todo o sistema é construído a partir de ácidos nucleicos, ele pode se integrar diretamente à caixa de ferramentas em rápido crescimento de circuitos de DNA e nanodispositivos. Isso cria uma base para materiais e tecidos projetados que não apenas detectam quando células empurram ou puxam, mas também respondem com ações bioquímicas cronometradas, potencialmente guiando cura, crescimento ou tratamento do câncer de maneira altamente programável.
Citação: Xu, T., Sethi, S., Drees, C. et al. Synthetic aptamer mechanoreceptors enable cell-specific force sensing and temporal control via DNA circuits. Nat Commun 17, 2492 (2026). https://doi.org/10.1038/s41467-026-70765-w
Palavras-chave: mecano-transdução, aptâmeros de DNA, mecânica celular, biologia sintética, redes de reação de DNA