Clear Sky Science · pt
Um atuador mioneural com biofísica projetada para sistemas biohíbridos implantáveis
Reconstruindo músculos como máquinas vivas inteligentes
Imagine se os médicos pudessem transformar o próprio músculo de uma pessoa em um motor vivo que não se cansa, pode ser controlado por um computador e pode conviver com órgãos delicados por anos. Este estudo descreve uma forma de fazer exatamente isso. Os pesquisadores desenvolvem um “atuador mioneural” em ratos — um músculo cuja fiação nervosa é deliberadamente rearranjada para que possa ser acionado por eletrônicos, resistir à fadiga e ainda se comportar como tecido natural. Esses atuadores vivos poderiam, um dia, restaurar movimentos, dar suporte a órgãos em falha ou transmitir sensações realistas de próteses avançadas.
Por que músculos vivos são motores melhores
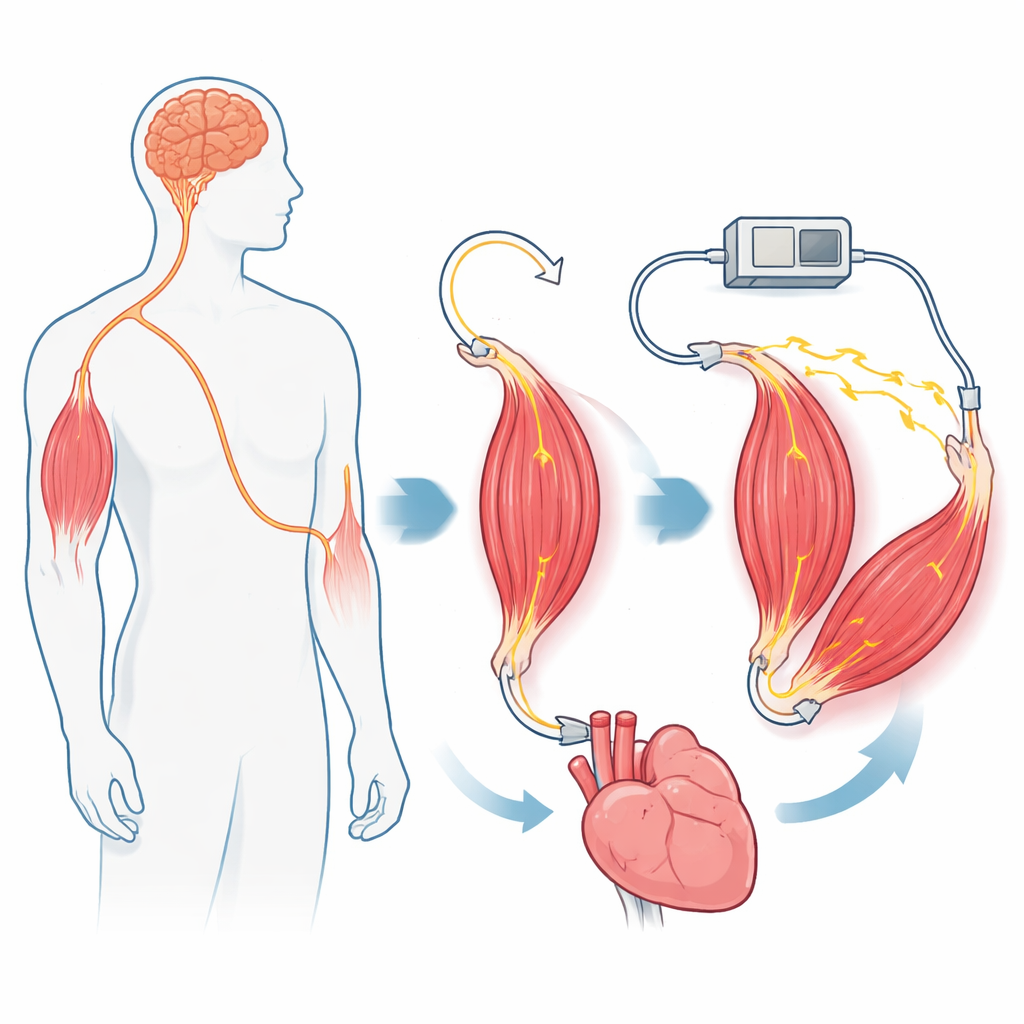
Motores artificiais que funcionam com eletricidade, ar ou fluidos são potentes, mas são pesados, difíceis de reduzir a tamanhos compatíveis com o corpo e feitos de materiais que não se integram bem ao tecido vivo. Em contraste, o músculo esquelético é leve, energeticamente eficiente, autorreparador e já projetado para trabalhar dentro do corpo. Ele pode crescer, se adaptar e responder a sinais nervosos minúsculos. No entanto, quando músculos são controlados diretamente por pulsos elétricos de um dispositivo implantado, eles se cansam rapidamente. Essa fadiga ocorre porque a estimulação elétrica padrão tende a recrutar primeiro as fibras maiores, mais rápidas, porém menos duráveis. Para aproveitar o músculo como um motor implantável e confiável, a equipe precisou mudar como suas fibras nervosas são organizadas e recrutadas — sem sacrificar a saúde e a sustentabilidade naturais do músculo.
Trocando vias nervosas para reescrever o controle
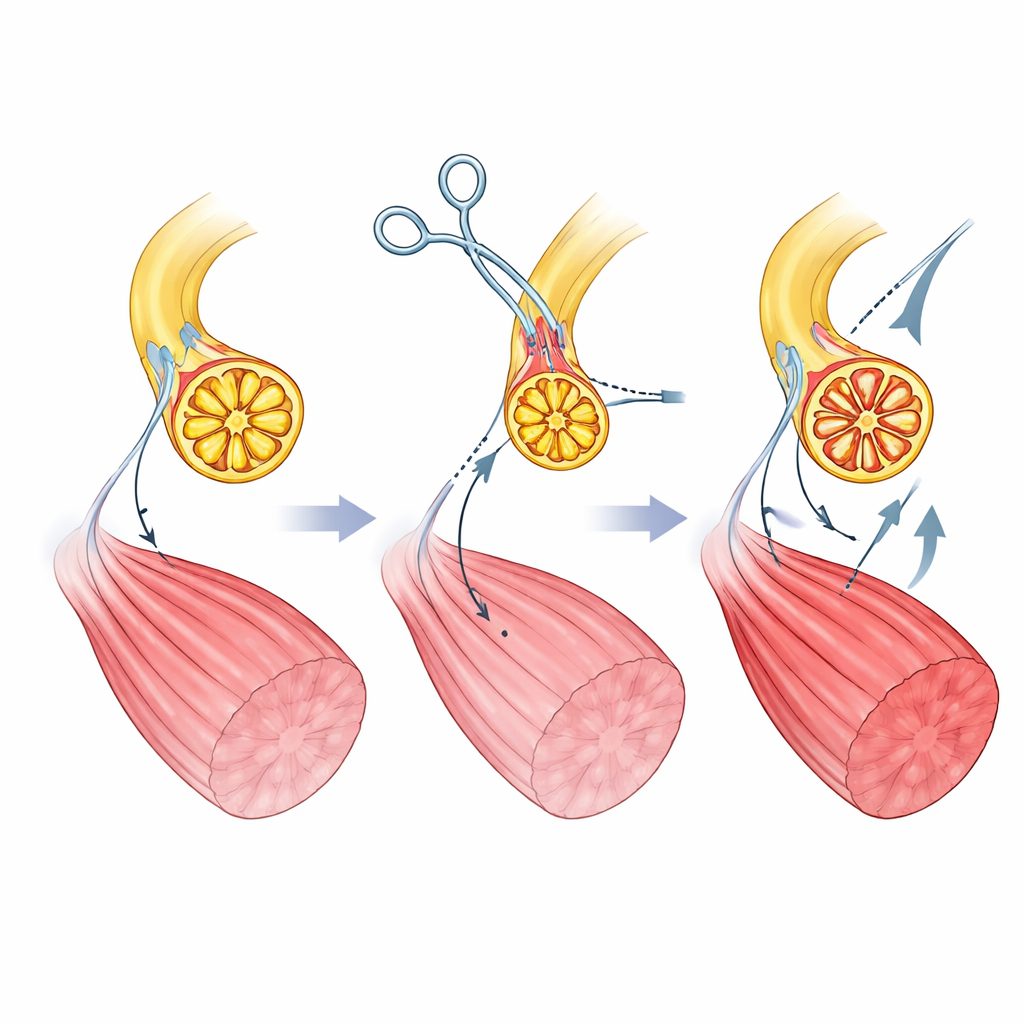
Os autores criam seu atuador mioneural em ratos ao reconectar cirurgicamente um músculo da perna. Primeiro, eles cortam o nervo motor normal que leva comandos da medula espinhal e impedem que ele regenere. Em seguida, encaminham um nervo diferente — um que normalmente conduz sinais de toque e alongamento da pele e dos tecidos — diretamente para o músculo. Com o tempo, esse nervo “sensitivo” regenera-se dentro do músculo e forma novos pontos de contato com as fibras musculares. A microscopia mostra que essas novas junções se parecem e funcionam como conexões motoras normais, e o músculo recupera a capacidade de contrair-se quando o nervo sensitivo é estimulado eletricamente. Importante, os axônios nesse nervo sensitivo são mais uniformes e menores em tamanho do que os do nervo motor original, preparando o terreno para um recrutamento de fibras musculares mais equilibrado sob controle computacional.
Músculos que continuam funcionando quando exigidos
Depois que os músculos reconectados cicatrizaram, a equipe os submeteu a rotinas de teste exigentes. Compararam músculos nativos com os novos atuadores durante contrações únicas repetidas e durante longos períodos de contração contínua. Os atuadores mioneurais perderam força muito mais lentamente e mostraram saída mais estável ao longo do tempo, com uma melhoria de 260% na resistência à fadiga sob trabalho contínuo. O comportamento deles ao longo de minutos foi fundamentalmente diferente do músculo não modificado: em vez de uma queda rápida na força, o declínio foi mais gradual e depois estabilizou. Apesar de terem perdido alguma massa durante o processo de reconexão, os atuadores preservaram uma estrutura saudável das fibras e produziram força por unidade de massa semelhante ao músculo nativo, mantendo sua condição por pelo menos 15 semanas, mesmo sem exercício ou estimulação adicional.
Controle por computador sem perturbar o cérebro
Como a nova fiação nervosa desconecta o músculo dos sinais motores normais do cérebro, todas as contrações passam a ser geradas por um estimulador externo. Os pesquisadores inserem o músculo em um laço de realimentação: um sensor mede a força, um controlador ajusta a estimulação do nervo e o sistema acompanha uma força-alvo escolhida ao longo de muitos ciclos. Músculos nativos falham rapidamente nesse arranjo, mas os atuadores mioneurais continuam seguindo os sinais de comando. Para tornar o sistema mais seguro e flexível, a equipe também introduz um “bloqueio nervoso” reversível. Aplicando um sinal elétrico de alta frequência no nervo mais próximo da medula espinhal, eles impedem que pulsos de estimulação enviem sinais indesejados de volta ao sistema nervoso central, permitindo ainda que o lado muscular responda. Nos testes, o atuador continuou a gerar forças controladas enquanto o cérebro permanecia efetivamente isolado da estimulação artificial.
De membros biônicos a suporte para órgãos falhando
Para mostrar como esse motor vivo poderia ser usado, os autores constroem dois sistemas demonstrativos em ratos. No primeiro, eles acoplam o atuador em série com outro músculo que representa o músculo residual em um ponto de amputação. Ao apertar ou relaxar esse par, mudam o alongamento do músculo residual e, por sua vez, a atividade de suas fibras nervosas sensoriais — essencialmente aumentando ou diminuindo a sensação de posição e força do membro. Essa “interface mecanoneural proprioceptiva” poderia, eventualmente, fornecer feedback com sensação natural de membros robóticos ou avatares virtuais. No segundo sistema, eles envolvem o atuador ao redor de um segmento de intestino delgado preenchido com fluido. Quando acionado por estimulação nervosa, o músculo comprime e libera o segmento intestinal, e o rastreamento de movimento mostra que o órgão se move em sincronia com o atuador. Isso sugere dispositivos futuros que poderiam emprestar força mecânica a órgãos enfraquecidos, como intestino, bexiga ou até mesmo o coração.
O que isso pode significar para a medicina futura
No geral, este trabalho demonstra que, ao redirecionar nervos com cuidado, o próprio músculo de uma pessoa pode ser transformado em um atuador resistente à fadiga, controlado por computador, que ainda se comporta como tecido nativo e pode ser eletricamente isolado do cérebro quando necessário. Como a abordagem depende de técnicas cirúrgicas e eletrodos que já se assemelham a ferramentas clínicas existentes, pode ser mais fácil de traduzir do que implantes totalmente sintéticos ou tecidos cultivados em laboratório. Se atuadores mioneurais semelhantes puderem ser construídos e controlados com segurança em humanos, eles poderão formar o núcleo de novos sistemas biohíbridos que restauram a sensação de membros, auxiliam órgãos em falha e fornecem sinais mecânicos precisos ao corpo sem o volume e a rigidez das máquinas tradicionais.
Citação: Song, H., Herrera-Arcos, G., Friedman, G.N. et al. A myoneural actuator with engineered biophysics for implantable biohybrid systems. Nat Commun 17, 2584 (2026). https://doi.org/10.1038/s41467-026-70626-6
Palavras-chave: atuador biohíbrido, neuropróteses, fadiga muscular, regeneração nervosa, suporte a órgãos