Clear Sky Science · pt
Uma base metrológica para transcriptômica absoluta usando calibradores ancorados ao Sistema Internacional de Unidades
Por que transformar sinais de RNA em números reais importa
Testes gênicos modernos conseguem ler quais genes estão ativados ou desativados em nossas células, mas tropeçam numa questão básica: quantas moléculas estão realmente presentes? As tecnologias atuais de sequenciamento de RNA comparam, em sua maioria, mudanças relativas entre amostras em vez de fornecer contagens absolutas e confiáveis. Isso é um problema se você quer definir limiares universais para doenças, comparar resultados entre hospitais ou construir modelos precisos do funcionamento celular. Este estudo apresenta uma nova maneira de ancorar o sequenciamento de RNA às mesmas unidades internacionais usadas em química e física, transformando sinais relativos imprecisos em números absolutos e comparáveis.
O problema de comparar a atividade gênica
O sequenciamento de RNA funciona fragmentando moléculas de RNA e contando quantas vezes cada gene é representado. Mas dois tipos de distorção surgem. Primeiro, diferenças sistêmicas entre experimentos — como diferentes laboratórios, máquinas ou métodos de preparação de amostras — criam “efeitos de lote” que fazem a mesma amostra parecer diferente quando processada em momentos distintos. Segundo, efeitos dependentes da sequência — em que genes com certos comprimentos ou composições de bases são mais ou menos propensos a ser capturados — significam que, mesmo dentro de uma única amostra, alguns genes são consistentemente supercontados e outros subcontados. Como resultado, os cientistas são em grande parte forçados a falar sobre mudanças relativas entre condições em vez de contagens verdadeiras de moléculas, e essas mudanças relativas podem ser enganosas de um lote para outro.
Um novo conjunto de referências para medições de RNA
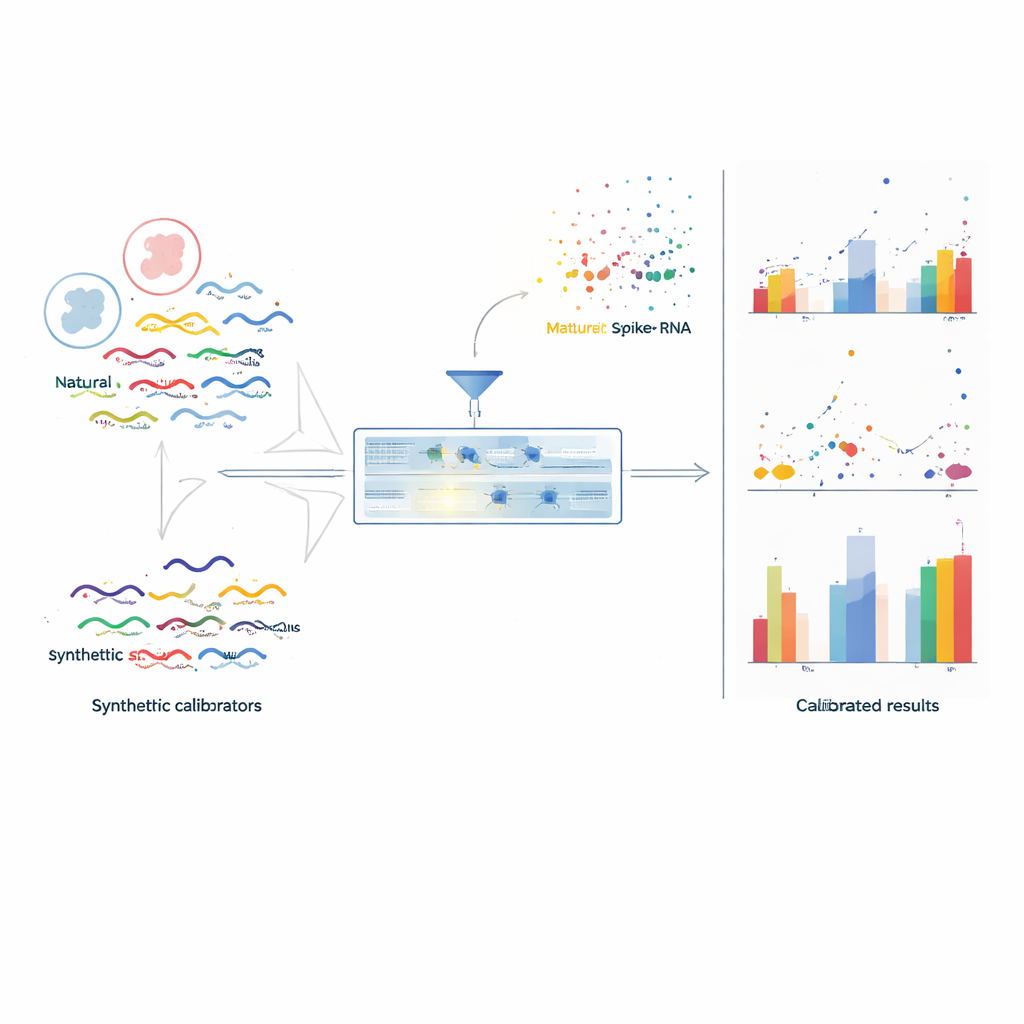
Para resolver isso, os autores criaram o TranScale, um painel de 100 moléculas sintéticas de RNA projetadas para se comportar como transcritos humanos reais, mas permanecendo computacionalmente distintas. Esses padrões abrangem uma ampla gama de comprimentos, características de sequência e variantes clinicamente relevantes, como formas de splicing e fusões gênicas, refletindo de perto a diversidade do RNA celular real. Crucialmente, cada molécula TranScale recebe uma concentração exata usando uma técnica de medição primária chamada espectrometria de massa com diluição isotópica, que é rastreável ao Sistema Internacional de Unidades (SI). Ao misturar uma quantidade conhecida e muito pequena de TranScale em cada amostra de RNA antes do sequenciamento, o experimento ganha uma régua interna que sofre os mesmos passos laboratoriais e distorções que os RNAs naturais.
Transformando leituras ruidosas em contagens absolutas
Com o TranScale presente em cada biblioteca, a equipe pode comparar o número de leituras de sequenciamento para cada molécula spike-in com sua concentração certificada. Para cada lote, eles selecionam spike-ins bem comportados e ajustam uma curva de calibração linear ligando as unidades baseadas em leitura às contagens verdadeiras de moléculas. Esse modelo simples captura simultaneamente tanto os vieses de lote quanto os relacionados à sequência. A mesma curva é então aplicada a todos os genes da amostra, convertendo suas leituras relativas em números absolutos de cópias por unidade de RNA. Em um amplo estudo multi-laboratorial e multi-plataforma, projetado deliberadamente para produzir fortes efeitos de lote, essa calibração reduziu a variação mediana das medições absolutas entre centros de acima de 85% para abaixo de 15–25%, e restaurou o agrupamento correto de amostras biológicas que havia sido obscurecido pelo ruído técnico.
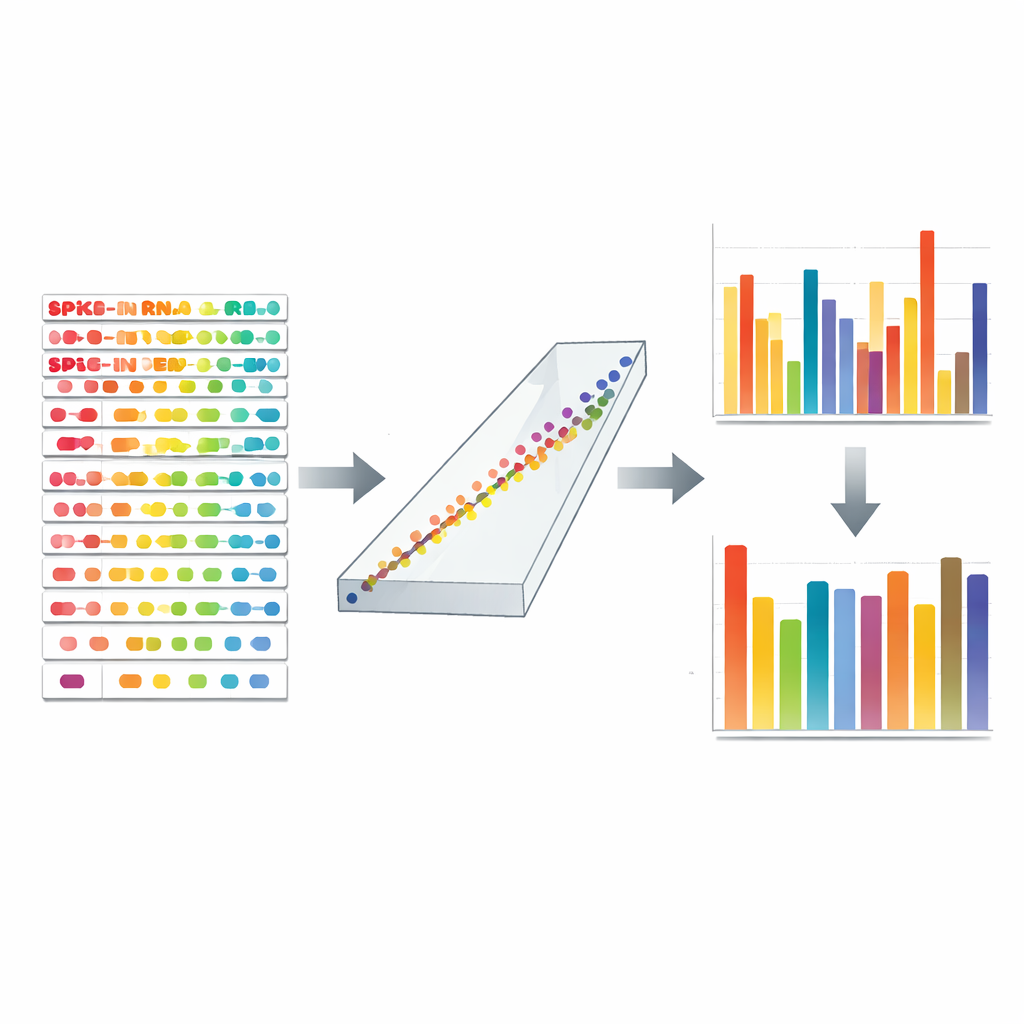
Detectando erros ocultos e corrigindo-os
Os padrões TranScale também atuam como sondas diagnósticas da qualidade dos dados. Ao comparar os valores medidos com suas verdades certificadas, os autores separaram dois tipos de erro: o quão errada está cada medição absoluta de um gene e o quão erradas estão as proporções entre condições. Encontraram exemplos surpreendentes em que diferenças relativas pareciam consistentes, mas os números absolutos estavam fortemente distorcidos, e vice-versa. Isso significa que verificações convencionais que focam apenas em mudanças relativas podem perder problemas sérios. Após a calibração, tanto os níveis absolutos quanto as proporções de spike-ins e de milhares de genes humanos reais bateram próximo às medições independentes por PCR digital e a um conjunto de referência externo. Os dados corrigidos revelaram um panorama quantitativo muito mais claro, permitindo comparar genes de manutenção a genes impulsionadores do câncer na mesma escala absoluta e ligar alterações no DNA, como genes co-amplificados em câncer, diretamente às suas saídas de RNA.
De tendências relativas a limiares clínicos
Finalmente, os pesquisadores mostraram como a escalação absoluta pode afiar decisões médicas. Usando um oncogene frequentemente medido em câncer de mama, eles definiram um ponto de corte fixo baseado em PCR digital e perguntaram se o sequenciamento de RNA poderia classificar amostras como normais ou tumorais de forma confiável através de muitos lotes. Dados não corrigidos deram respostas inconsistentes por causa de efeitos de lote. Após a calibração com TranScale, todas as bibliotecas concordaram com a classificação verdadeira. Ao vincular o sequenciamento de RNA às unidades SI por meio de padrões biomiméticos, este trabalho estabelece uma base metrológica para a transcriptômica. Abre a porta para pontos de corte diagnósticos universais, compartilhamento robusto de dados entre centros e modelos de nível de sistema mais precisos de como os genes são expressos em saúde e doença.
Citação: Zhang, Y., Yang, B., Yu, Y. et al. A metrological foundation for absolute transcriptomics using International System of Units-anchored calibrators. Nat Commun 17, 2747 (2026). https://doi.org/10.1038/s41467-026-70582-1
Palavras-chave: Sequenciamento de RNA, quantificação absoluta, metrologia, calibração de expressão gênica, padrões biomoleculares