Clear Sky Science · pt
StrucGAP: uma plataforma modular, enxuta e rastreável de mineração de dados para glicoproteômica estrutural e site‑específica
Decifrando os Revestimentos Açucarados das Proteínas
Cada célula do nosso corpo está coberta por uma espécie de floresta de estruturas açucaradas ligadas a proteínas. Essas “camadas de açúcar”, conhecidas como glicanos, ajudam silenciosamente a controlar como as células se aderem, comunicam e respondem ao ambiente. Instrumentos modernos conseguem catalogar esses padrões de açúcar com detalhes impressionantes, mas os pesquisadores frequentemente se afogam no volume e na complexidade dos dados. Este estudo apresenta o StrucGAP, uma nova plataforma computacional projetada para transformar essas medições densas em histórias claras e biologicamente significativas, usando o envelhecimento do útero de camundongos como caso de teste.
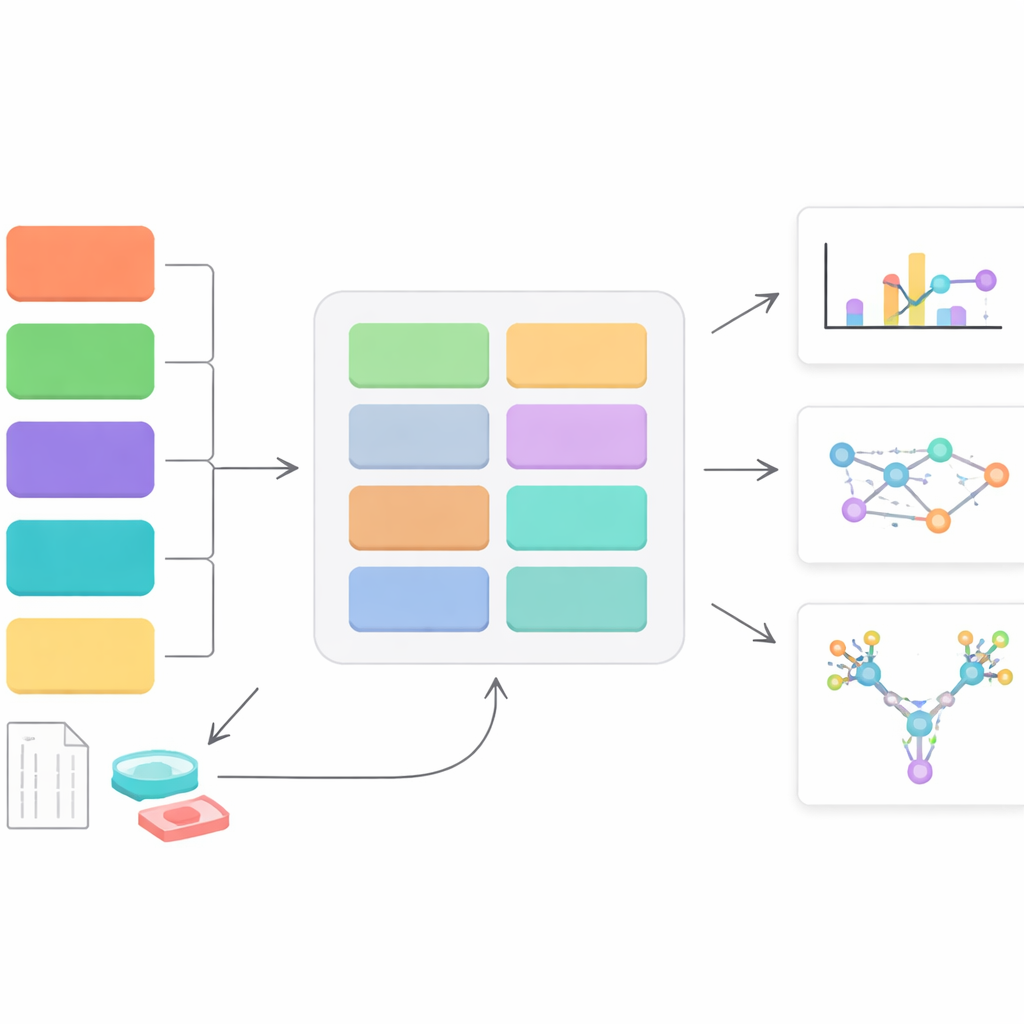
Um Novo Centro de Controle para Dados de Camadas Açucaradas
StrucGAP é uma plataforma de software construída para analisar um tipo específico de decoração açucarada: os glicanos N‑ligados, que se prendem a locais particulares nas proteínas. Em vez de tentar ser uma ferramenta de uso geral, o StrucGAP foi concebido desde o início para esse problema. Ele aceita resultados de vários “motores de busca” de espectrometria de massas populares que identificam quais glicanos estão em quais sítios proteicos. Uma vez feitas essas identificações, o StrucGAP as processa por meio de uma série de módulos que verificam a qualidade dos dados, resumem padrões gerais de glicanos, rastreiam como sítios específicos mudam entre condições e vinculam essas mudanças a funções biológicas e vias conhecidas.
Dividindo Glicanos Complexos em Partes Significativas
A maioria das ferramentas existentes trata cada glicano como um objeto único e indivisível. O StrucGAP adota uma abordagem diferente: divide cada glicano em blocos de construção menores e biologicamente significativos, como núcleos comuns, padrões de ramificação e motivos conhecidos que incluem fucose ou ácido siálico. Em seguida, pergunta não apenas quais glicanos inteiros aumentam ou diminuem, mas quais motivos aparecem com mais frequência, com menos frequência ou em novas combinações. Essa visão por “subestruturas” torna a análise mais robusta a atribuições incertas e ajuda a descobrir padrões que poderiam ficar escondidos, especialmente quando motivos raros, mas importantes, tornam‑se enriquecidos em uma condição específica.
Acompanhando Mudanças Açucaradas Durante o Envelhecimento Uterino
Para demonstrar o que o StrucGAP pode fazer, os autores o aplicaram a um conjunto de dados detalhado do tecido uterino de camundongas jovens e de meia‑idade. O experimento bruto identificou mais de vinte mil glicopeptídeos únicos, cada um representando um sítio proteico específico com um glicano particular. O StrucGAP primeiro limpou e padronizou os dados, depois mapeou como os glicanos estavam distribuídos pelos sítios proteicos e quantas variações estruturais apareciam em cada posição. O útero revelou‑se rico tanto em glicanos simples do tipo high‑mannose quanto em tipos complexos mais elaborados, com muitas composições de glicanos existindo como vários isômeros estruturais. Ao reduzir o foco para subestruturas, a plataforma catalogou com que frequência diferentes núcleos, contagens de ramificações e motivos — como epítopos Lewis ou formas específicas de ácido siálico — ocorriam e co‑ocorriam.
De Padrões à Função: Aderência e Remodelamento
O módulo quantitativo do StrucGAP então comparou úteros jovens e envelhecidos, encontrando mais de mil glicopeptídeos que aumentaram e algumas centenas que diminuíram com a idade. Um tema recorrente foi a “fucosilação do núcleo” — uma forma específica de ligação de uma unidade de fucose ao núcleo do glicano — que mostrou alterações em ambos os sentidos, sugerindo uma regulação finamente ajustada em vez de um interruptor simples ligado/desligado. Outros padrões emergiram à medida que os limiares estatísticos foram ajustados: glicanos com mais ramificações, motivos do tipo Lewis específicos e ácidos siálicos contendo Neu5Ac tornaram‑se progressivamente enriquecidos. Ao vincular essas características estruturais a bancos de dados de funções gênicas e vias, o StrucGAP revelou que os glicanos em mudança estavam concentrados em proteínas envolvidas na adesão celular, nas interações com a matriz circundante e no remodelamento da arquitetura tecidual. A plataforma também conectou esses padrões a mudanças nas enzimas que montam e apararam glicanos, bem como a proteínas ligadoras de glicanos, esboçando redes coordenadas que podem impulsionar o envelhecimento uterino.
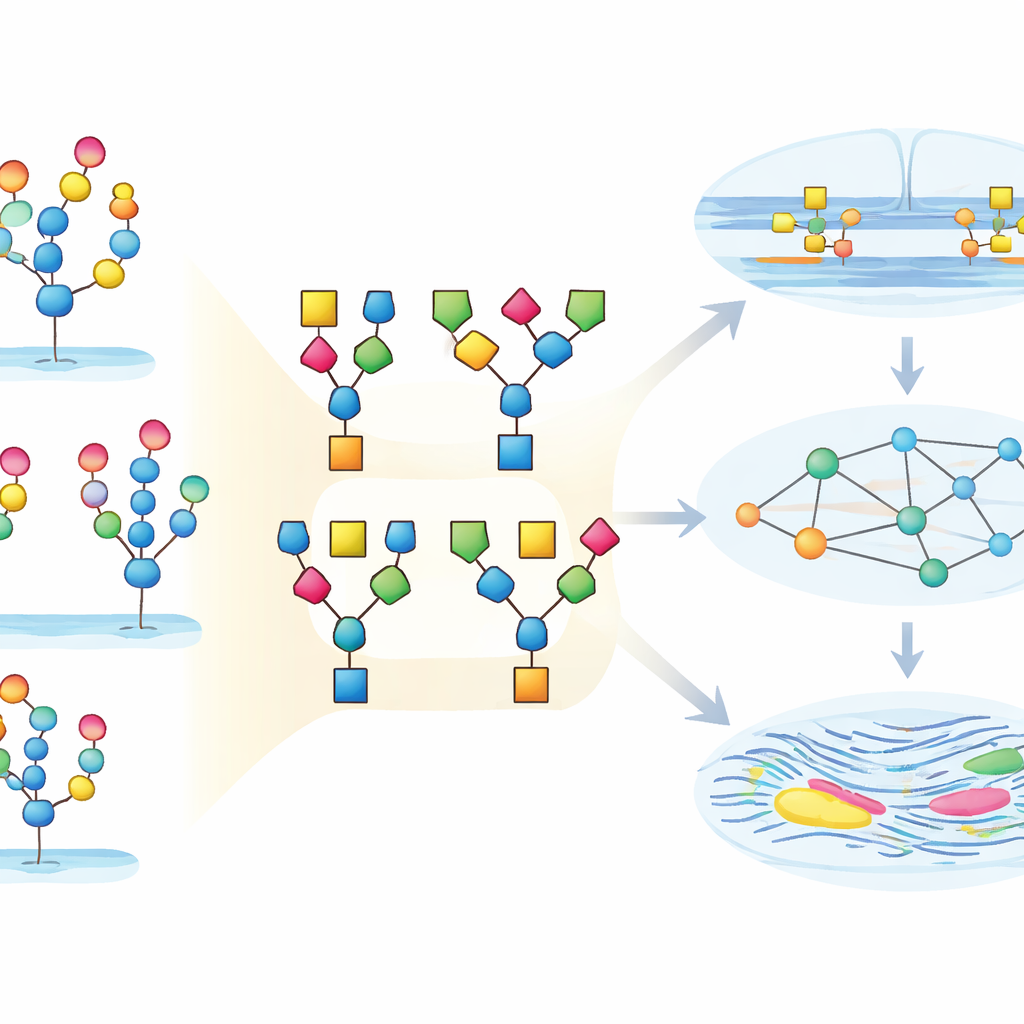
Transformando a Enxurrada de Dados em Intuição Biológica
Em termos práticos, este trabalho mostra como uma massa altamente técnica de medições de “açúcar‑em‑proteína” pode ser transformada em um mapa legível de como os tecidos mudam ao longo do tempo. O StrucGAP atua tanto como guardião da qualidade quanto como um motor de narrativa: limpa os dados, resume motivos açucarados-chave, associa‑os às enzimas que os moldam e às vias que influenciam, e gera automaticamente gráficos e relatórios que destacam as descobertas mais importantes. No útero de camundongo, isso revela uma mudança coordenada em direção a glicanos mais fortemente decorados, ricos em Neu5Ac e fucose, ligados à adesão e ao remodelamento tecidual. De forma mais ampla, o StrucGAP oferece aos pesquisadores um caminho prático para passar de dados brutos de glicoproteômica a ideias testáveis sobre como as camadas de açúcar ajudam a controlar saúde, doença e envelhecimento.
Citação: Yang, M., Wu, Y., Zhang, Z. et al. StrucGAP: a modular, streamlined and traceable data mining platform for structural and site-specific glycoproteomics. Nat Commun 17, 2579 (2026). https://doi.org/10.1038/s41467-026-70560-7
Palavras-chave: glicoproteômica, N‑glicosilação, plataforma de bioinformática, envelhecimento uterino, glicosilação de proteínas