Clear Sky Science · pt
Transições estruturais na montagem passo a passo das partículas centrais do proteassoma
Como as Células Eliminam o Lixo Molecular
Dentro de cada uma de nossas células, proteínas gastas e danificadas precisam ser degradadas antes que se acumulem como lixo. Uma máquina molecular gigante chamada proteassoma realiza grande parte dessa limpeza e já é alvo de medicamentos anticâncer. Este estudo revela os bastidores de como o núcleo catalítico do proteassoma é montado passo a passo em leveduras, expondo atalhos inesperados e mecanismos de segurança que ajudam a garantir que a máquina final funcione com precisão e apenas quando estiver pronta.
Construindo um Barril Triturador de Proteínas
A parte ativa do proteassoma é um núcleo em forma de barril composto por anéis empilhados de subunidades proteicas. Esse barril abriga os locais de corte ocultos que fragmentam outras proteínas em pedaços menores. Porque ativar esses cortadores cedo demais seria perigoso, as células montam o barril através de uma série de intermediários parcialmente formados. Os autores concentraram-se em versões iniciais do núcleo, conhecidas como complexos precursores, que normalmente são raras e efêmeras. Ao desacelerar levemente uma das etapas finais da montagem, conseguiram capturar e purificar essas formas iniciais de levedura e imaginá‑las com crio‑microscopia eletrônica de alta resolução, que congela moléculas em ação e revela suas formas tridimensionais.
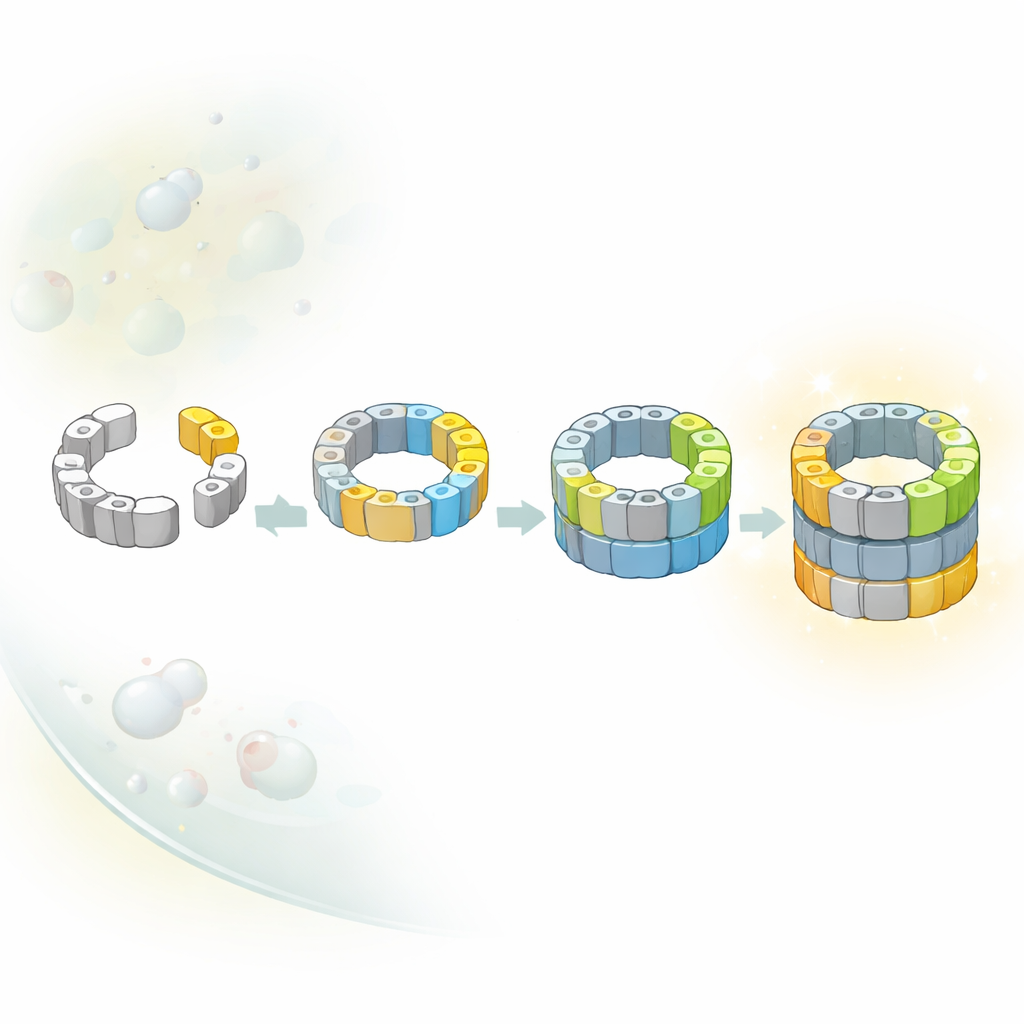
Vários Caminhos para o Mesmo Núcleo
Diagramas clássicos de livros didáticos muitas vezes sugerem que máquinas complexas dentro das células são montadas por uma rota única e fixa. Aqui, os pesquisadores descobriram que esse não é o caso para o núcleo do proteassoma. Identificaram diversos intermediários distintos que diferem em quais subunidades catalíticas já se integraram ao meio‑barril incompleto. Combinando instantâneos estruturais com truques genéticos que ativam ou desativam subunidades individuais, mostraram que pelo menos dois caminhos alternativos levam de um meio‑barril inicial a um quase completo. Em um caminho, uma subunidade particular chamada β5 chega primeiro; em outro, uma subunidade diferente, β1, pode se juntar mais cedo. O equilíbrio entre essas rotas provavelmente depende de quais blocos de construção estão mais disponíveis no ambiente congestionado da célula.
De Peças Soltas a uma Câmara de Corte Travada
As estruturas também revelam como os sítios de corte do proteassoma são cuidadosamente preparados à medida que a montagem avança. Em intermediários iniciais, regiões de loop ao redor dos resíduos de corte enterrados são flexíveis e pouco ordenadas, e os centros catalíticos ainda estão bloqueados por curtos segmentos “pró‑peptídicos”. À medida que subunidades adicionais se encaixam ao redor do anel, esses loops gradualmente assumem formas mais definidas que alinham aminoácidos cruciais necessários para a autoativação. Só quando dois meio‑barris finalmente se unem, completando o barril de anéis duplos, esses loops travam completamente em sua configuração ativa e desencadeiam a remoção dos segmentos bloqueadores. Esse acoplamento de geometria e química ajuda a garantir que a poderosa atividade de corte só apareça dentro de uma câmara selada, protegendo o restante da célula.
Chaperonas Ajudantes Guiam e Depois Se Libertam
No decorrer do processo, proteínas auxiliares especializadas chamadas chaperonas escoltam o barril em montagem e evitam combinações incorretas. Uma chaperona, Ump1, começa amplamente desestruturada, mas se dobra progressivamente à medida que mais subunidades a envolvem, acabando presa na cavidade central e depois degradada quando o barril fica ativo. Outro par de chaperonas, Pba1–Pba2, prende a superfície do anel externo de duas maneiras engenhosas. Um loop flexível de Pba1 se insere entre duas subunidades do anel externo como um espaçador, mantendo‑as ligeiramente separadas e evitando o fechamento prematuro. Ao mesmo tempo, a extremidade terminal de uma subunidade do anel externo (α1) ajuda a posicionar segmentos vizinhos de modo que, na etapa final, as chaperonas possam ser liberadas e o anel possa se fechar corretamente. Quando os pesquisadores deletaram a cauda de α1, o barril emperrou em um estado tardio, quase completo, que teimosamente reteve suas chaperonas, confirmando que essa pequena região atua como parte de um interruptor de liberação.
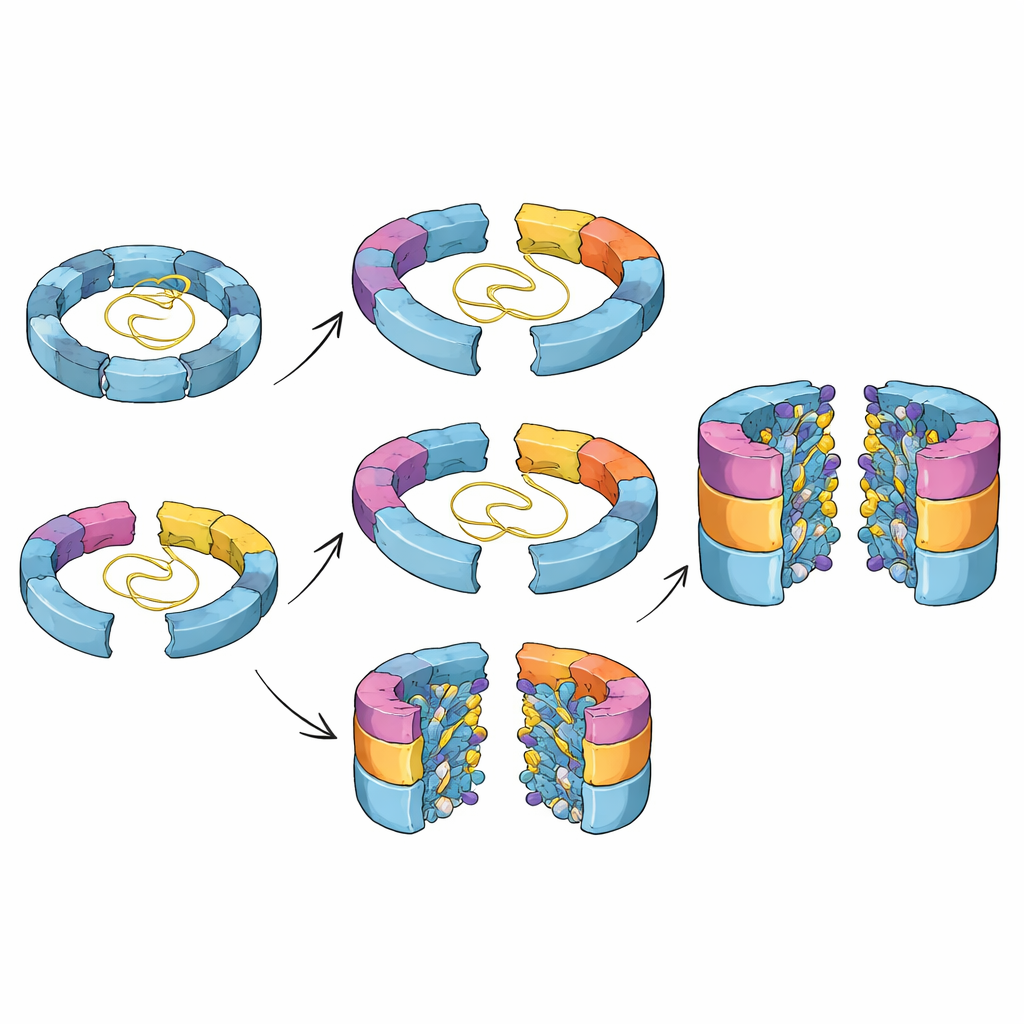
Por Que Essas Etapas Ocultas Importam
Juntas, essas descobertas desenham um retrato detalhado de como as células coreografam a montagem de um triturador de proteínas perigoso, porém essencial. O trabalho mostra que o núcleo do proteassoma pode ser construído por mais de uma rota, que seus sítios ativos são esculpidos gradualmente no lugar, e que proteínas auxiliares não apenas estabilizam intermediários iniciais, mas também estão integradas a um circuito de temporização que garante sua saída no momento certo. Entender essas etapas ocultas ajuda a explicar como pequenas mudanças genéticas em fatores de montagem podem contribuir para doenças e pode auxiliar o desenho de fármacos que ajustem a atividade do proteassoma no câncer, em desordens imunológicas ou na neurodegeneração ao mirar sua construção em vez de sua forma final.
Citação: Mark, E., Ramos, P.C., Nunes, M.M. et al. Structural transitions in the stepwise assembly of proteasome core particles. Nat Commun 17, 2582 (2026). https://doi.org/10.1038/s41467-026-70525-w
Palavras-chave: montagem do proteassoma, degradação de proteínas, chaperonas moleculares, crio-microscopia eletrônica, controle de qualidade celular