Clear Sky Science · pt
Quimerismo molecular transitório para explorar organelas xenogênicas
“Painéis solares” emprestados em uma única célula
Costumamos pensar na vida movida pela energia solar em termos de plantas e algas, mas alguns predadores unicelulares seguem um atalho: roubam os “painéis solares” — os cloroplastos — de suas presas. Este estudo explora como um desses microrganismos, Rapaza viridis, mantém essas peças roubadas funcionando por semanas, mesmo sendo de uma espécie totalmente diferente. Ao revelar como proteínas do próprio hospedeiro penetram e sustentam esses cloroplastos estrangeiros, o trabalho lança luz sobre como componentes celulares complexos, como cloroplastos, podem ter evoluído originalmente.
Como um microbe rouba e usa energia verde
Rapaza viridis é um minúsculo flagelado que se alimenta de uma alga verde específica chamada Tetraselmis. Em vez de digerir tudo, Rapaza conserva os cloroplastos capturados, agora chamados “kleptoplastos”, e descarta o resto da célula da alga, incluindo seu núcleo. Esses kleptoplastos são cortados em pedaços e transmitidos às células-filhas de Rapaza. Por cerca de duas semanas, o hospedeiro pode viver quase inteiramente da energia e do carbono produzidos por esses cloroplastos emprestados, mesmo sem receber instruções ou peças de reposição do genoma algal original. Esse estilo de vida incomum oferece uma janela ao vivo sobre os passos iniciais que podem ter levado à formação de cloroplastos permanentes.
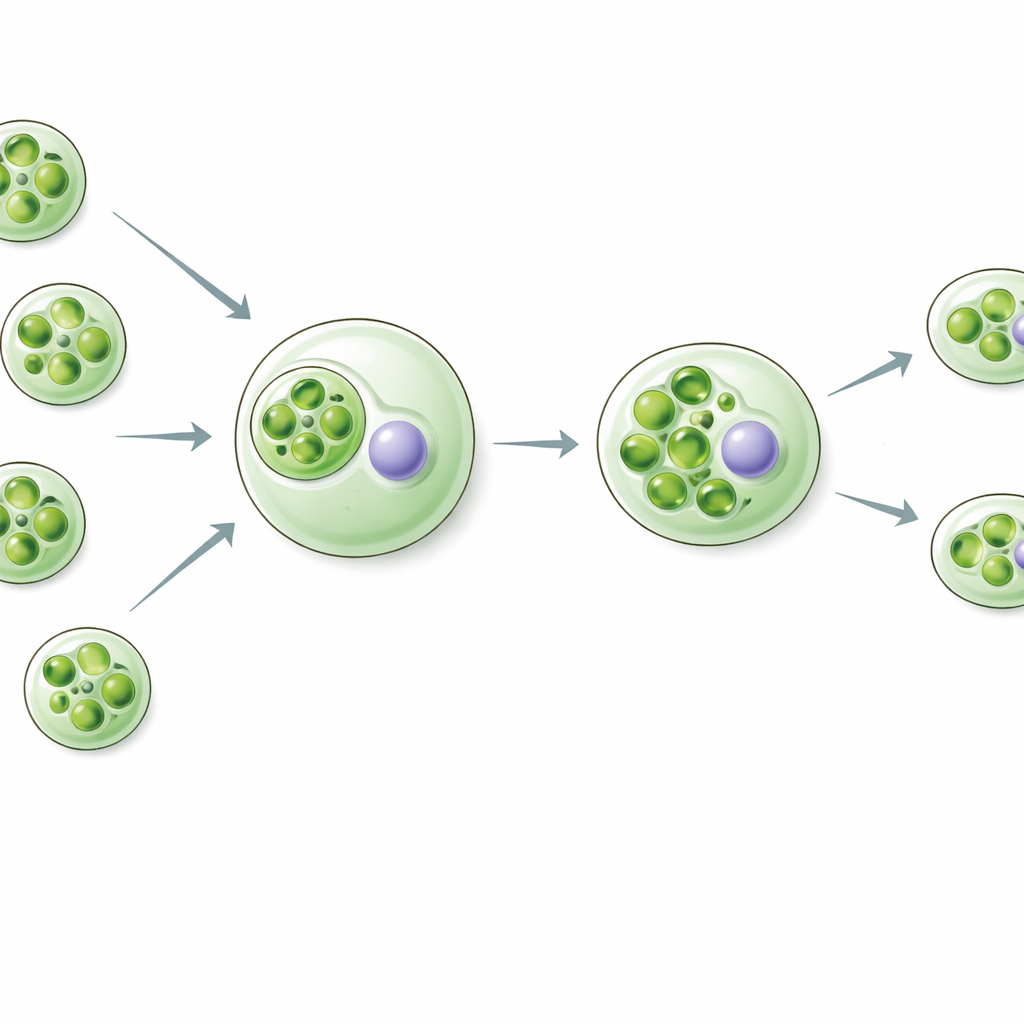
Genes do hospedeiro entram em ação para manter as peças roubadas vivas
Os pesquisadores fizeram uma pergunta crucial: se o núcleo algal se foi, quem fornece as proteínas necessárias para manter o kleptoplast funcionando? Ao analisar a atividade gênica ao longo do tempo em Rapaza, identificaram 37 genes do hospedeiro cujos produtos parecem operar dentro de cloroplastos. Muitos desses genes assemelham-se a componentes da maquinaria fotossintética — proteínas de captação de luz, partes do transporte de elétrons e enzimas que fixam carbono. Dois destacaram-se: uma proteína semelhante à pequena subunidade da RuBisCO (RvRbcS-like) e uma proteína semelhante à ativase da RuBisCO (RvRca-like). Ambas estão relacionadas a auxiliares-chave da RuBisCO, a enzima central que captura dióxido de carbono. Esses genes do hospedeiro são fortemente ativados após a predação, exatamente quando os kleptoplastos estão sendo remodelados e preparados para uso de longo prazo.
Provando que as proteínas do hospedeiro entram nos kleptoplastos
Encontrar sequências gênicas sugestivas não basta; as proteínas devem realmente alcançar o interior dos kleptoplastos. Usando anticorpos personalizados e microscopia fluorescente, a equipe rastreou onde as proteínas RvRbcS-like e RvRca-like se acumulam. Eles engenheiraram linhagens de Rapaza com pequenas etiquetas detectáveis em RvRbcS-like e mostraram que o sinal se sobrepunha aos kleptoplastos e à própria RuBisCO. Imagens semelhantes com um anticorpo contra RvRca-like revelaram que essa proteína também se concentra dentro dos kleptoplastos. Em géis de proteínas, ambas as proteínas apareceram encurtadas, consistente com a remoção de um segmento frontal especial à medida que cruzam membranas — exatamente como sinais de direcionamento que guiam proteínas para cloroplastos comuns.
Por que esses ajudantes emprestados importam
Para testar se essas proteínas do hospedeiro são realmente importantes, os autores usaram edição genômica baseada em CRISPR para eliminar cada gene. Células sem RvRbcS-like cresceram mal, perderam força fotossintética, produziram bem menos grãos de armazenamento ricos em energia e morreram muito mais cedo que o normal. Os níveis da grande subunidade da RuBisCO algal também caíram, sugerindo que, sem a subunidade pequena substituta do hospedeiro, o complexo enzimático se desmonta. A remoção de RvRca-like teve um efeito mais brando, mas ainda nítido: o crescimento inicial permaneceu próximo do normal, mas posteriormente a fotossíntese e o armazenamento de carbono declinaram, revelando perda gradual de eficiência. Juntos, esses resultados mostram que Rapaza não se limita a estacionar cloroplastos roubados; ele os mantém e remonta ativamente com seu próprio conjunto de proteínas.
Etiquetas de entrega sob medida e estruturas internas reconstruídas
A maioria das proteínas putativamente direcionadas aos kleptoplastos em Rapaza compartilha “cabeças” longas e de baixa estrutura em sua extremidade frontal, frequentemente com segmentos previstos para atravessar membranas. Ao fundir uma dessas cabeças a uma proteína repórter luciferase, os autores demonstraram que esse segmento sozinho basta para transportar uma proteína cargueira para os kleptoplastos. Análises detalhadas de sequência revelaram várias classes dessas regiões de direcionamento, que se assemelham muito às usadas por um grupo relacionado de algas para importar proteínas em seus cloroplastos permanentes de três membranas. Uma proteína do hospedeiro especialmente notável, RvRbcS-like, carrega quatro domínios relacionados à RuBisCO e uma cauda flexível rica em motivos repetidos, pensada para promover separação de fases de proteínas. Os autores propõem que essa cauda ajuda a reorganizar o pirenoide — o denso polo de fixação de carbono dentro do kleptoplast — em múltiplas gotas que podem ser herdadas pelas células-filhas.
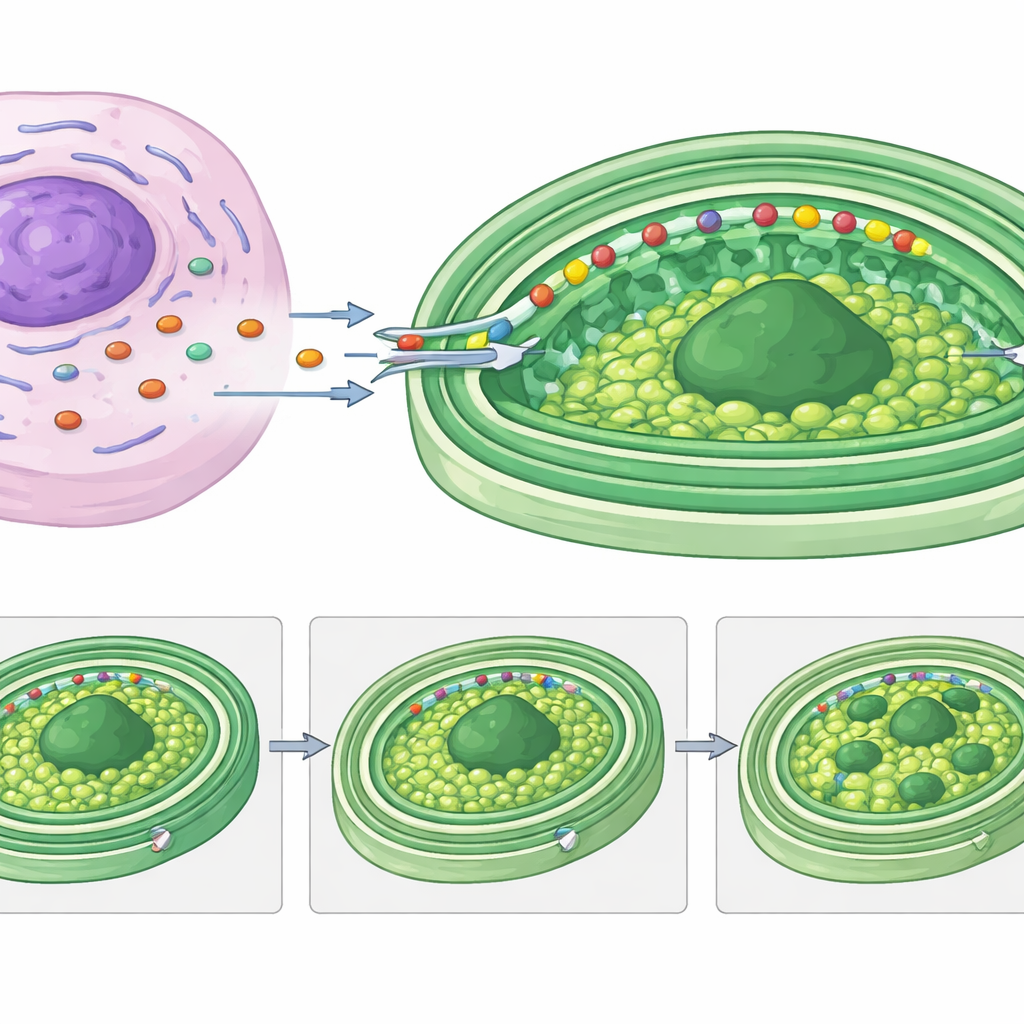
O que isso significa para a história das células complexas
Para quem não é especialista, a mensagem-chave é que Rapaza viridis mostra uma versão viva e reversível do que pode ter acontecido quando células antigas transformaram bactérias livres em componentes permanentes como cloroplastos. Aqui, o hospedeiro constrói rapidamente uma parceria molecular temporária: seus próprios genes fornecem peças de reposição cruciais e até remodelam a estrutura interna dos cloroplastos roubados, tudo guiado por etiquetas de entrega especializadas. Esse “quimerismo molecular transitório” demonstra que integrações entre espécies, mesmo de curta duração, podem ser sofisticadas e finamente ajustadas. Estudar esse sistema oferece aos cientistas um modelo poderoso para descobrir como células complexas aprenderam a controlar, alimentar e usar com segurança fábricas de energia estrangeiras — e como novas organelas ainda podem emergir ao longo do tempo evolutivo.
Citação: Kashiyama, Y., Maruyama, M., Nakazawa, M. et al. Transient molecular chimerism for exploiting xenogeneic organelles. Nat Commun 17, 2371 (2026). https://doi.org/10.1038/s41467-026-70516-x
Palavras-chave: kleptoplastia, evolução dos cloroplastos, Rapaza viridis, <keyword>biogênese de organelas