Clear Sky Science · pt
Caracterização sem rótulo de massa e tamanho de biomoléculas de poucas kDa por meio de microscopia de espalhamento nanofluídico augmentada por transformador visual hierárquico
Vendo as Menores Moléculas
Muitos dos mensageiros mais importantes do corpo — como hormônios e sinais do sistema imune — são tão minúsculos que permaneciam praticamente invisíveis para poderosos microscópios, exceto quando marcados com rótulos fluorescentes. Esses rótulos podem alterar o comportamento das moléculas, um problema sério para o desenvolvimento de fármacos e a biologia básica. Este estudo apresenta uma maneira de pesar e medir individualmente moléculas tão pequenas quanto a insulina sem qualquer rótulo, usando uma combinação de chips nanofluidicos e inteligência artificial avançada. Isso abre um caminho para observar moléculas biológicas-chave em seu estado natural, uma a uma.
Canais Minúsculos como Tubos de Ensaio
No cerne do método está a microscopia de espalhamento nanofluídico, que usa um chip do tamanho de uma unha gravado com canais extremamente estreitos. Esses canais têm apenas algumas dezenas de nanômetros de largura — milhares de vezes mais finos que um fio de cabelo humano. Moléculas dissolvidas em um tampão derivam livremente por esses canais, em vez de ficarem presas a uma superfície. Quando o chip é iluminado com luz visível, tanto as paredes do canal quanto qualquer molécula em trânsito espalham luz. Como o canal é muito maior que a molécula, as luzes espalhadas interferem de modo a amplificar substancialmente a assinatura óptica da molécula. Ao subtrair imagens de um canal vazio das imagens tomadas quando há uma molécula presente, os pesquisadores obtêm um registro em estilo de filme (um quimógrafo) de sua passagem pelo canal, contendo informações tanto sobre sua massa quanto sobre a rapidez com que ela difunde.
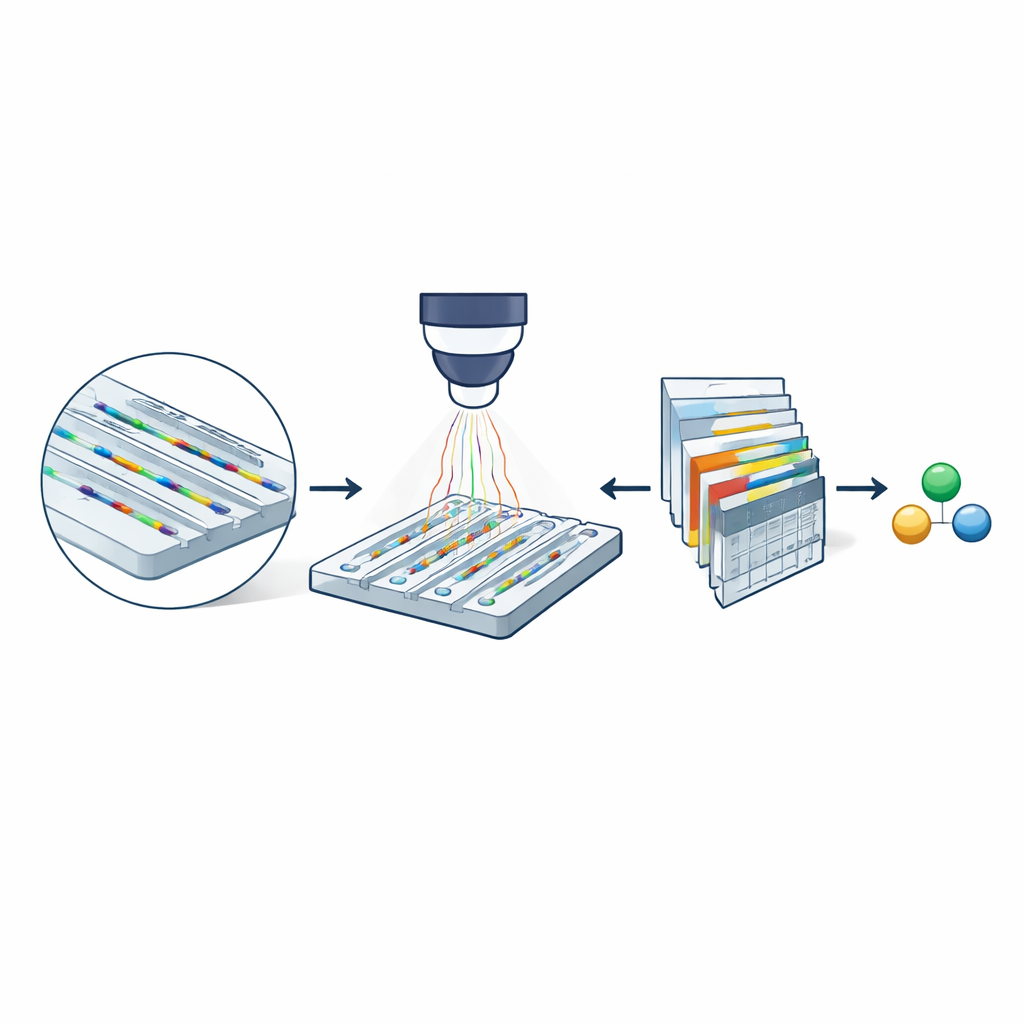
Por Que Canais Menores Importam
Mesmo com esse reforço óptico, versões anteriores da técnica só conseguiam caracterizar moléculas com massa superior a cerca de 60 kilodaltons — proteínas grandes típicas — porque sinais de espécies menores se afogavam no ruído. A equipe mostra que reduzir a seção transversal dos nanocanais melhora dramaticamente a sensibilidade: o contraste óptico de uma molécula aumenta à medida que a área do canal diminui. Experimentos comparando dois tamanhos de canal com a proteína albumina sérica bovina revelam que seu trajeto é claramente visível no canal mais estreito, mas quase desaparece no mais largo. Essa mudança geométrica simples indica que, em princípio, biomoléculas muito menores podem ser detectáveis se seus sinais fracos puderem ser extraídos de forma confiável de sequências de imagens ruidosas.
Deixando uma IA Ler Filmes Ruidosos
Para atingir esse regime, os pesquisadores desenvolveram um modelo de deep learning especializado chamado transformador visual hierárquico. Em vez de tentar reconstruir o trajeto exato de cada molécula pixel a pixel, o modelo examina o quimógrafo em múltiplas escalas e produz dois resultados: um mapa de probabilidade que marca onde uma molécula provavelmente está em cada ponto no espaço e no tempo, e um mapa de propriedades que codifica estimativas de massa molecular e tamanho hidrodinâmico. Ao ponderar as estimativas de propriedades com o mapa de probabilidade, o modelo pode ignorar regiões que são majoritariamente ruído. O treinamento depende inteiramente de trajetórias simuladas sobrepostas ao ruído de fundo medido experimentalmente, permitindo que o sistema aprenda como sinais reais devem parecer mesmo quando mal visíveis a olho nu.
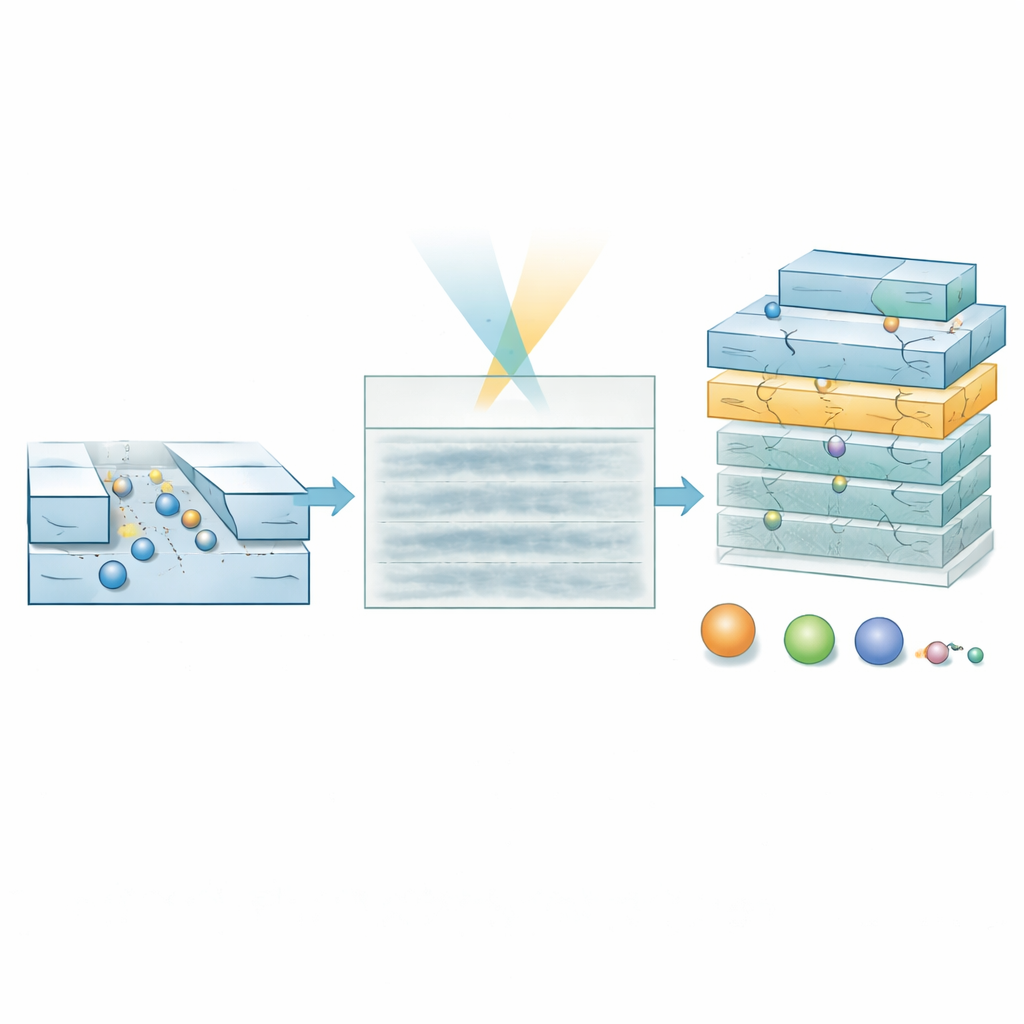
Testes com DNA e Moléculas Hormonais
Os autores primeiro validaram a abordagem usando uma “escada” padrão de DNA, uma mistura de fragmentos de fita dupla de comprimentos e massas conhecidas, em canais relativamente largos onde todos os fragmentos estão deliberadamente abaixo do limite usual de detecção. Nos filmes brutos, não é possível ver trilhas claras de DNA. Ainda assim, o modelo de IA produz mapas de probabilidade que destacam corretamente onde as moléculas passam e prevê massas que correspondem aos valores esperados, uma vez filtrados os dados de baixa confiança. O método também relata corretamente tamanhos efetivos menores para os fragmentos rígidos e semelhantes a varetas do DNA do que seu comprimento físico total, refletindo como sua forma afeta a difusão. O teste mais exigente usou canais ultrasmalls para estudar o hormônio peptídico insulina, que pesa apenas cerca de 5,8 kilodaltons e tem aproximadamente 1,5 nanômetros de diâmetro. Aqui também, os quimógrafos parecem sem características, mas o modelo extrai um aglomerado estreito de valores de massa e tamanho em excelente acordo com números da literatura, claramente separado dos controles contendo apenas tampão.
Empurrando os Limites
Para entender até onde essa estratégia pode chegar, a equipe comparou a precisão do modelo com o limite inferior de Cramér–Rao, um limite estatístico que define a melhor acurácia possível para qualquer estimador não viesado dado o ruído nos dados. Usando grandes conjuntos de simulações, mostram que, à medida que o número de quadros que contribuem para a trajetória de uma molécula excede cerca de dez mil, as estimativas de massa e tamanho do modelo se aproximam desse ótimo teórico mesmo para uma partícula de seis kilodaltons. Experimentos com insulina em diferentes concentrações reproduzem a mesma tendência: trajetórias efetivas mais longas geram medições mais precisas, limitadas principalmente pelo tempo que pequenas moléculas de difusão rápida permanecem no campo de visão. Os autores propõem estratégias futuras — como aprisionar suavemente moléculas nos canais ou reutilizar dados com bootstrap — para aumentar ainda mais o tempo observável útil.
O Que Isso Significa para Biologia e Medicina
Em termos práticos, este trabalho mostra que agora é possível pesar e medir individualmente algumas das menores e mais importantes moléculas do organismo, sem tocar nelas com marcadores fluorescentes ou prendê-las a uma superfície. Ao casar canais nanofabricados com uma IA projetada para ler filmes ruidosos de espalhamento de luz, o método reduz o limite de detecção de massa dessa abordagem de microscopia sem rótulos em cerca de um fator de dez. Isso abre a porta para estudar famílias de pequenas proteínas de sinalização e hormônios peptídicos — como citocinas, quimiocinas e insulina — no nível de uma única molécula, e para caracterizar nanopartículas biológicas minúsculas e transportadores de fármacos com sensibilidade sem precedentes. À medida que a tecnologia amadurecer, ela pode se tornar uma ferramenta poderosa na descoberta de fármacos, diagnóstico e em estudos fundamentais de como as interações moleculares moldam a vida nas menores escalas.
Citação: K. Moberg, H., Yeroshenko, B., Fritzsche, J. et al. Label-free mass and size characterization of few-kDa biomolecules by hierarchical vision transformer augmented nanofluidic scattering microscopy. Nat Commun 17, 2533 (2026). https://doi.org/10.1038/s41467-026-70514-z
Palavras-chave: microscopia de uma molécula sem rótulo, espalhamento nanofluídico, transformador visual, pequenas biomoléculas, detecção de insulina