Clear Sky Science · pt
Um atlas de interações em todo um gênero entre ortólogos de NS4B identifica um papel conservado da UFMilação na replicação de ortoflavivírus
Por que este estudo sobre vírus é importante
Vírus como dengue, Zika e West Nile estão se espalhando para novas regiões e podem causar desde febre até infecções cerebrais e malformações congênitas. Ainda assim, carecemos de tratamentos amplos e confiáveis. Este estudo explora como uma parceria oculta entre esses vírus e um sistema celular pouco conhecido de marcação chamado UFMilação ajuda os patógenos a se multiplicarem. Ao mapear essa relação em vários vírus relacionados, os autores descobrem um ponto fraco compartilhado que pode ser explorado para desenvolver futuros antivirais.
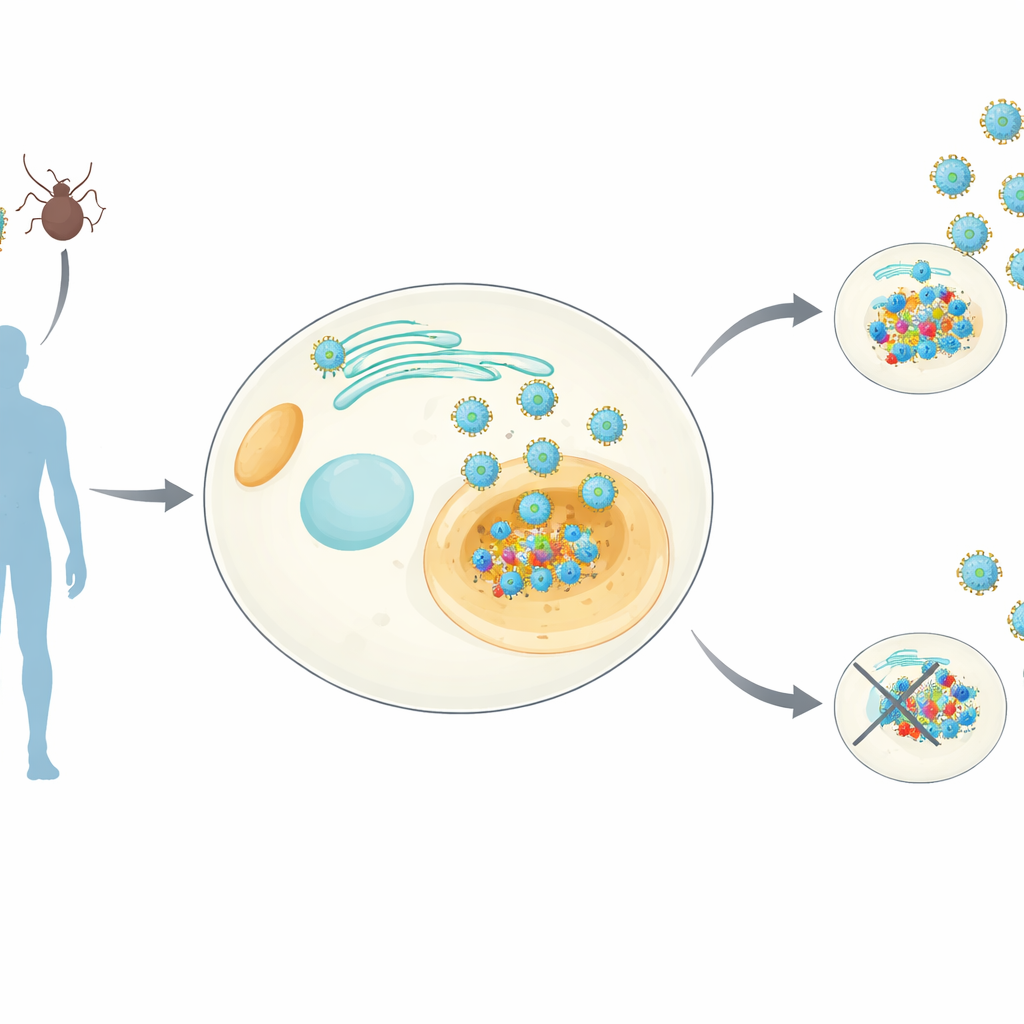
Seguindo um informante viral-chave
Os ortoflavivírus – o grupo que inclui dengue, Zika, febre amarela e outros – todos carregam uma pequena proteína chamada NS4B que se aloja nas membranas dentro de nossas células. Sabe‑se que a NS4B é essencial para a replicação viral, mas suas funções exatas permaneceram obscuras. Os pesquisadores criaram linhagens celulares humanas que produzem de forma estável a NS4B de oito ortoflavivírus diferentes. Em seguida, usaram técnicas sensíveis de espectrometria de massa para puxar a NS4B junto com quaisquer proteínas humanas associadas a ela, e, em paralelo, mediram como a expressão de NS4B altera o conjunto geral de proteínas na célula. Isso produziu um “atlas de interações” em nível de gênero – que eles chamam de NS4Bome – mostrando tanto alvos hospedeiros comuns quanto específicos de cada vírus.
Truques compartilhados e adaptações específicas
O atlas revelou 538 proteínas humanas que interagem com NS4B e mais de 500 cuja abundância muda quando NS4B está presente. Muitas dessas proteínas se concentram em vias que gerenciam a produção de energia nas mitocôndrias, a modelagem de membranas internas e o tráfego de proteínas e lipídios recém-sintetizados. Algumas interações foram compartilhadas pela maioria dos vírus, indicando truques preservados evolutivamente que todos os ortoflavivírus utilizam. Outras apareceram apenas em certas espécies ou cepas, potencialmente explicando por que alguns vírus preferem mosquitos a carrapatos, ou causam doenças cerebrais em vez de febre hemorrágica. Essa visão sistemática transforma um conjunto confuso de estudos fragmentados anteriores em um mapa coerente de como esses vírus reprogramam a célula.
Um aliado surpreendente: o sistema de UFMilação
Entre os muitos parceiros aos quais a NS4B se ligou, um se destacou: UBA5, a enzima inicial da via de UFMilação. A UFMilação é um sistema celular que anexa uma pequena proteína sinalizadora, UFM1, a alvos selecionados, influenciando processos como controle de qualidade proteica e respostas ao estresse. Utilizando interferência por RNA e nocaute gênico baseado em CRISPR, a equipe mostrou que células sem UBA5 ou incapazes de realizar UFMilação apresentaram replicação drasticamente reduzida de Zika e de vários vírus relacionados. Reintroduzir UBA5 normal restaurou o crescimento viral, enquanto formas mutantes que não podiam mais promover a UFMilação não o fizeram, provando que a atividade de marcação em si é crucial para a infecção.
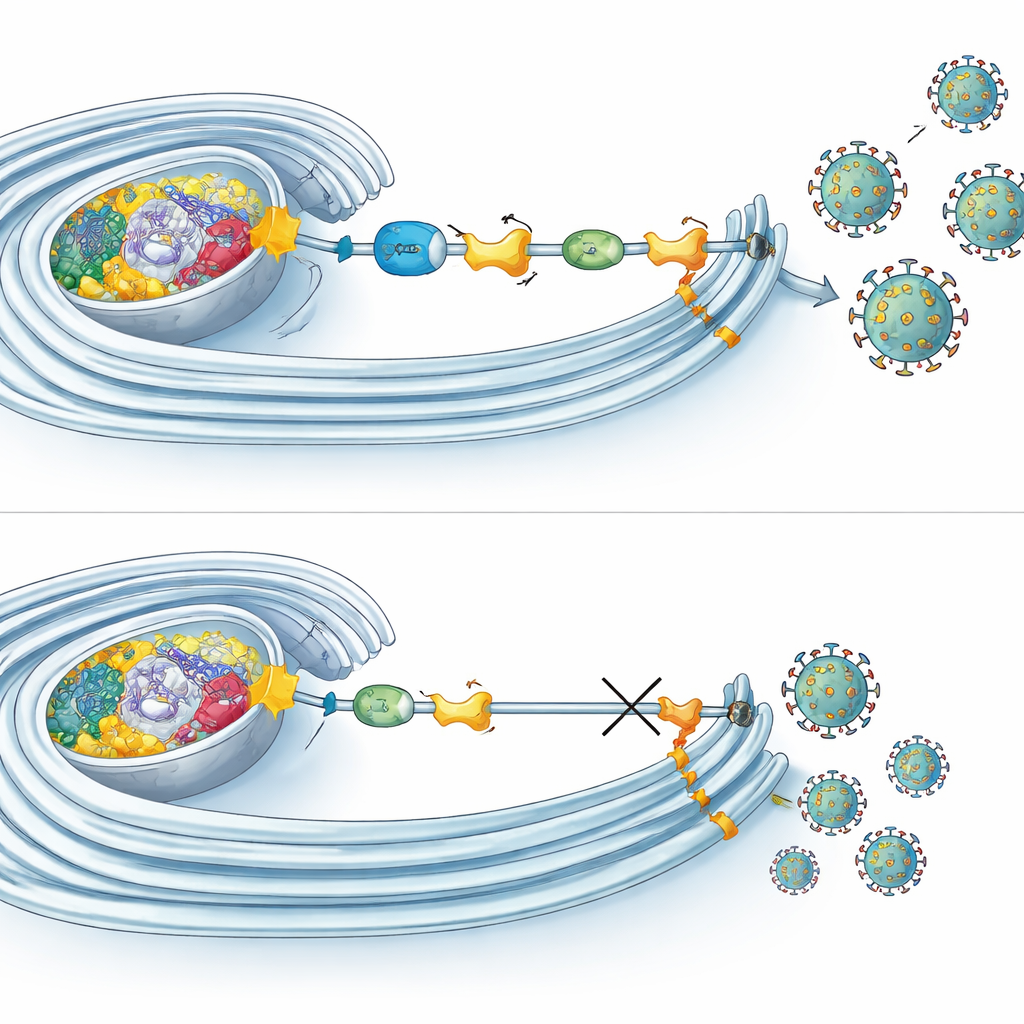
Como a marcação sustenta as fábricas virais
Experimentos de microscopia e bioquímica revelaram que múltiplos componentes da UFMilação se reúnem exatamente nos locais onde o RNA viral é copiado dentro de membranas remodeladas. Ali, eles se associam não apenas com NS4B, mas também com outras proteínas virais que montam a maquinaria de replicação. Curiosamente, bloquear a UFMilação não interrompeu a entrada viral, a produção de RNA ou a síntese proteica. Em vez disso, prejudicou principalmente as fases tardias do ciclo, como a montagem ou liberação de partículas infecciosas. Ao mesmo tempo, a UFMilação influenciou como as mitocôndrias respiram: quando a via foi desabilitada, as células apresentaram consumo de oxigênio reduzido e formas mitocondriais alteradas. Em contraste, no início da infecção por Zika, a respiração mitocondrial aumentou, sugerindo que os vírus podem explorar a UFMilação para impulsionar a produção de energia da célula justamente quando mais precisam.
Testando um medicamento em células e peixinhos
Os autores então testaram um composto de pequena molécula, DKM 2‑93, que bloqueia o sítio ativo da UBA5. Em células humanas cultivadas, esse inibidor reduziu a produção do vírus Zika em cerca de dez vezes em doses que deixaram as células em grande parte saudáveis, e mostrou atividade em vários tipos celulares. Para avaliar se essa estratégia poderia funcionar em um organismo vivo, usaram um modelo de zebrafish de infecção por Zika, que imita características-chave da doença no cérebro em desenvolvimento. Tratar embriões infectados com DKM 2‑93 durante o desenvolvimento cerebral precoce reduziu significativamente os níveis de RNA viral e diminuiu a proporção de peixes com malformações graves, indicando benefício antiviral genuíno in vivo.
O que isso significa para tratamentos futuros
Ao construir um mapa abrangente de como a NS4B de muitos ortoflavivírus interage com proteínas humanas, este estudo destaca a UFMilação como uma via auxiliar conservada da qual esses vírus dependem para produzir partículas infecciosas. Como o mesmo sistema hospedeiro parece apoiar dengue, Zika, West Nile e outros, drogas que reduzam seletivamente a UFMilação podem atuar como antivirais de amplo espectro, em vez de visar um único vírus por vez. Embora sejam necessários mais estudos para entender exatamente quais proteínas são marcadas e para garantir segurança, os achados identificam um alvo promissor baseado no hospedeiro que um dia poderá ajudar a conter surtos de múltiplas doenças transmitidas por mosquitos e carrapatos com uma única abordagem terapêutica.
Citação: Rajasekharan, S., Barragan Torres, V.A., Pinheiro Gomes, Y.C. et al. A genus-wide interaction atlas across NS4B orthologues identifies a conserved role for UFMylation in orthoflavivirus replication. Nat Commun 17, 2489 (2026). https://doi.org/10.1038/s41467-026-70437-9
Palavras-chave: vírus Zika, dengue, interações hospedeiro–vírus, UFMilação, antivirais de amplo espectro