Clear Sky Science · pt
Modificações ribossômicas estão associadas à seleção do destino mesenquimal na linhagem da crista neural
Como pequenas fábricas celulares moldam rostos e tumores
Nossos rostos e partes do sistema nervoso são construídos a partir de um grupo migratório de células embrionárias chamado crista neural. Essas células podem se transformar em osso, cartilagem, nervos e mais. Este estudo mostra que suas escolhas são influenciadas não apenas por genes, mas por ajustes químicos sutis nas máquinas de fabricar proteínas da célula — os ribossomos. As mesmas características moleculares que ajudam a construir um rosto normal podem, quando mal reguladas, assinalar formas mais perigosas de câncer infantil.
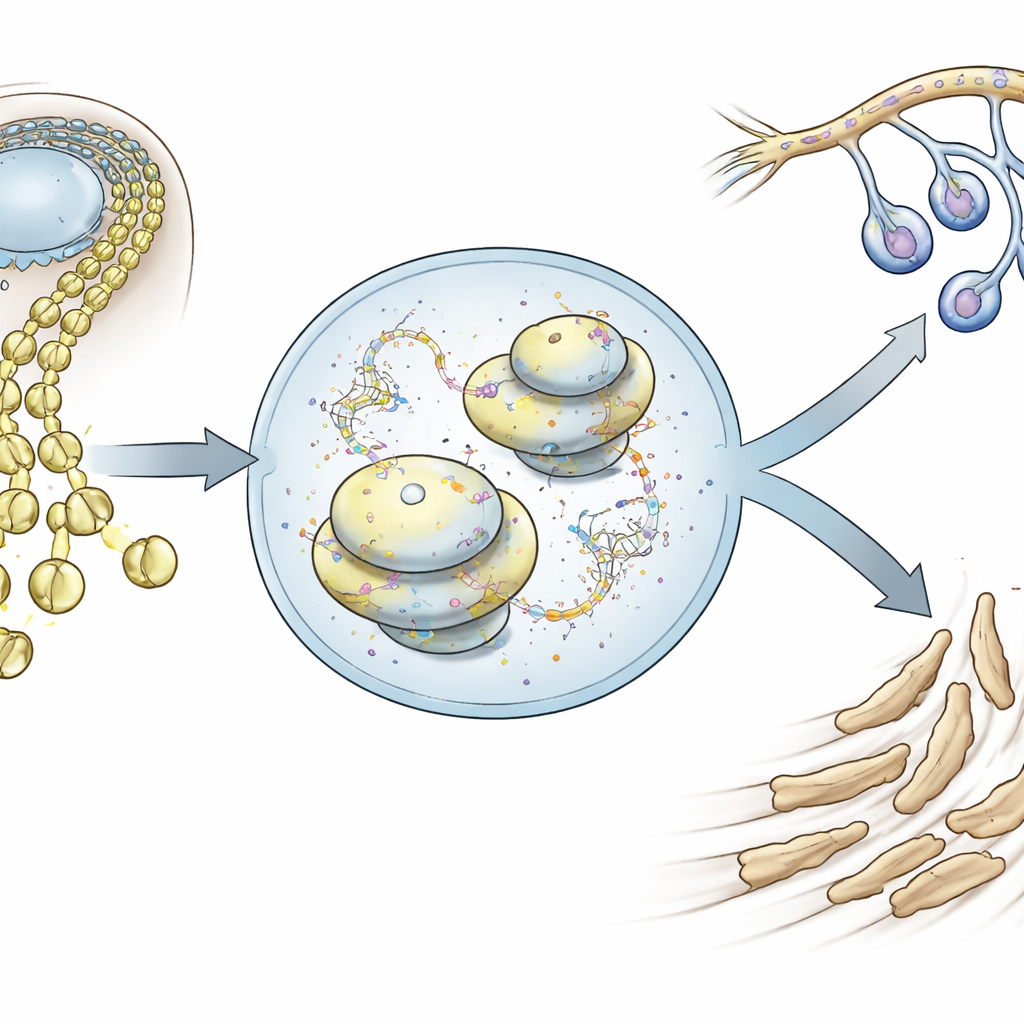
Células metamórficas que constroem o rosto
As células da crista neural surgem ao longo do cérebro e da medula espinhal em desenvolvimento e depois migram para fora, formando grande parte do crânio, das mandíbulas e dos nervos periféricos. Usando sequenciamento de RNA de célula única em embriões de camundongo, os autores rastrearam milhares de células individuais da crista neural craniana à medida que deixavam o tubo neural e se deslocavam para a face. Eles descobriram que, muito cedo, essas células já mostram uma inclinação sutil para um de dois destinos principais: um caminho mesenquimal que formará ossos e cartilagens faciais, ou um caminho neuro-glial que dará origem a neurônios e células de suporte glial. Esses dois programas de atividade gênica estão inicialmente misturados nas mesmas células, mas tornam-se mutuamente exclusivos conforme o desenvolvimento avança, forçando uma decisão de destino.
Fábricas de proteína como tomadoras de decisão
Ao examinar quais genes se associavam ao viés inicial em direção ao mesênquima facial, a equipe identificou dois grandes grupos. Um continha atores já conhecidos que impulsionam as células a afrouxar-se, migrar e mudar de identidade, um processo conhecido como transição epitélio-mesenquimal. O outro, mais surpreendente, centrava-se na montagem de ribossomos e na modificação química do RNA ribossômico, o núcleo da maquinaria de síntese proteica. Em vez de simplesmente produzir mais ribossomos, as células da crista neural craniana ativaram fatores que afinam como os ribossomos são montados e quimicamente marcados. Perturbar a produção de RNA ribossômico em embriões de camundongo no momento da escolha de destino poupou em grande parte o desenvolvimento dos nervos, mas prejudicou severamente as estruturas esqueléticas faciais, mostrando que a via mesenquimal é especialmente dependente desse controle ribossômico.
Uma marca especial no RNA ribossômico
Aprofundando-se, os pesquisadores focaram em um único nucleotídeo dentro do RNA ribossômico 18S, em uma posição crucial para a precisão da síntese proteica. Em células da crista neural craniana enviesadas para destinos mesenquimais, o sequenciamento repetidamente interpretou mal essa posição, um sinal de intensa modificação química em vez de mutação verdadeira. Trabalhos anteriores mostraram que um trio de enzimas adiciona uma modificação complexa nesse sítio por meio de várias etapas. Ao combinar dados genômicos e de RNA humanos com espectrometria de massa de tecidos embrionários de camundongo, o estudo confirmou que esse sítio é normal no DNA, mas quimicamente alterado em graus variados no RNA, e que a proporção dessa forma modificada difere entre tecidos cerebrais e faciais. Superexpressão ou exclusão das enzimas que constroem essa modificação em culturas celulares e em embriões de camundongo perturbou o desenvolvimento da crista neural e produziu defeitos craniofaciais marcantes, ressaltando que níveis precisos dessa marca de RNA ajudam a direcionar as células para a via esquelética.
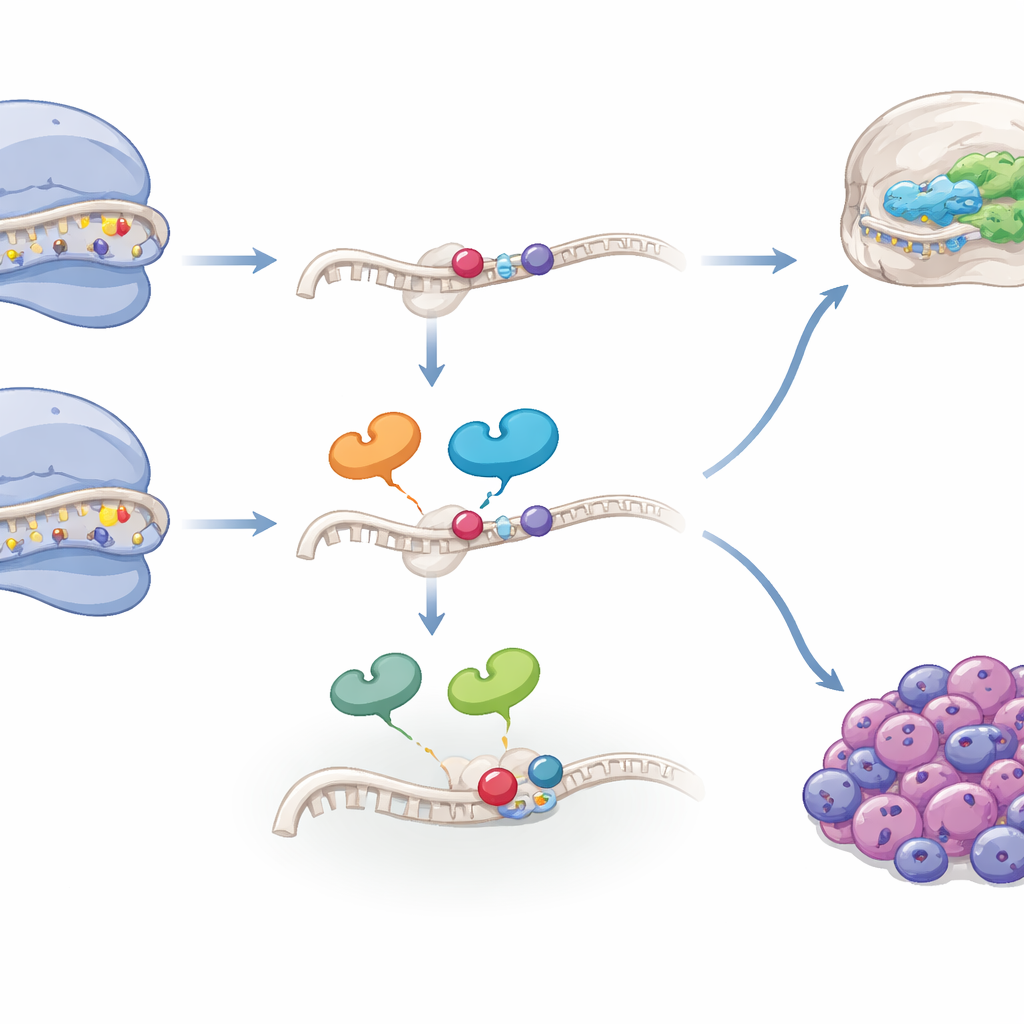
Do desenvolvimento ao risco de câncer
Como as células da crista neural também podem originar tumores como o neuroblastoma, os autores investigaram se as mesmas características ribossômicas aparecem no câncer. Analisando dados de RNA de célula única e em amostras em massa de vários coortes de neuroblastoma e tumores cerebrais, eles encontraram que uma assinatura gênica de “controle ribossômico e modificação de RNA” está enriquecida em subpopulações tumorais com traços mais semelhantes ao mesênquima — estados frequentemente associados à resistência a terapias e prognóstico ruim. Em múltiplos coortes de pacientes, níveis altos dessa assinatura previram fortemente pior sobrevida, particularmente em casos de neuroblastoma sem amplificação do conhecido gene de risco MYCN. Componentes específicos, como o fator de montagem WDR74 e a enzima de modificação TSR3, estavam elevados em linhagens celulares agressivas e tornavam essas células mais vulneráveis a fármacos que estressam o ribossomo. Curiosamente, tumores com níveis muito baixos ou muito altos da modificação chave de RNA no sítio destacado tiveram desfechos piores do que aqueles com níveis intermediários, sugerindo que tanto a deficiência quanto o excesso desse pool de ribossomos especializados podem ser prejudiciais.
O que isso significa para rostos e cânceres infantis
Em conjunto, esses achados sugerem que os ribossomos não são apenas fábricas passivas de proteínas, mas dispositivos ajustados cuja composição química ajuda a decidir como células embrionárias constroem o rosto e como alguns tumores se comportam. Em células da crista neural, uma marca química particular no RNA ribossômico parece favorecer a produção de proteínas necessárias à formação de osso e cartilagem faciais, enquanto sua desregulação no câncer está ligada a células tumorais mais perigosas e metamórficas. Compreender e, potencialmente, direcionar esse “detalhe fino” ribossômico pode abrir novas maneiras de prevenir malformações craniofaciais e de identificar ou tratar neuroblastomas de alto risco.
Citação: Poverennaya, I., Murtazina, A., Li, L. et al. Ribosomal modifications are associated with mesenchymal fate selection in the neural crest lineage. Nat Commun 17, 2326 (2026). https://doi.org/10.1038/s41467-026-70375-6
Palavras-chave: desenvolvimento da crista neural, modificações do ribossomo, formação craniofacial, neuroblastoma, ribossomos especializados