Clear Sky Science · pt
Controle da função lisossomal pela proteína ativadora de GTPase TBC1D9B e seu parceiro de ligação TMEM55B
Como os centros de reciclagem das células mantêm o equilíbrio
Dentro de cada uma de nossas células existem pequenas bolsas chamadas lisossomos que atuam como centros de reciclagem e centros de controle para o crescimento. Quando funcionam bem, peças desgastadas são degradadas e seus componentes são reutilizados; quando falham, os resíduos se acumulam e doenças, incluindo neurodegeneração e câncer, podem surgir. Este estudo revela como duas proteínas pouco conhecidas ajudam a alternar os lisossomos entre um estado de circulação, favorável ao crescimento, e um modo agrupado, voltado para a limpeza de resíduos, lançando luz sobre como as células se adaptam a fartura e escassez.
Movendo os centros de reciclagem pela célula
Os lisossomos não são fixos. Eles viajam ao longo de trilhos internos, puxados para fora por um conjunto de motores moleculares e atraídos para dentro por outro. A posição deles na célula importa: quando os nutrientes são abundantes, os lisossomos se espalham em direção às regiões externas da célula e ajudam a sustentar sinais de crescimento; quando o alimento é escasso, eles recuam para o centro, tornam‑se mais ácidos e aumentam a degradação do material celular. Uma pequena proteína tipo interruptor chamada ARL8 é conhecida por empurrar os lisossomos para fora, mas até agora ninguém havia identificado um sistema de freio dedicado para contê‑la. Os autores suspeitaram que tal freio seria crucial para permitir que as células mudem rapidamente para um modo de conservação durante a inanição.
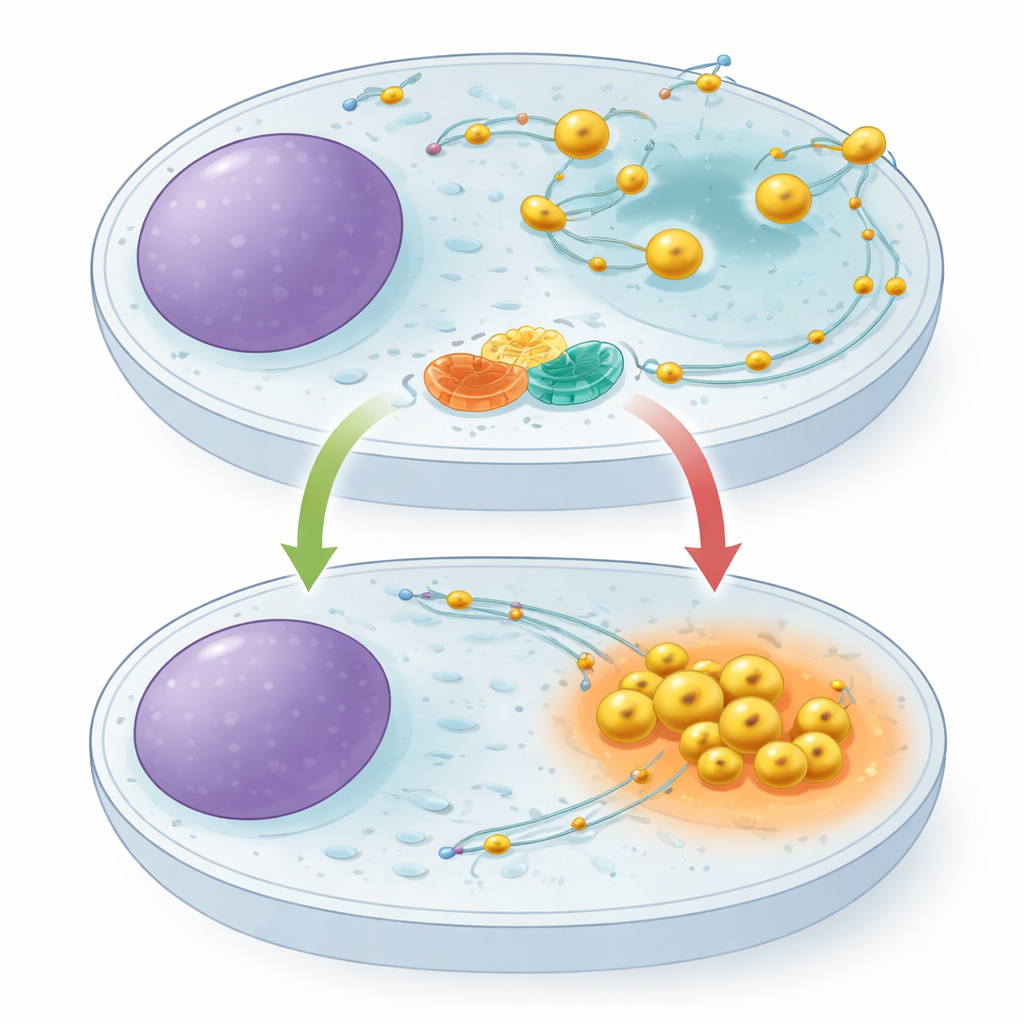
Uma parceria molecular na superfície do lisossomo
Usando técnicas de "pesca" de proteínas e espectrometria de massa, os pesquisadores descobriram que uma proteína chamada TBC1D9B se liga a uma proteína de membrana lisossomal chamada TMEM55B. TMEM55B atravessa a casca externa do lisossomo, enquanto TBC1D9B é em grande parte solúvel e pode se acoplar à membrana. A equipe mostrou que essas duas formam um complexo direto: TBC1D9B purificado adere à parte exposta de TMEM55B em tubos de ensaio, e versões marcadas das proteínas se precipitam mutuamente a partir de extratos celulares. Mapas cuidadosos dos segmentos protéicos revelaram que várias regiões de TBC1D9B contactam TMEM55B, posicionando TBC1D9B na superfície do lisossomo sem bloquear a parte da proteína responsável por sua atividade catalítica.
Quando o freio falha, os lisossomos se descontrolam
Para descobrir o que essa parceria faz, os autores usaram edição CRISPR para remover TMEM55B ou TBC1D9B de células humanas. Em ambos os casos, os lisossomos deixaram de se agrupar perto do núcleo e, em vez disso, se dispersaram em direção à periferia da célula e se moveram mais rápido ao longo de seus trilhos, imitando células em estado constantemente alimentado. Reintroduzir TBC1D9B normal restaurou o posicionamento adequado, mas uma versão sem poder catalítico não o fez, indicando que sua atividade enzimática é essencial. Quando as células foram submetidas à privação de nutrientes, as células controle puxaram seus lisossomos para dentro e aumentaram seu poder digestivo, como mostrado pelo aumento da atividade de enzimas-chave e pela intensificação da degradação de cargas‑teste. Células sem TMEM55B ou TBC1D9B não conseguiram fazer isso: seus lisossomos permaneceram periféricos e sua resposta degradativa à inanição foi atenuada. A autofagia, o processo pelo qual as células se autodigerem componentes danificados, também foi prejudicada, com processamento menos eficiente de um repórter de autofagia e acúmulo da proteína adaptadora p62.
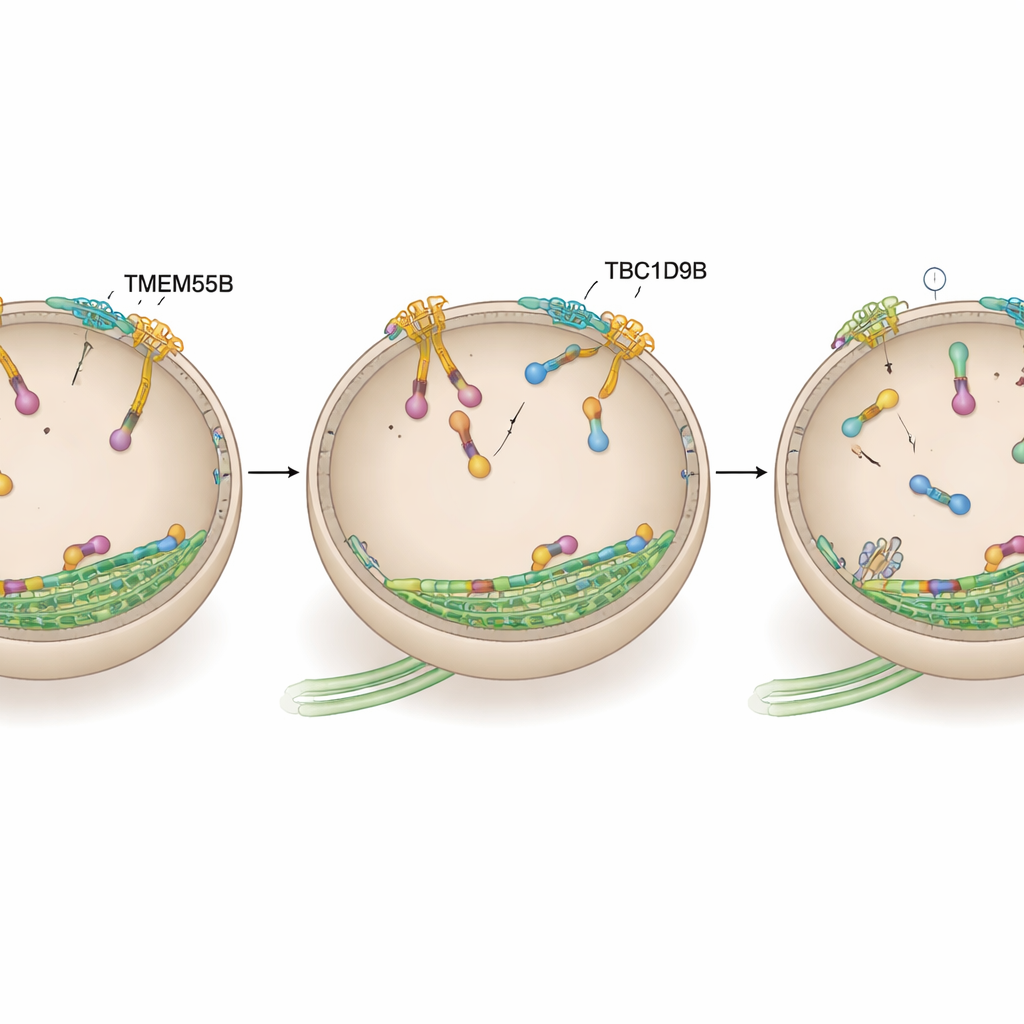
Desligando o motor lisossomal
A equipe então perguntou se TBC1D9B exerce seus efeitos agindo diretamente sobre ARL8, o interruptor motor que dirige para fora. Usando marcação por proximidade em neurônios humanos e testes de ligação em linhagens celulares e proteínas purificadas, eles mostraram que TBC1D9B se liga seletivamente à forma ativa, carregada de GTP, da variante ARL8B, mas não à sua forma inativa nem à ARL8A intimamente relacionada. Modelagem estrutural previu que resíduos-chave em TBC1D9B contactam o pocket de GTP de ARL8B. Em ensaios bioquímicos, TBC1D9B acelerou a hidrólise do GTP ligado a ARL8B, convertendo efetivamente a proteína de seu estado “ligado” para o estado “desligado”; uma versão mutante de TBC1D9B sem esses resíduos já não conseguia fazê‑lo. Consistente com isso, células sem TMEM55B ou TBC1D9B mostraram aumento de ARL8B nos lisossomos, enquanto a superexpressão de TBC1D9B trouxe os lisossomos de volta para o centro, semelhante a reduzir a atividade de ARL8B.
Um novo botão de controle para a manutenção celular
Finalmente, os autores testaram se esse freio sobre ARL8B explica as mudanças celulares observadas quando falta TBC1D9B. Quando ARL8B foi depletado, os lisossomos permaneceram agrupados perto do núcleo independentemente da presença de TMEM55B ou TBC1D9B, e os defeitos na autofagia causados pela perda de TBC1D9B foram em grande parte revertidos. Em conjunto, os dados sustentam um modelo no qual TMEM55B recruta TBC1D9B aos lisossomos, onde ele inativa ARL8B e permite que os lisossomos mudem de um estado disperso, que apoia o crescimento, para um estado centralizado, focado na digestão. Para não especialistas, isso significa que o estudo revelou um disco importante que as células usam para decidir quando reciclar com mais vigor, um processo com implicações para distúrbios de acúmulo de resíduos no cérebro, metabolismo e câncer.
Citação: Duhay, V., Tian, M., Kosieradzka, K. et al. Control of lysosome function by the GTPase-activating protein TBC1D9B and its binding partner TMEM55B. Nat Commun 17, 2487 (2026). https://doi.org/10.1038/s41467-026-70345-y
Palavras-chave: lisossomos, autofagia, sinalização celular, transporte de organelas, neurodegeneração