Clear Sky Science · pt
NAA40 e NAC cooperam na acetilação cotradução de histonas em humanos
Como as células afinam seus interruptores genéticos
Dentro de cada célula humana, proteínas recém-produzidas são quimicamente modificadas à medida que emergem das máquinas de fabricação de proteínas da célula, os ribossomos. Esses pequenos ajustes podem decidir para onde uma proteína vai, quanto tempo ela dura e até como nossos genes são ativados ou silenciados. Este artigo foca em uma proteína altamente específica chamada NAA40 e em um complexo cooperador chamado NAC, revelando como eles atuam juntos no ribossomo para modificar proteínas histonas — os carretéis em torno dos quais o DNA é enrolado — e, assim, influenciar a atividade gênica e potencialmente o desenvolvimento do câncer.
Uma pequena capa que muda o comportamento das histonas
Muitas proteínas humanas recebem uma pequena capa química em sua extremidade inicial, um processo conhecido como acetilação N-terminal. As histonas H2A e H4, que ajudam a empacotar o DNA em cromatina, são quase sempre modificadas dessa forma. A NAA40 é incomum entre as enzimas porque se especializa praticamente só em adicionar essa capa nessas histonas enquanto elas estão sendo produzidas. Essa marca de acetil compete com outras modificações químicas, como fosforilação e metilação, na mesma região das histonas, de modo que a atuação ou não da NAA40 pode alterar o grau de compactação do DNA e a regulação gênica. Importante, níveis alterados de NAA40 têm sido associados a vários tipos de câncer, tornando-a um alvo promissor para novas terapias.
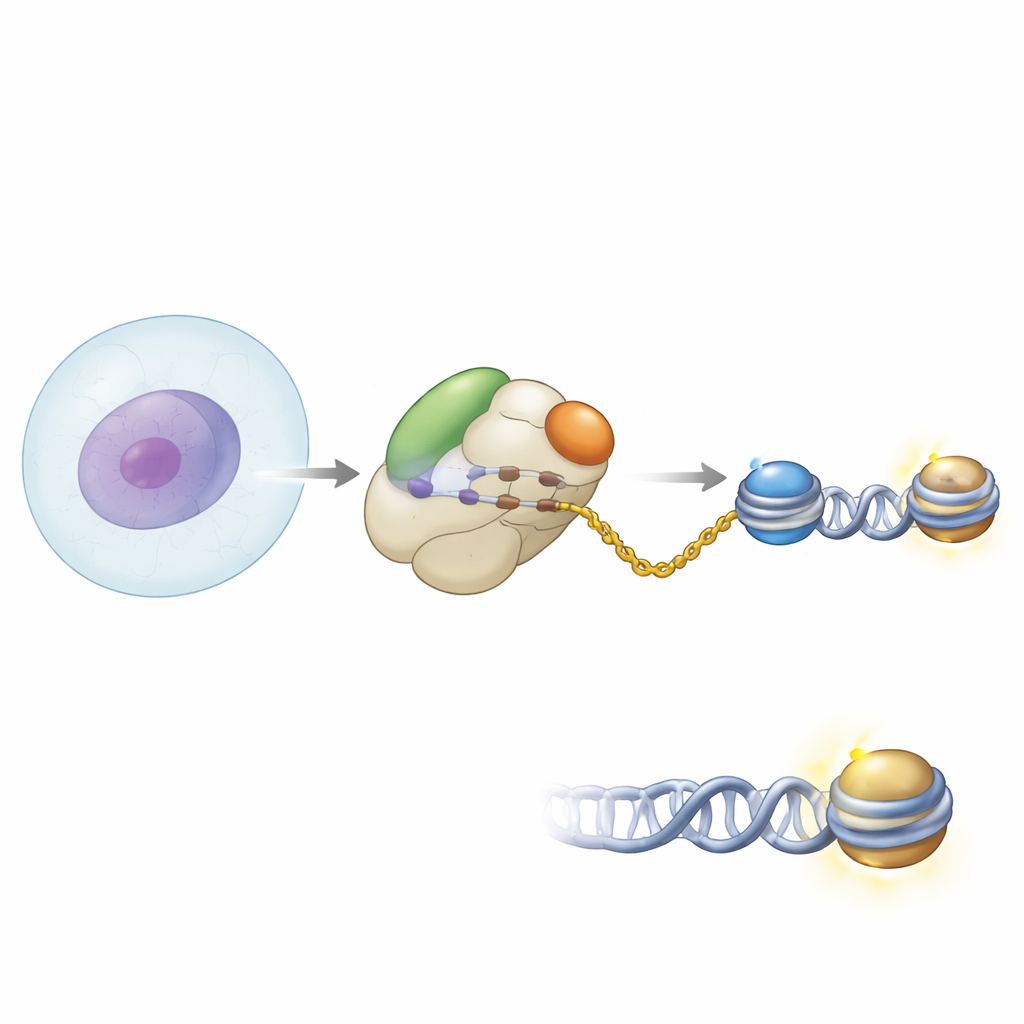
Parceria na entrada da fábrica de proteínas
Os autores usaram métodos bioquímicos e criomicroscopia eletrônica de alta resolução para ver como a NAA40 se posiciona no ribossomo humano. Eles descobriram que a NAA40 fica bem na saída do túnel onde as novas cadeias proteicas emergem. Ali, ela não age sozinha: liga-se ao lado do complexo associado a polipeptídeos nascente, ou NAC, um ajudante comum ligado ao ribossomo que vigia as novas proteínas conforme saem. Instantâneos estruturais mostraram a NAA40 ancorada ao ribossomo por um segmento helicoidal positivamente carregado em sua extremidade inicial, enquanto o NAC está ligado à superfície ribossomal por uma de suas subunidades. Um domínio flexível do NAC estende-se para contatar a NAA40, efetivamente fazendo uma ponte entre a enzima e o ribossomo.
Por que o NAC é necessário para o ajuste das histonas
Para testar a importância dessa parceria, os pesquisadores reconstituíram essas interações com componentes purificados em tubos de ensaio. Observaram que a NAA40 isolada liga-se apenas fracamente aos ribossomos, mas quando o NAC está presente, a ligação ao ribossomo se torna muito mais forte. Se removeram uma região específica “UBA” do NAC que contacta a NAA40, esse aumento de ligação desapareceu. Em células humanas, a depleção de NAC levou à redução da acetilação dependente de NAA40 da histona H4 e a um aumento correspondente de uma marca rival de fosforilação na mesma cauda de histona. Essa mudança ocorreu sem alterar a quantidade ou a localização da própria NAA40, indicando que o papel principal do NAC é recrutar e posicionar corretamente a NAA40 nos ribossomos em tradução para que as histonas possam ser modificadas de forma eficiente à medida que são produzidas.
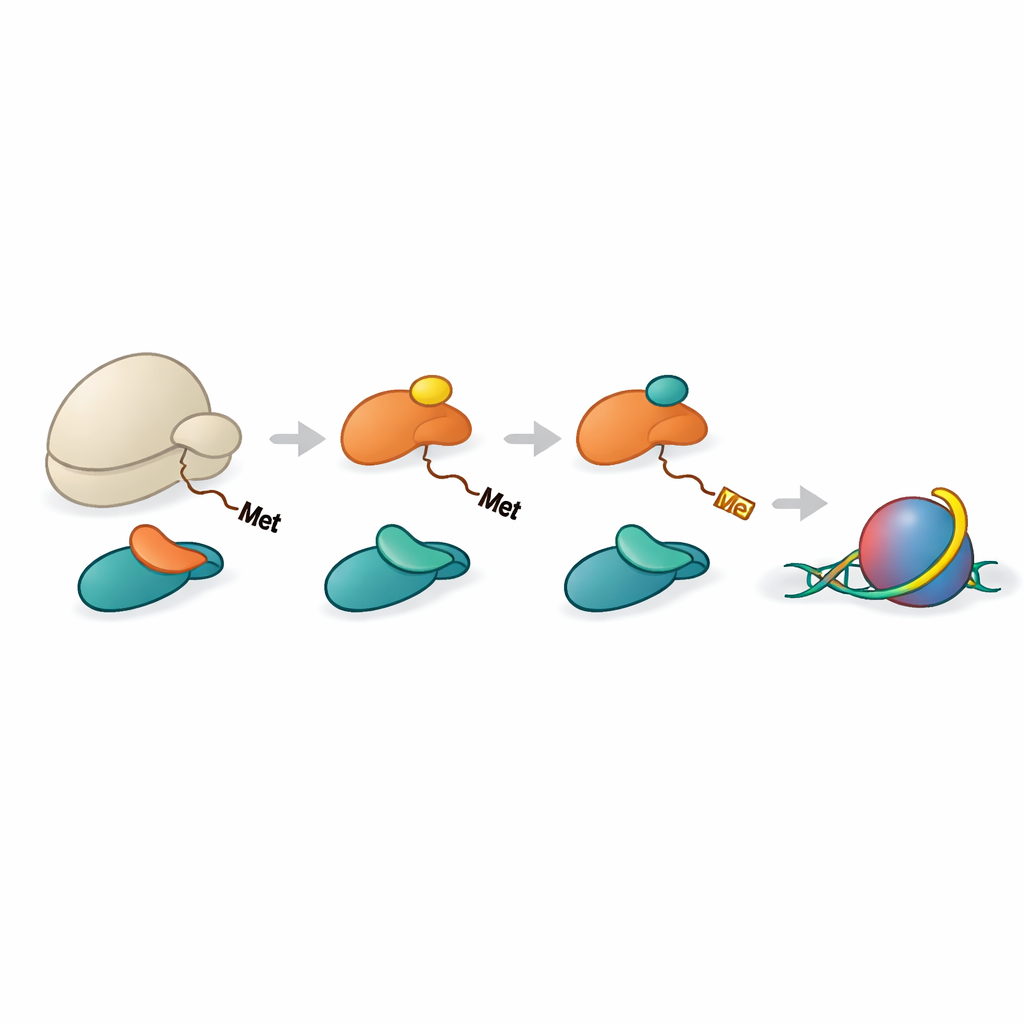
Uma linha de montagem coordenada para o processamento de histonas
As histonas H2A e H4 devem primeiro perder seu aminoácido metionina inicial antes que a NAA40 possa reconhecê‑las. Outra enzima, METAP1, realiza esse corte inicial. A equipe mostrou que o NAC pode ajudar a reunir METAP1 e NAA40 com o ribossomo, formando um complexo multi-enzimático na saída do peptídeo. Estruturas de alta resolução de complexos reconstituídos revelaram METAP1 e NAA40 ligados lado a lado no ribossomo, com seus sítios ativos posicionados a distâncias quase iguais da saída do túnel. Essa geometria significa que, uma vez que a cauda da histona se estenda apenas uma dúzia ou mais de aminoácidos além do ribossomo, o METAP1 pode remover a metionina inicial e a NAA40 pode imediatamente adicionar a capa acetil, minimizando qualquer atraso entre os dois passos.
Implicações para o controle gênico e o câncer
No conjunto, o estudo mostra que a NAA40 não fica simplesmente flutuando pela célula à procura de histonas para modificar. Em vez disso, ela é ancorada ao ribossomo pelo NAC, formando parte de uma estação de processamento organizada que prepara histonas no exato momento em que são sintetizadas. Ao acoplar estreitamente a remoção da metionina e a adição do acetil, a célula garante que as histonas H2A, H4 e a variante H2A.X, ligada a danos no DNA, recebam rapidamente uma marca de acetil que pode moldar a estrutura da cromatina e a expressão gênica. Como perturbações nessa etapa inicial de marcação das histonas podem favorecer o crescimento cancerígeno, entender o arranjo preciso de NAA40, NAC e METAP1 no ribossomo fornece um roteiro estrutural que pode orientar o desenho de fármacos destinados a ajustar esse ponto crítico de controle epigenético.
Citação: Guan, D., Denk, T., Klavaris, A. et al. NAA40 and NAC cooperate in co-translational histone acetylation in humans. Nat Commun 17, 2486 (2026). https://doi.org/10.1038/s41467-026-70279-5
Palavras-chave: acetilação de histonas, NAA40, ribossomo, complexo associado a polipeptídeos nascente, regulação epigenética