Clear Sky Science · pt
Uma transição dependente do ciclo celular de acetilação para fosforilação regula a maturação oportuna do centríolo
Mantendo nossa carga genética no caminho certo
Cada vez que uma célula do nosso corpo se divide, ela precisa distribuir seu DNA com precisão notável. Quando esse processo falha, as células podem ganhar ou perder cromossomos, um estado perigoso associado ao câncer e a outras doenças. Este estudo revela um dispositivo molecular de temporização que ajuda as células a construir as pequenas estruturas necessárias para separar os cromossomos corretamente, expondo uma possível vulnerabilidade que terapias anti‑câncer futuras poderiam explorar.
Os pequenos centros de trânsito da célula
No centro de cada célula em divisão estão os centríolos, estruturas pequenas que funcionam como centros de tráfego para as fibras que puxam os cromossomos. Antes que uma célula entre em divisão, esses centros precisam “maturar”: eles se reforçam com proteínas auxiliares e se tornam organizadores poderosos de microtúbulos, as fibras dinâmicas que formam o fuso de divisão. Se essa maturação acontece cedo demais, tarde demais ou não ocorre, os cromossomos podem ser distribuídos de forma incorreta, levando a células com números cromossômicos anormais. Entender como as células ativam os centríolos no momento certo tem sido uma questão de longa data na biologia celular.
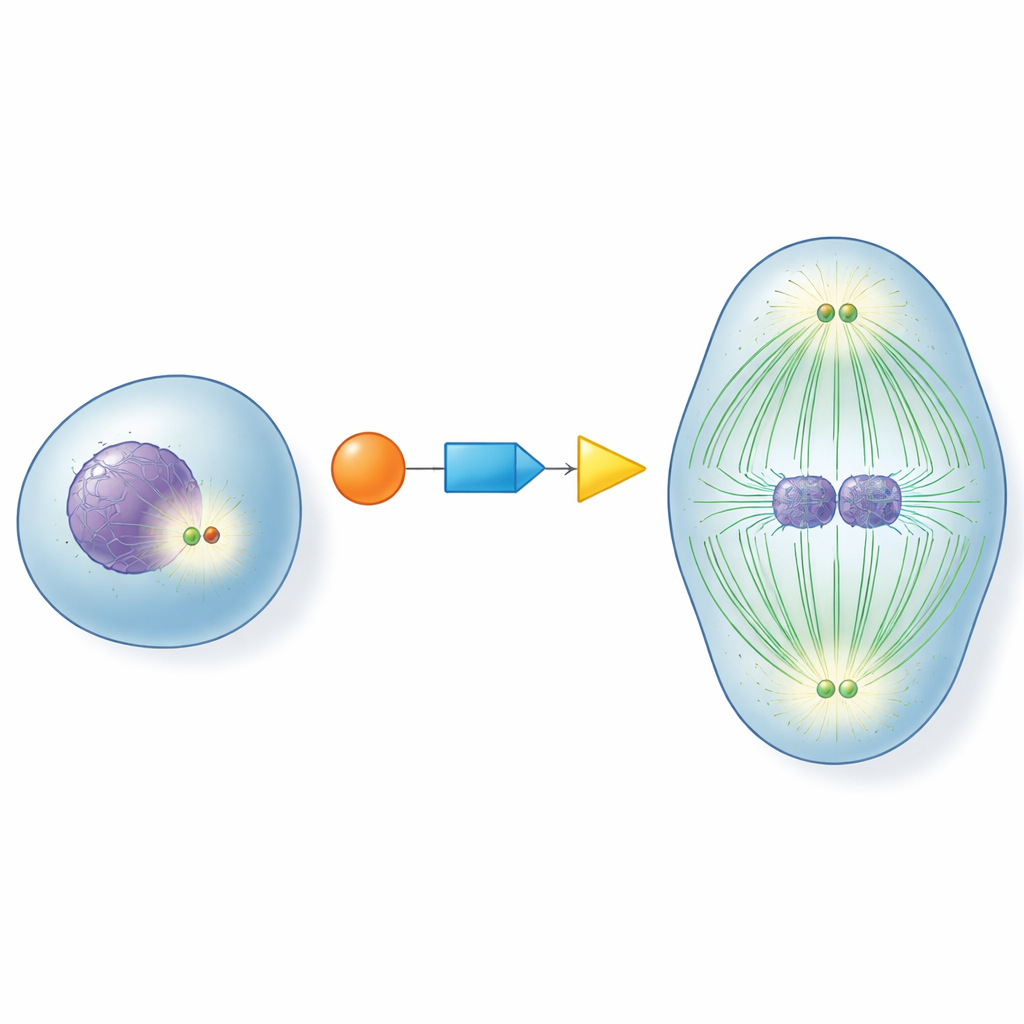
Um revezamento molecular para temporização perfeita
Os autores focaram em três proteínas-chave que atuam juntas como um revezamento: CDK1, um controlador mestre do ciclo celular; RNF40, previamente conhecido principalmente por modificar proteínas que embalam o DNA; e PLK1, um grande motor da divisão celular. Eles descobriram que o RNF40 está fisicamente presente nos centríolos ao longo do ciclo celular e se liga diretamente ao PLK1. À medida que as células se aproximam da divisão, o CDK1 marca quimicamente o RNF40 em dois pontos específicos, o que por sua vez torna o RNF40 um local de acoplamento melhor para o PLK1. Essa cadeia CDK1–RNF40–PLK1 garante que o PLK1 chegue aos centríolos precisamente durante a fase tardia de preparação para a divisão, desencadeando uma maturação robusta dos centríolos, crescimento de microtúbulos e montagem de um fuso bipolar bem formado.
Um interruptor proteico que muda de forma
Curiosamente, o RNF40 nem sempre aceita essas marcas ativadoras. Nas fases em que a célula não se divide ou está copiando o DNA, o RNF40 carrega uma decoração química diferente — grupos acetil — em duas posições próximas. Essas marcas acetil são adicionadas por uma enzima chamada PCAF e removidas mais tarde por um parceiro desacetilante, o HDAC1. A versão acetilada do RNF40 resiste à modificação pelo CDK1, bloqueando efetivamente a etapa seguinte do revezamento. À medida que as células avançam para o estágio final pré‑divisão, o HDAC1 apaga gradualmente as marcas acetil, permitindo que o CDK1 adicione grupos fosfato em seu lugar. Essa mudança cuidadosamente temporizada de acetilação para fosforilação converte o RNF40 de um estado de “espera” para um estado “ligado”, pronto para recrutar o PLK1 e ativar o centríolo.
O que acontece quando a temporização falha
Para investigar o quão crucial é esse interruptor, os pesquisadores engenhariaram células em que o RNF40 não podia mais ser fosforilado, ou em que era forçado a permanecer em um estado que imita a acetilação. Em ambos os casos, o PLK1 não se acumulou adequadamente nos centríolos. Essas células mostraram crescimento reduzido de microtúbulos a partir dos centríolos, fusos deformados e cromossomos desalinhados. Muitas apresentaram cromossomos extras ou faltantes — uma condição anormal conhecida como aneuploidia — e algumas tornaram‑se binucleadas, sinais de erros catastróficos na divisão. Em modelos de câncer, células travadas no estado de RNF40 “acetilado” formaram tumores menores em camundongos e foram mais sensíveis a quimioterápicos comuns usados no tratamento do câncer colorretal, sugerindo que perturbar esse interruptor pode retardar o crescimento tumoral.
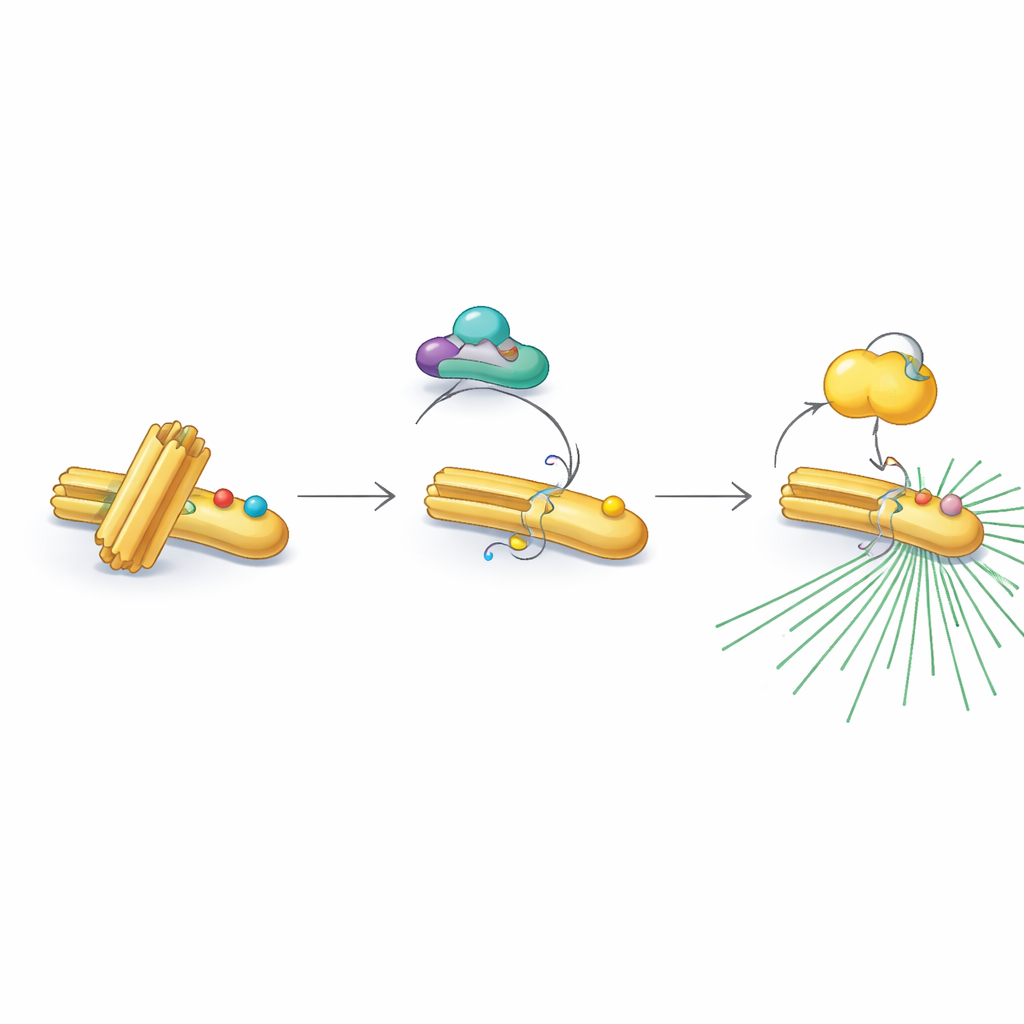
Relações com o câncer humano e possibilidades futuras
O grupo também examinou dados de pacientes e amostras tumorais. Eles descobriram que o RNF40 é frequentemente anormalmente abundante em cânceres colorretais e que certas mutações associadas ao câncer próximas aos seus locais de modificação perturbam sua fosforilação, comprometendo a função adequada dos centríolos. Essas observações conectam o mecanismo de temporização recém‑descrito diretamente à doença humana. Ao identificar uma proteína específica que coordena quando os centríolos amadurecem e como os cromossomos são separados, o estudo destaca um “nó” de sinalização que poderia ser alvo para forçar células tumorais que se dividem rapidamente a cometer erros letais na divisão, ao mesmo tempo que afeta menos as células saudáveis.
Uma nova alavanca para uma divisão celular fiel
Para não especialistas, a mensagem chave é que as células dependem de um interruptor químico finamente ajustado em uma única proteína, o RNF40, para decidir exatamente quando ativar a maquinaria que separa os cromossomos. Essa transição de acetilação para fosforilação comporta‑se como um semáforo em um cruzamento movimentado, ficando verde somente quando a célula está realmente pronta para dividir. Quando o semáforo falha, as células tropeçam na divisão, acumulam erros genéticos e podem tornar‑se cancerosas. Entender e controlar esse interruptor pode abrir novos caminhos para tratamentos que desestabilizem seletivamente células cancerosas ao sabotar sua capacidade de se dividir corretamente.
Citação: Li, J., Liang, J., Chen, G. et al. A cell cycle-dependent transition of acetylation to phosphorylation regulates timely centrosome maturation. Nat Commun 17, 2583 (2026). https://doi.org/10.1038/s41467-026-70271-z
Palavras-chave: maturação do centríolo, divisão celular, instabilidade cromossômica, sinalização PLK1, câncer colorretal