Clear Sky Science · pt
Restaurar a desregulação sináptica pós-natal precoce resgata a degeneração de neurônios motores em um modelo murino da Atrofia Espinobulbar
Por que pequenas alterações precoces podem importar para fraqueza muscular tardia
A atrofia espinobulbar (SBMA) é uma condição hereditária rara em que adultos, geralmente homens, perdem gradualmente força nos membros, no tronco e na garganta. Os sintomas surgem na meia-idade, mas problemas sutis começam muito antes. Este estudo faz uma pergunta surpreendente: eventos breves nos primeiros dias após o nascimento poderiam, silenciosamente, preparar o terreno para a perda de células nervosas décadas depois — e corrigir essas falhas iniciais poderia proteger o movimento?
Uma doença enraizada em um interruptor sensível a hormônios
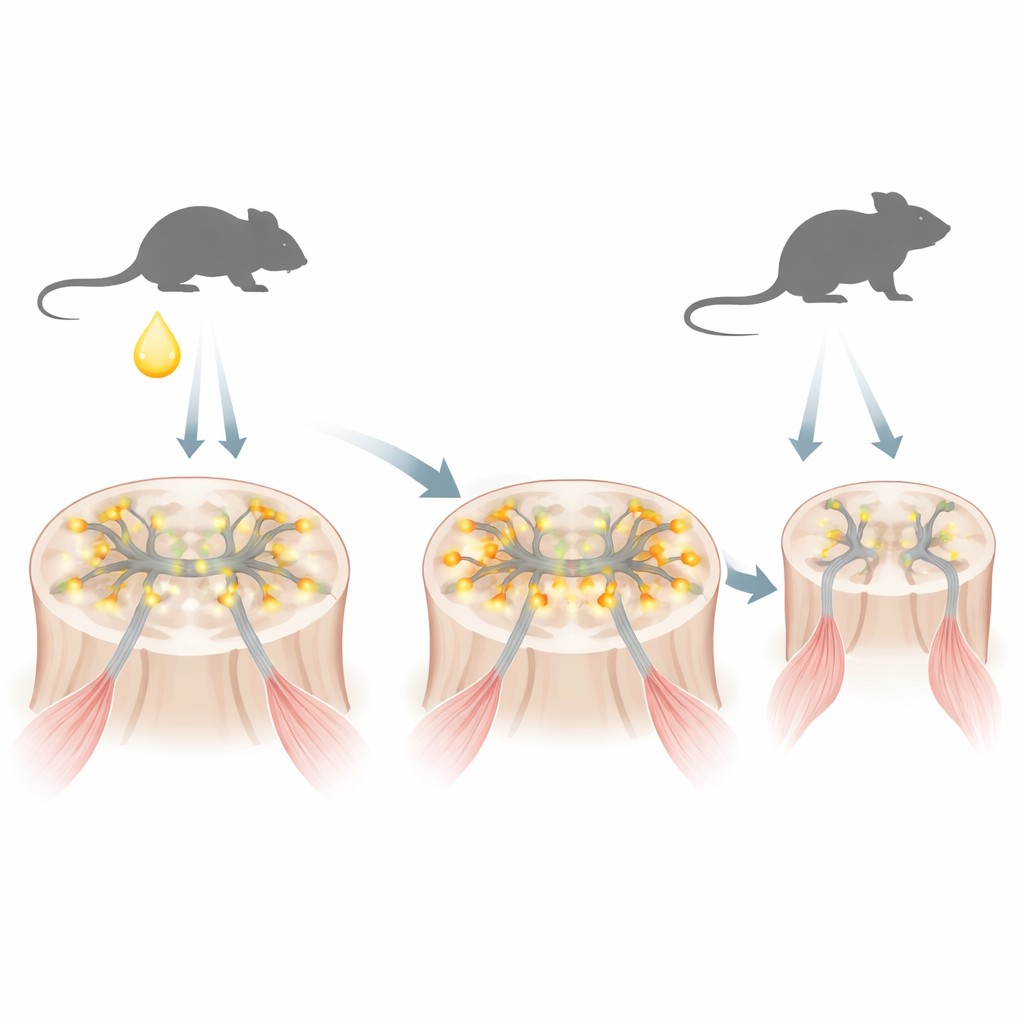
A SBMA é causada por uma versão alterada do receptor de andrógeno, uma proteína que detecta hormônios masculinos como a testosterona. O receptor alterado carrega um alongamento excessivo do aminoácido glutamina. Em um modelo murino que imita a doença humana, os autores descobriram que logo após o nascimento, quando a testosterona sobe brevemente em machos neonatos, esse receptor mutante acumula-se rapidamente dentro dos núcleos dos neurônios motores — as células nervosas que controlam os músculos. Nessa fase inicial a proteína ainda não se aglomerou nos grandes agregados tipicamente ligados à neurodegeneração, mas já está mudando quais genes são ativados ou silenciados.
Excesso sináptico precoce e neurônios motores inquietos
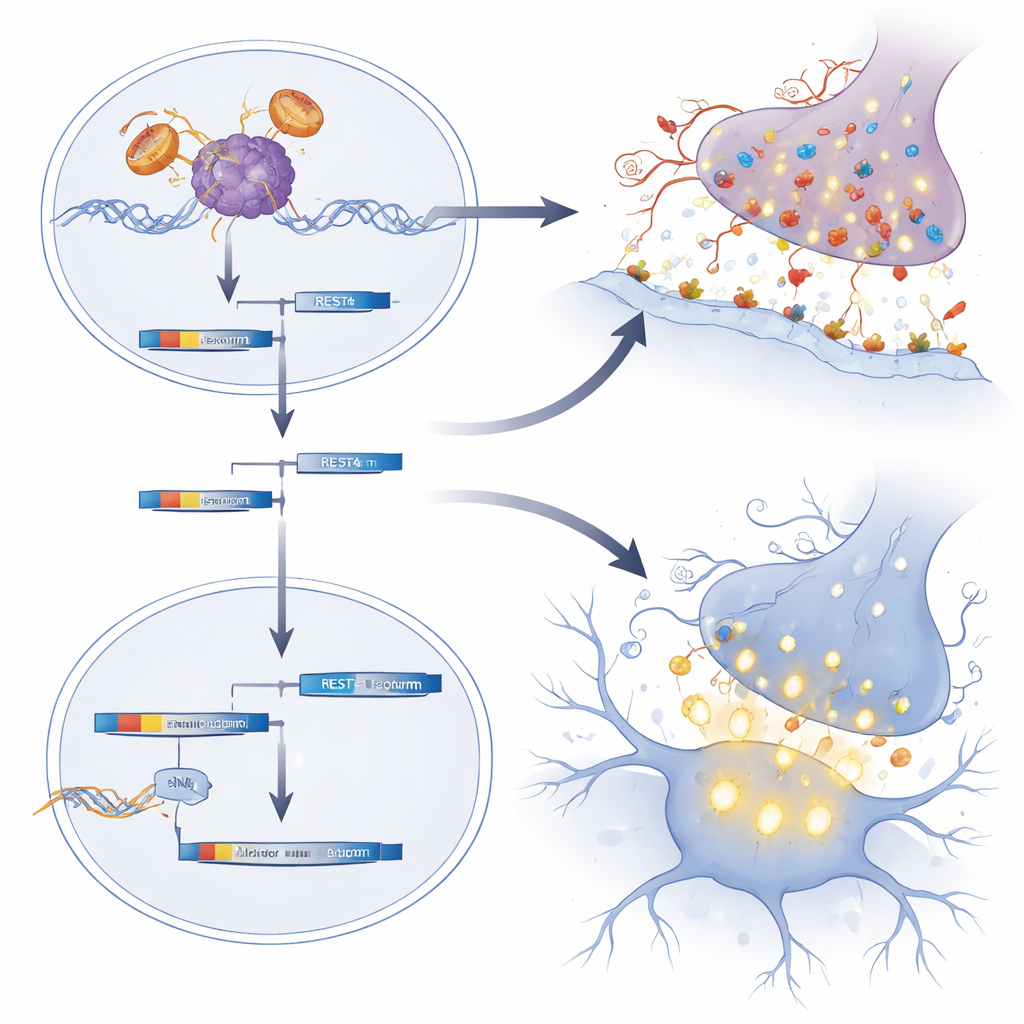
Usando sequenciamento de RNA em escala genômica de medulas espinhais de camundongos recém-nascidos, a equipe descobriu que muitos genes envolvidos em sinapses excitatórias — os pontos de contato onde células nervosas se comunicam — estavam incomumente ativos. Muitos desses genes codificam receptores de glutamato, que tornam os neurônios mais propensos a disparar. O grupo rastreou esse padrão até a perturbação de REST, uma proteína mestre “freio” que normalmente mantém esses genes sinápticos sob controle rígido durante o desenvolvimento. Em camundongos com SBMA e em neurônios motores derivados de células-tronco pluripotentes induzidas de pacientes, a atividade de REST estava enfraquecida e uma forma encurtada chamada REST4 era favorecida, levantando o freio e aumentando os genes de sinapses glutamatérgicas. Em consonância com isso, neurônios motores neonatais com SBMA mostraram níveis mais altos de c-Fos, um marcador de disparo recente, e neurônios motores derivados de pacientes humanos exibiram rajadas de cálcio mais fortes e mais frequentes, características de hiperexcitabilidade.
Tratamento breve precoce que altera o curso vitalício
Os pesquisadores então perguntaram se reduzir o receptor mutante ou restaurar o freio REST apenas durante essa janela neonatal poderia alterar o curso da doença a longo prazo. Eles administraram oligonucleotídeos antisenso — curtas fitas de material genético modificado — no líquido que envolve o cérebro e a medula espinhal de camundongos SBMA com um dia de vida. Um tipo de oligonucleotídeo reduziu temporariamente tanto o receptor de andrógeno mutante quanto o normal no sistema nervoso central. Um segundo tipo deslocou o splicing de REST para longe de REST4 e de volta à REST de comprimento completo, reprimindo assim genes sinápticos. Notavelmente, embora esses tratamentos fossem administrados apenas uma vez e seus efeitos moleculares diretos tenham desaparecido dentro de algumas semanas, os camundongos viveram mais, caminharam melhor em um eixo rotatório e mantiveram uma pegada mais forte no decorrer da vida. Seus neurônios motores e fibras musculares estavam menos atrofiados, e marcadores precoces de hiperatividade neuronal e picos posteriores de neuropeptídeos relacionados ao estresse foram atenuados.
Como hormônios precoces e ajuste gênico moldam a vulnerabilidade
O trabalho também ressalta a vulnerabilidade especial dos neurônios motores ao breve surto de testosterona que ocorre logo após o nascimento. Quando camundongos SBMA recém-nascidos receberam testosterona extra, sua fraqueza e perda de peso posteriores pioraram, e programas gênicos ligados à maturação saudável dos neurônios motores foram ainda mais perturbados. Camundongos normais não apresentaram esse dano, enfatizando que é a combinação do receptor mutante com o surto hormonal que é prejudicial. Juntos, os achados sugerem que na SBMA, excesso de sinapses excitatórias e neurônios motores excessivamente excitáveis no início da vida direcionam lentamente o sistema à falência, mesmo que sintomas óbvios não surjam até a meia-idade.
O que isso significa para pessoas que vivem com SBMA
Para um leitor não especialista, a mensagem principal é que a SBMA pode ser, em parte, uma doença de sinapses fora de hora e mal conectadas durante os primeiros dias após o nascimento. Um sensor hormonal defeituoso empurra neurônios motores em desenvolvimento para um estado de hiperexcitação, e esse estresse inicial contribui eventualmente para sua degeneração anos depois. A notícia encorajadora é que medicamentos genéticos cuidadosamente projetados, administrados durante essas janelas críticas, podem restabelecer o equilíbrio de sinais nos neurônios motores, acalmar sua hiperatividade e retardar ou reduzir de forma significativa a perda posterior de células nervosas em animais. Embora a tradução de tais intervenções na vida precoce para humanos exija grande cuidado e estudos adicionais, esses resultados apontam para novas estratégias que atacam as raízes da SBMA muito antes que a fraqueza apareça.
Citação: Hirunagi, T., Sahashi, K., Iida, M. et al. Restoring early postnatal synaptic dysregulation rescues motor neuron degeneration in a mouse model of Spinal and Bulbar Muscular Atrophy. Nat Commun 17, 2412 (2026). https://doi.org/10.1038/s41467-026-70244-2
Palavras-chave: atrofia espinobulbar, hiperexcitabilidade do neurônio motor, receptor de andrógeno, regulação sináptica REST, terapia com oligonucleotídeo antisenso