Clear Sky Science · pt
Seleção de caminhos entre reações de clique e transferência de acila impulsionadas por aminoacil fosfatos
Por que o tempo importa na química do dia a dia
Dentro de cada célula, moléculas importantes são construídas e modificadas em uma ordem muito precisa, como etapas de uma receita. Esse tempo decide se uma proteína é ativada, desativada ou até mesmo altera sua conformação. Químicos gostariam de imitar esse tipo de cronograma embutido usando moléculas simples, não vivas, em água, sem depender de enzimas ou gatilhos externos como luz ou variações de pH. Este artigo descreve um sistema reacional artificial que faz exatamente isso: utiliza a estrutura de pequenos peptídeos e uma reação formadora de ligações popular da “química click” para decidir qual etapa química acontece primeiro e qual precisa esperar sua vez.
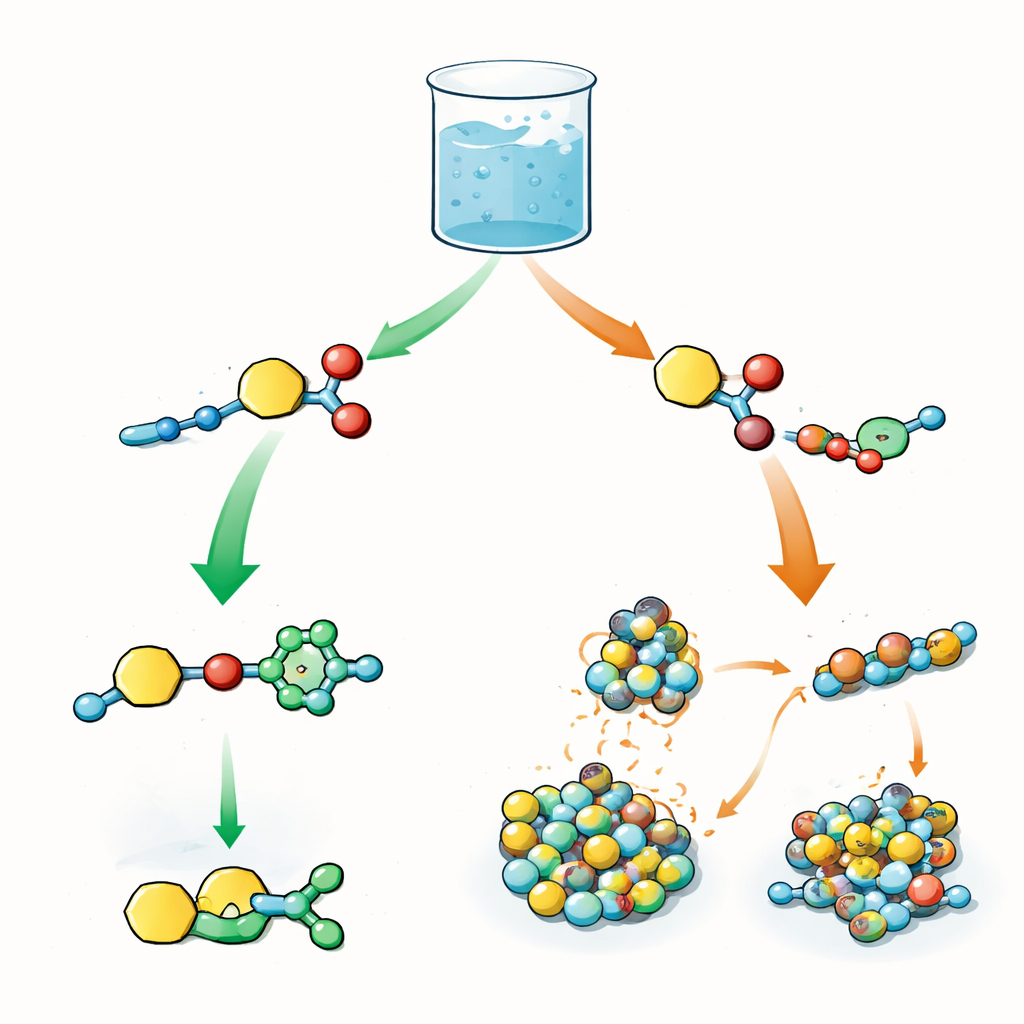
Dupla de reações rivais em um mesmo frasco
Os autores projetam um bloco de construção central que carrega duas características reativas: uma capaz de transferir um grupo “acila” (um fragmento químico pequeno frequentemente usado para modificar proteínas) e outra que pode passar por uma reação click chamada cicloadição azida‑alquino catalisada por cobre. No mesmo béquer, esse bloco de construção é misturado com azidas e com peptídeos curtos que atuam como nucleófilos, ou seja, capturam o grupo acila. Na biologia, a ordem de etapas como ativação, transferência e modificações posteriores controla o comportamento das proteínas. Aqui, a questão é semelhante: quando ambas as reações são possíveis ao mesmo tempo, o sistema escolhe primeiro a reação click, a transferência de acila, ou alguma mistura de ambas?
Oxigênio lento, enxofre rápido
A equipe primeiro estuda peptídeos contendo tirosina, um aminoácido com cadeia lateral baseada em oxigênio. Em condições levemente básicas, a reação click dispara à frente: o alcino e a azida se unem rapidamente, enquanto a transferência de acila para a cadeia lateral da tirosina é lenta e mal forma intermediários detectáveis. Vários produtos derivados do click coexistem, e há pouca lacuna de tempo clara entre as etapas. Quando os pesquisadores mudam para cisteína, um aminoácido com cadeia lateral de enxofre, a história se inverte. A cisteína forma rapidamente tioésteres—produtos de acilação ligados ao enxofre—que aparecem em alto rendimento muito antes de quaisquer produtos de click. Só depois de muitas horas os produtos de click começam a emergir. Essa mudança ocorre porque o enxofre não só reage mais prontamente, como também se liga aos íons de cobre, sequestrando o catalisador e “pausando” temporariamente a via do click.
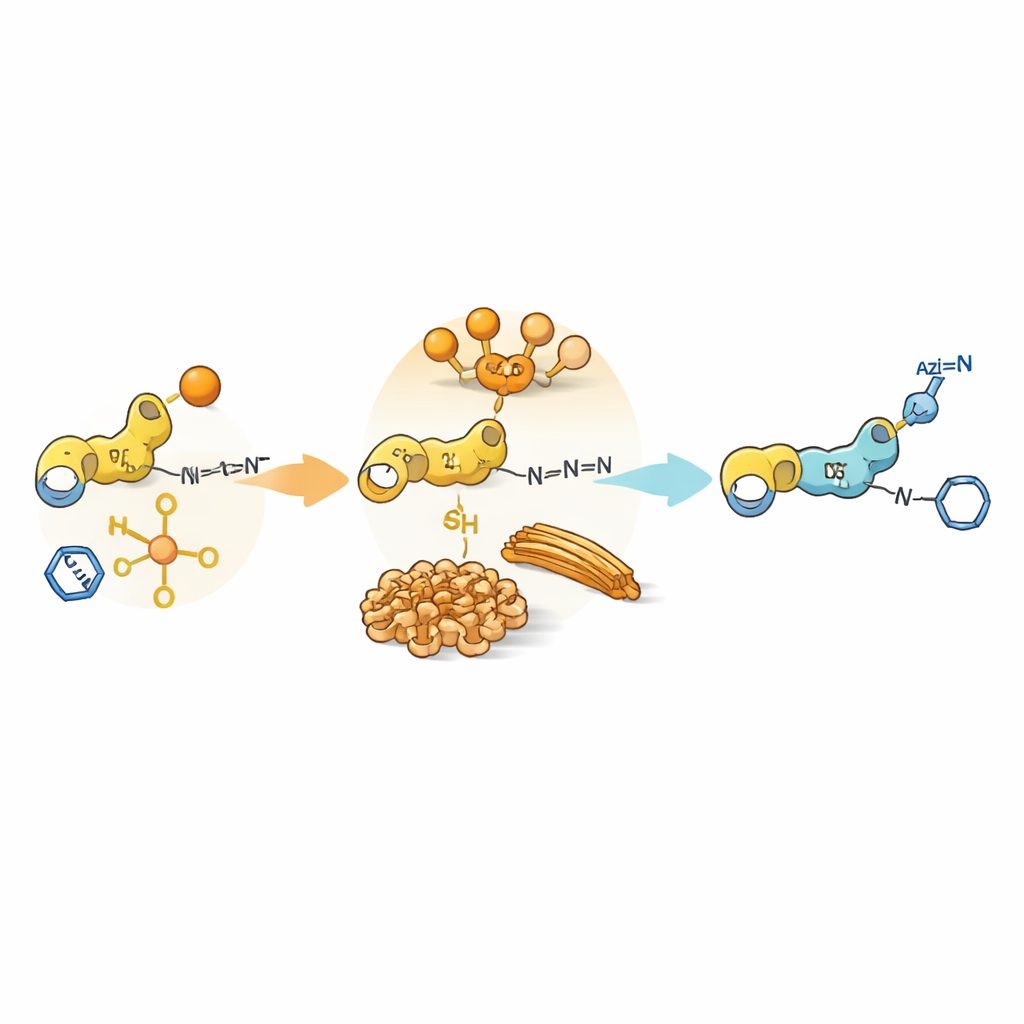
Auto‑organização como um portão químico
Além da reatividade simples, os próprios peptídeos podem se aglomerar em estruturas maiores, formando géis macios ou fibras em água. Essas montagens criam domínios minúsculos onde alguns parceiros ficam concentrados e outros são excluídos. Para certos dipeptídeos contendo tirosina ou cisteína que carregam grupos aromáticos extras, os intermediários se auto‑organizam em fibrilas ou partículas densas. Nessas regiões compactas, a transferência de acila é favorecida porque nucleófilo e doador de acila ficam lado a lado, enquanto a azida e o catalisador de cobre permanecem principalmente na solução circundante. Como resultado, embora a reação click seja intrinsecamente rápida em solução livre, ela é retardada pela necessidade de alcançar sítios reativos enterrados. Essa “mismatch de fase” entre onde o catalisador vive e onde os substratos estão localizados amplia a vida útil dos intermediários acilados e atrasa o início da química click.
Programando cascatas e escolhas
Para testar até onde podem levar esse agendamento embutido, os autores projetam situações mais complexas. Em um caso, um único peptídeo contém tanto cisteína quanto tirosina, oferecendo dois sítios diferentes de transferência de acila. A reação prossegue como uma cascata de três etapas: primeiro forma‑se um tioéster na cisteína, depois um segundo grupo acila movimenta‑se para a tirosina, e somente após essas etapas surgem os produtos de click. Em outro conjunto de experimentos, duas azidas diferentes—uma flexível e alifática, a outra rígida e aromática—competem pelo mesmo centro reativo. Surpreendentemente, o sistema prefere consistentemente a azida alifática, revelando que até a forma e o caráter eletrônico da azida podem enviesar quais produtos dominam, enquanto o tempo de transferência de acila permanece sob controle do peptídeo.
O que isso significa para materiais inteligentes no futuro
Em linguagem cotidiana, este trabalho mostra como é possível juntar múltiplas reações potencialmente concorrentes na mesma mistura aquosa simples e ainda fazê‑las ocorrer em uma ordem definida—sem enzimas, bombas ou interruptores externos. Ao escolher se um peptídeo carrega oxigênio ou enxofre, ao ajustar sua tendência a auto‑organizar‑se e ao modificar a natureza do parceiro azida, os autores codificam uma espécie de relógio interno em uma pequena rede química. Transferências de acila iniciais e reversíveis criam intermediários de curta duração que moldam quando e como a etapa robusta e quase irreversível do click ocorre. Sequências programadas assim podem tornar‑se a base para materiais inteligentes e redes reacionais sintéticas que “decidem” seus próprios caminhos ao longo do tempo, assim como a química cuidadosamente temporizada em ação nas células vivas.
Citação: Bhattacharjee, D., Sharma, A., Dai, K. et al. Pathway selection between click and acyl transfer reactions driven by aminoacyl phosphates. Nat Commun 17, 2407 (2026). https://doi.org/10.1038/s41467-026-70199-4
Palavras-chave: química click, transferência de acila, montagem supramolecular, redes de reação, química de peptídeos