Clear Sky Science · pt
Mapeamento molecular em DNA-PAINT via Modelagem de Mistura Gaussiana modificada
Vendo o mundo invisível das moléculas
A biologia moderna depende cada vez mais de microscópios capazes de enxergar não apenas células, mas moléculas individuais dentro delas. Ainda assim, transformar a luz fraca e piscante emitida por essas moléculas em um “mapa” confiável de onde cada uma se encontra é surpreendentemente difícil. Este estudo apresenta um novo método computacional, chamado G5M, que torna esses mapas moleculares muito mais precisos e detalhados, ajudando cientistas a entender como proteínas estão organizadas e agrupadas em células reais, até escalas de apenas alguns bilionésimos de metro.
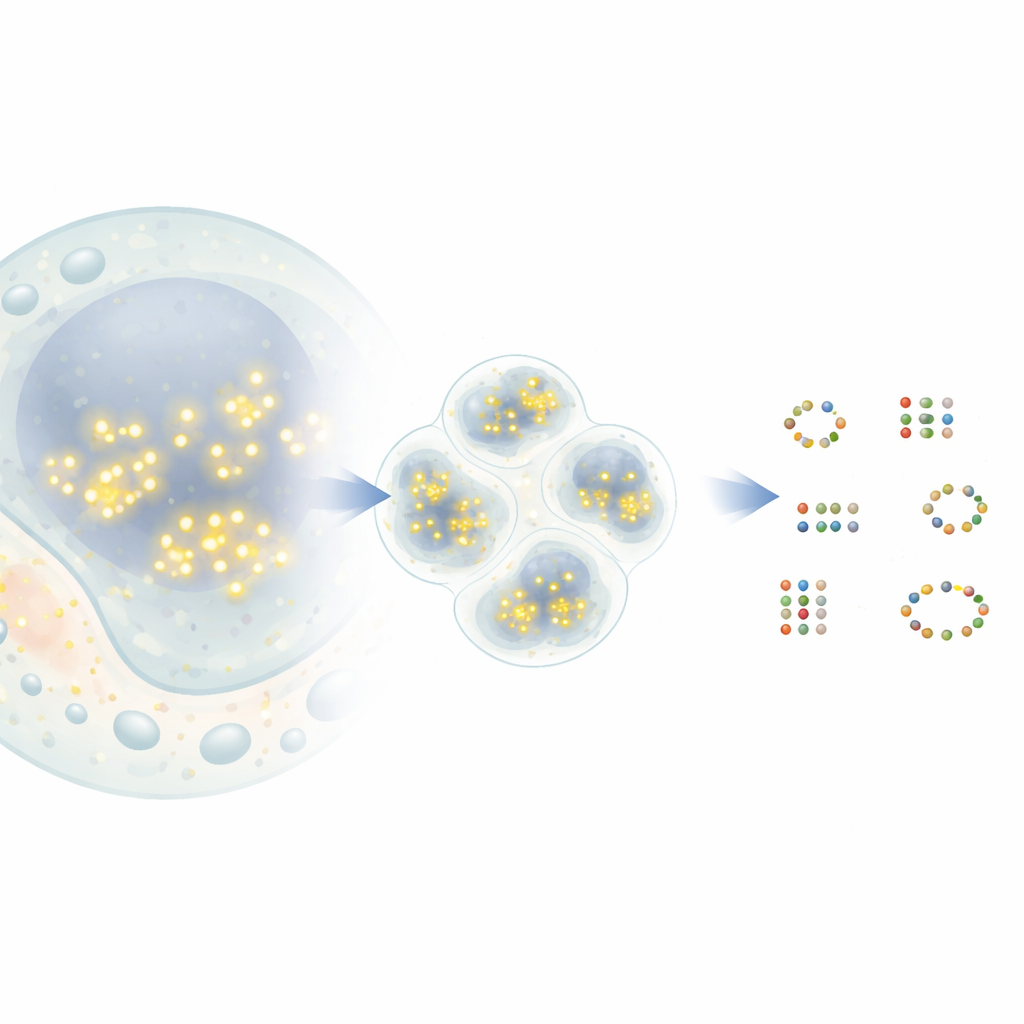
Dos pontos que piscam aos mapas moleculares
Em uma técnica popular de super‑resolução chamada DNA‑PAINT, pequenos trechos de DNA carregando corantes fluorescentes se ligam e desligam brevemente a etiquetas de DNA correspondentes presas às proteínas-alvo. Cada vez que um corante se liga, ele aparece como um ponto brilhante no microscópio antes de desaparecer novamente. Com o tempo, muitos desses eventos criam uma nuvem de pontos ao redor de cada proteína. Em princípio, o centro de cada nuvem marca a posição real de uma proteína com precisão na escala de nanômetros. Na prática, porém, pontos de proteínas vizinhas podem se sobrepor, e alguns pontos vêm de sinais de fundo aleatórios. Ferramentas de análise existentes frequentemente fundem vizinhos próximos em uma única proteína ou, ao contrário, inventam proteínas que não existem, limitando a quantidade de insight biológico que pode ser extraído.
Uma forma mais inteligente de encontrar moléculas reais
O novo método, G5M, trata o enxame de pontos como uma mistura de nuvens simples em forma de sino, cada uma correspondendo a uma molécula real. Em vez de apenas agrupar pontos próximos por densidade, o G5M usa um modelo probabilístico que incorpora o que já se sabe sobre o experimento: quão precisamente as posições podem ser medidas, com que rapidez os fios de DNA se ligam e desligam, e como o microscópio desfoca a luz em duas ou três dimensões. Em seguida, testa diferentes explicações possíveis — diferentes números e formas de nuvens — e escolhe automaticamente aquela que melhor equilibra ajuste e simplicidade. Salvaguardas adicionais rejeitam soluções suspeitas, como nuvens que são muito estreitas, muito largas, baseadas em poucos pontos ou não claramente separadas entre si.
Provando sua eficácia em simulações e nanostruturas de DNA
Para testar o G5M, os autores primeiro usaram simulações computacionais realistas de cenas simples: pares de moléculas e pequenas grades de doze moléculas espaçadas a apenas alguns nanômetros. Em comparação com o método líder atual, conhecido como Gradient Ascent, o G5M encontrou muito mais das moléculas que deveriam ser visíveis no limite teórico de resolução, enquanto quase nunca relatava moléculas que não existiam. Em casos chave, recuperou pares próximos 27 vezes com mais frequência do que o método antigo e melhorou a resolução efetiva em mais da metade. A equipe então confirmou esses ganhos experimentalmente usando estruturas de DNA origami — formas artificiais de DNA com locais de ancoragem colocados em posições precisamente conhecidas — mostrando que o G5M podia contar e localizar de forma confiável quase todos os sítios esperados em uma variedade de condições de imagem.
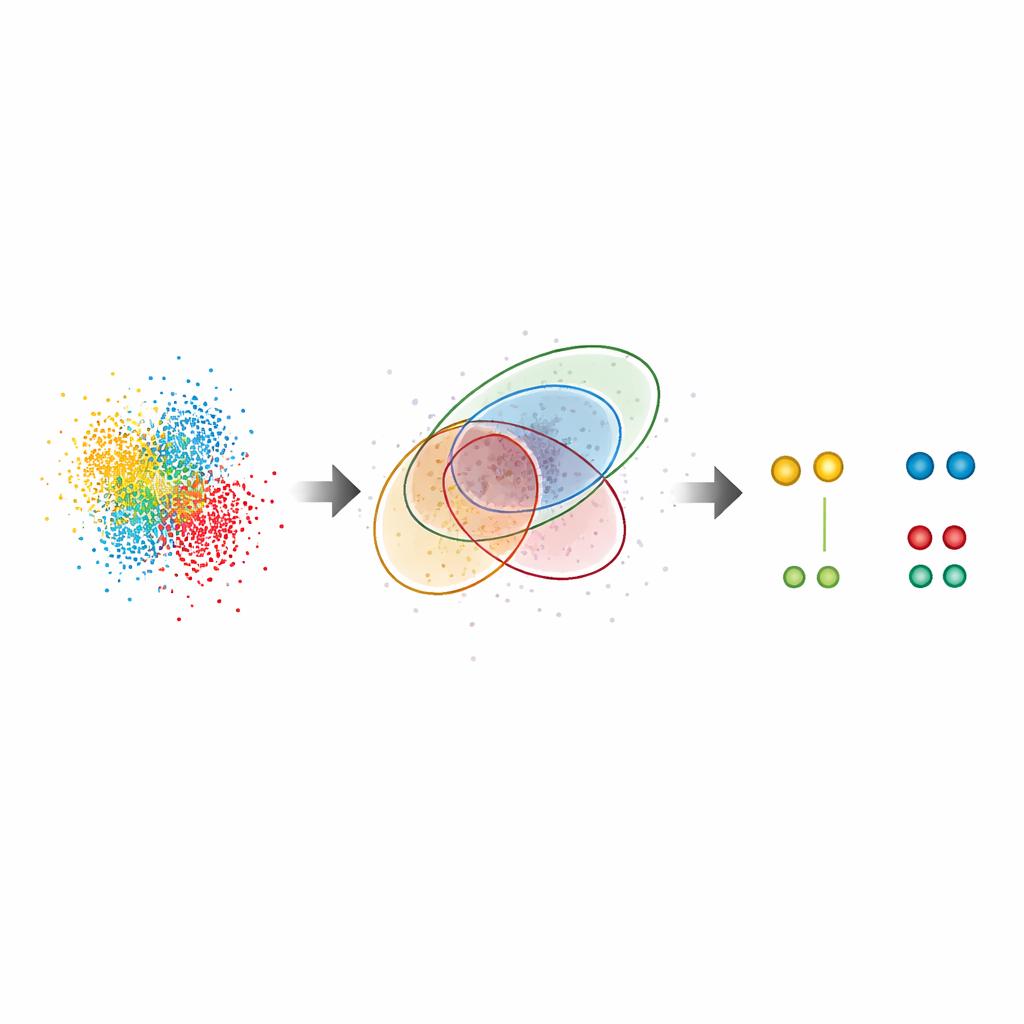
Revelando padrões ocultos em células reais
Além de amostras de teste, o G5M foi aplicado a sistemas biológicos complexos. Em complexos do poro nuclear, grandes portões no núcleo da célula, o método recuperou o arranjo conhecido em anel de uma proteína chave, Nup96, mesmo onde parceiros estavam separados por apenas cerca de dez nanômetros. Encontrou quase o dobro de pares de proteínas do que o método padrão e reproduziu estimativas independentes de eficiência de marcação, sugerindo que não perde muitas moléculas nem adiciona outras espúrias. Os autores também examinaram o CD20, um receptor de superfície envolvido em cânceres sanguíneos e alvo de anticorpos terapêuticos. Nesse caso, o G5M revelou significativamente mais pequenos aglomerados (dímeros, trímeros e tétrameros) de CD20 na membrana celular, esclarecendo como um anticorpo anticâncer e formatos de drogas relacionados reorganizam esses receptores. Ele até aumentou o desempenho de uma abordagem de ultra‑alta resolução chamada RESI, que depende de separar sinais através de múltiplas rodadas de imageamento.
O que isso significa para a microscopia futura
Ao extrair informações mais confiáveis a partir de dados de DNA‑PAINT existentes, o G5M mostra que software melhor por si só pode desbloquear novos detalhes biológicos, sem mudar microscópios ou corantes. O algoritmo mantém detecções falsas extremamente baixas enquanto resolve moléculas que estão quase se tocando, o que é essencial ao perguntar quantas proteínas estão em um complexo, como elas estão espaçadas ou como um medicamento altera seu arranjo. Integrado na plataforma de código aberto Picasso e robusto a configurações típicas, o G5M está posicionado para se tornar uma ferramenta padrão para transformar fluorescência piscante em mapas moleculares confiáveis, ajudando pesquisadores a traçar a organização em escala nanométrica da vida dentro das células.
Citação: Kowalewski, R., Reinhardt, S.C.M., Pachmayr, I. et al. Molecular mapping in DNA-PAINT via modified Gaussian Mixture Modeling. Nat Commun 17, 2315 (2026). https://doi.org/10.1038/s41467-026-70198-5
Palavras-chave: microscopia de super-resolução, DNA-PAINT, mapeamento molecular, oligomerização de proteínas, algoritmos de análise de imagem