Clear Sky Science · pt
Multiômica de célula única revela um eixo mecanossensível endotelial PIEZO1-IL-33 que impulsiona a fibrose pulmonar
Por que pulmões rígidos importam
A fibrose pulmonar é uma condição devastadora em que os alveólos, antes elásticos, gradualmente se transformam em tecido cicatricial rígido, tornando cada respiração um esforço. Atualmente os médicos só conseguem desacelerar a doença, não detê-la ou revertê-la. Este estudo investiga uma questão aparentemente simples, mas de grande alcance: como as células que revestem os vasos sanguíneos do pulmão detectam que o tecido ao redor ficou anormalmente rígido, e como essa sensação se transforma em mais formação de cicatriz? Ao seguir essa cadeia de eventos até células únicas e genes individuais, os pesquisadores descobrem um “interruptor” mecânico nos vasos sanguíneos que pode ser alvo de fármacos.
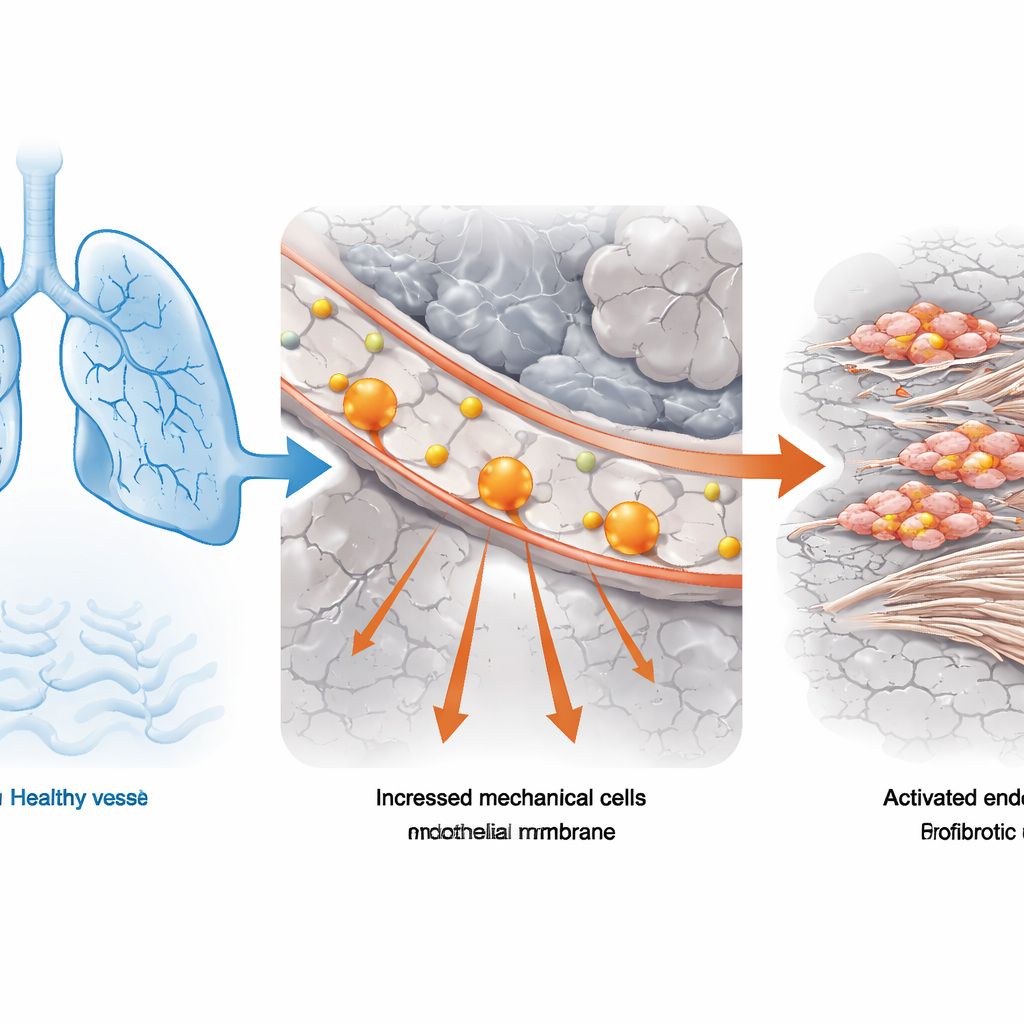
De testes de função pulmonar a células únicas
A equipe começou com tecido pulmonar de pessoas com fibrose pulmonar idiopática, a forma mais comum da doença, e de doadores com pulmões normais. Eles combinaram medições clínicas padrão de função pulmonar (quanto ar a pessoa consegue expirar com força) com sequenciamento de RNA de célula única, uma técnica que revela quais genes estão ativos em milhares de células individuais. Usando uma ferramenta computacional que vincula dados clínicos agregados a perfis de célula única, eles identificaram quais tipos celulares se associavam mais estreitamente à função pulmonar severamente comprometida. As células endoteliais vasculares — as que formam o revestimento interno dos vasos sanguíneos — destacaram‑se por estarem especialmente enriquecidas em pacientes cuja capacidade pulmonar era inferior à metade do normal. Nestas células endoteliais, programas genéticos relacionados ao “estresse mecânico” estavam consistentemente aumentados, sugerindo que forças físicas anormais faziam parte do problema.
Estresse mecânico como um motor oculto
Para testar se essa ligação entre detecção de estresse e doença era geral, os pesquisadores recorreram a dois modelos murinos de cicatrização pulmonar: um desencadeado pela quimioterápica bleomicina e outro por exposição prolongada à sílica, um risco ocupacional. Aplicando métodos de célula única nesses pulmões experimentais, eles novamente encontraram que as células endoteliais exibiam assinaturas claras de estresse mecânico aumentado. Em ambos os modelos, à medida que o tecido pulmonar circundante engrossava e enrijecia, o revestimento dos vasos parecia entrar em um estado mal adaptado. Essa convergência entre amostras humanas e modelos animais reforça a ideia de que forças físicas distorcidas no pulmão, e não apenas inflamação ou atividade imune, são centrais para o desenvolvimento e progressão da fibrose.
Um sensor de pressão com papel crítico
Aprofundando, a equipe procurou por “mecanossensores” específicos — proteínas que convertem alongamento físico em sinais bioquímicos — que estivessem regulados para cima nas células endoteliais sob estresse. Uma proteína de canal, chamada PIEZO1, emergiu repetidamente como suspeita principal. Em ratos e humanos com fibrose, os níveis de PIEZO1 eram marcadamente maiores nas células endoteliais vasculares do que em controles saudáveis. Quando os pesquisadores geraram camundongos nos quais o PIEZO1 foi deletado apenas no endotélio, esses animais mostraram muita resistência à cicatrização pulmonar induzida por bleomicina: apresentaram menos acúmulo de colágeno, menos células ativadas formadoras de cicatriz e níveis reduzidos de um marcador químico de fibrose. Bloquear farmacologicamente o PIEZO1 com um peptídeo inibidor também aliviou a cicatrização, enquanto ativá‑lo agravou a fibrose — a menos que o receptor estivesse ausente nas células endoteliais. Em conjunto, esses experimentos demonstraram que o PIEZO1 nas células que revestem os vasos não é um mero espectador, mas um motor necessário da doença.
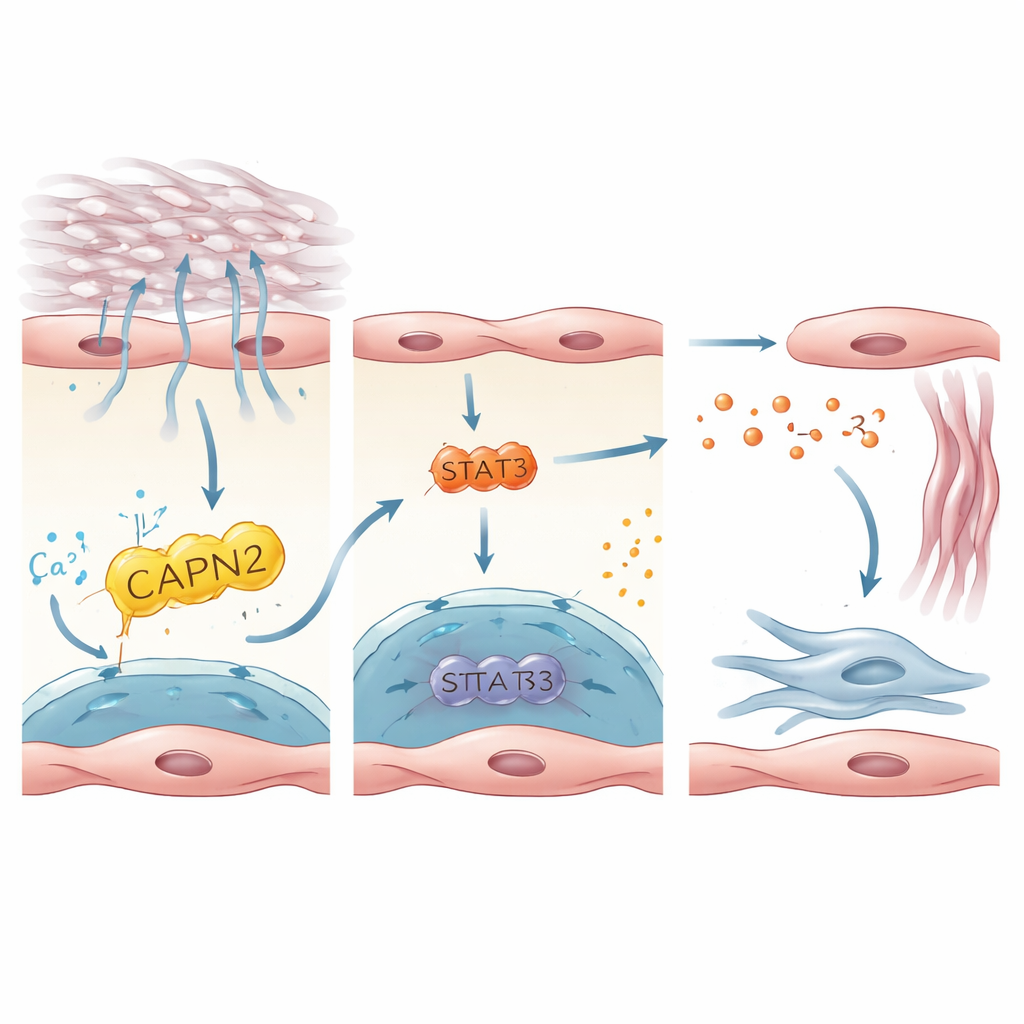
Uma cadeia de sinalização que desperta as células formadoras de cicatriz
O estudo então mapeou como a ativação do PIEZO1 dentro das células endoteliais é traduzida em sinais que despertam os fibroblastos, as células que depositam tecido cicatricial. Ao integrar conjuntos de dados humanos e de camundongos, os autores focalizaram a interleucina‑33 (IL‑33), uma pequena proteína liberada por células estressadas ou danificadas, como mensageira chave. A IL‑33 foi fortemente expressa em células endoteliais positivas para PIEZO1 e elevada em pulmões de pacientes e camundongos com fibrose. Em células endoteliais humanas cultivadas em substratos rígidos ou esticadas para imitar a respiração contra um pulmão rígido, a ativação do PIEZO1 aumentou a produção de IL‑33. Isso dependia de uma enzima a jusante, CAPN2, e de um fator de transcrição, STAT3, que juntos ajustavam a atividade do gene IL‑33. Em camundongos, deletar a IL‑33 especificamente nas células endoteliais protegeu contra a fibrose, enquanto forçar a superprodução de IL‑33 pelas células endoteliais anulou o efeito protetor da perda do PIEZO1. Esses resultados delineiam um eixo linear: estresse mecânico → PIEZO1 → CAPN2/STAT3 → IL‑33 → ativação de fibroblastos e formação de cicatriz.
O que isso significa para tratamentos futuros
Para não especialistas, a mensagem é que a fibrose pulmonar não é movida apenas por células imunes descontroladas; é também uma doença de “toque” defeituoso nos vasos sanguíneos. As células endoteliais percebem que seu entorno se tornou rígido demais, acionam o interruptor PIEZO1 e, em resposta, liberam IL‑33, um sinal de perigo que estimula os fibroblastos vizinhos a continuar depositando cicatriz. Ao dissecar essa cadeia desde a força mecânica até a expressão gênica, o trabalho destaca vários alvos promissores — o próprio PIEZO1, o sistema CAPN2‑STAT3 e a IL‑33 — para terapias que visem interromper o ciclo autorreforçador de rigidez e cicatrização. Embora sejam necessários mais estudos para modular com segurança essas vias em humanos, esse eixo endotelial mecanossensível oferece um novo ângulo, ancorado na fisiologia física, para enfrentar uma doença que há muito resiste a tratamentos eficazes.
Citação: Zhang, L., Gui, X., Hou, R. et al. Single-cell multiomics uncovers an endothelial mechanosensitive PIEZO1-IL-33 axis driving pulmonary fibrosis. Nat Commun 17, 2655 (2026). https://doi.org/10.1038/s41467-026-70193-w
Palavras-chave: fibrose pulmonar, células endoteliais, mecanotransdução, PIEZO1, IL-33