Clear Sky Science · pt
Adaptações na tubulina de Plasmodium determinam arquiteturas, mecânica e suscetibilidade a drogas distintas dos microtúbulos
Por que o esqueleto da malária importa
Os parasitas da malária sobrevivem dentro das células sanguíneas humanas, mas também precisam se espremer através de mosquitos e de diferentes tecidos. Para isso, dependem de um andaime interno composto por tubos microscópicos chamados microtúbulos. Este estudo faz uma pergunta simples, porém poderosa: como os microtúbulos do parasita podem ser tão especializados e resistentes quando seus blocos básicos parecem tão semelhantes aos das nossas próprias células? A resposta revela não apenas como o parasita mantém sua forma, mas também como poderíamos projetar drogas que ataquem seu esqueleto sem prejudicar o nosso. 
Os tubos minúsculos que moldam um parasita mortal
Microtúbulos são tubos proteicos ocos que ajudam as células a se dividir, mover e manter sua forma. Eles são construídos a partir de unidades proteicas pareadas chamadas tubulina. Em animais, plantas e parasitas, a tubulina é surpreendentemente similar, o que dificulta explicar por que os microtúbulos podem parecer e comportar-se de forma tão diferente entre organismos. No parasita da malária Plasmodium falciparum, os microtúbulos formam arranjos diversos: alguns são dinâmicos e auxiliam durante a divisão celular, enquanto outros são suportes longos e rígidos sob a membrana externa do parasita. Como essas estruturas são essenciais para o crescimento e a transmissão do parasita, elas são alvos atraentes para fármacos antimaláricos — especialmente com a crescente resistência aos tratamentos atuais.
Vendo a tubulina do parasita em detalhe atômico
Os pesquisadores purificaram tubulina diretamente de parasitas de P. falciparum e usaram crio-microscopia eletrônica de alta resolução para ver como ela se monta em microtúbulos. Compararam essas estruturas com os microtúbulos bem estudados do cérebro de mamífero. À primeira vista, a tubulina do parasita parece quase idêntica à versão humana e adota o mesmo dobramento geral. Mas uma comparação cuidadosa revelou aglomerados de pequenas mudanças de sequência em torno de bolsões-chave onde moléculas portadoras de energia (GTP e GDP) se ligam e onde certos fármacos interagem. Esses deslocamentos sutis alteram o posicionamento de hélices e laços próximos, especialmente na superfície do dímero de tubulina onde outras proteínas e drogas se prendem. O trabalho sugere que, embora o projeto geral seja conservado, ajustes locais no parasita remodelam levemente esses sítios importantes.
Tubos mais rígidos por ligações laterais mais fortes
Microtúbulos são polímeros: muitos dímeros de tubulina empilham-se extremidade a extremidade em protofilamentos, e vários protofilamentos alinham-se lado a lado para formar a parede do tubo. A equipe descobriu que, nos microtúbulos do parasita, os contatos longitudinais ao longo de cada protofilamento são muito semelhantes aos dos microtúbulos cerebrais. A diferença aparece nos contatos laterais, entre protofilamentos vizinhos. Embora a área de contato seja na verdade um pouco menor no parasita, simulações revelam que essas conexões laterais são coletivamente mais fortes, tornando a rede mais rígida. Modelagem computacional de fragmentos da parede do microtúbulo mostrou que a tubulina do parasita se dobra e torce menos que a tubulina cerebral. Tomografia eletrônica de extremidades reais de microtúbulos confirmou que os microtúbulos do parasita têm pontas de protofilamento mais curtas e menos abertas, um sinal de um tubo mais resistente. 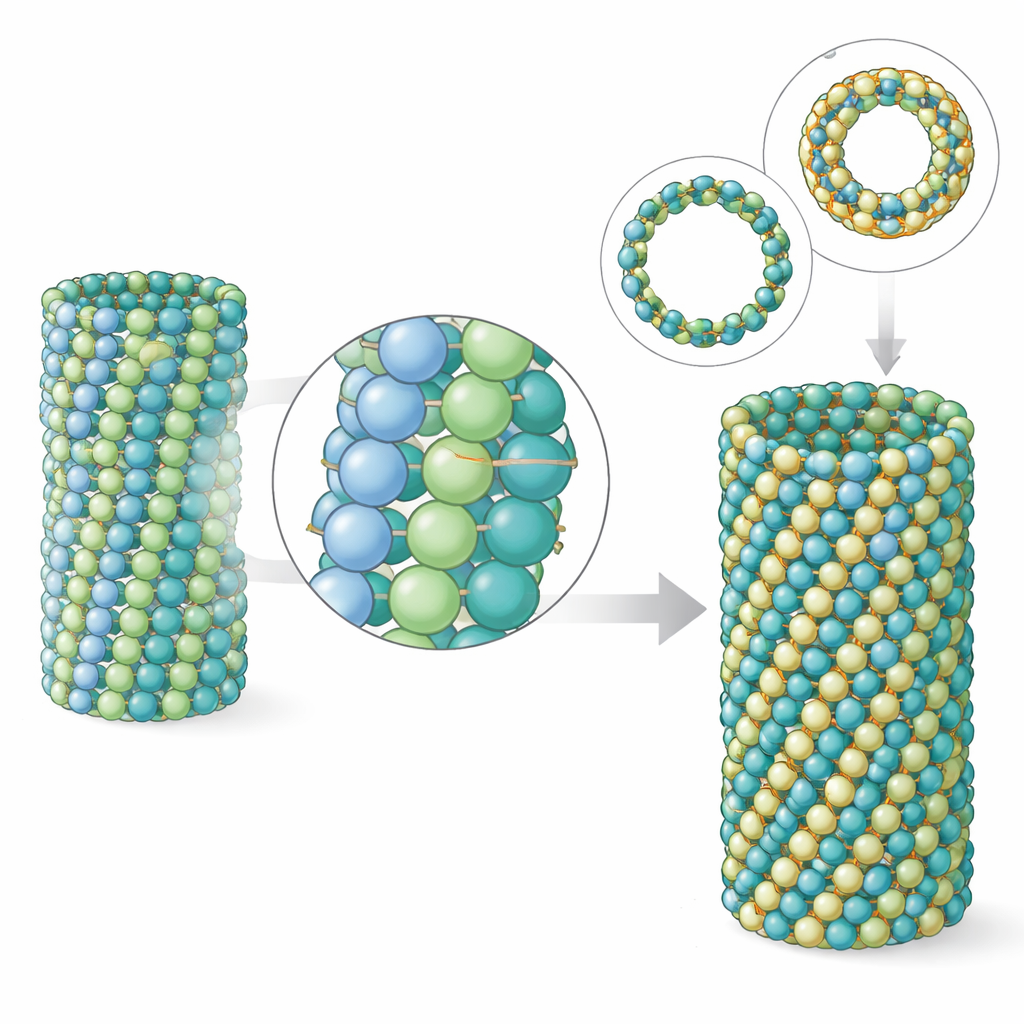
Tamanhos de tubo incomuns que combinam com a ação do parasita
Outra característica marcante de P. falciparum é que, em alguns estádios de vida, seus microtúbulos contêm mais blocos ao redor da circunferência do que as usuais 13 fileiras encontradas na maioria das células animais — frequentemente 15 ou até 17 protofilamentos. A equipe recriou esse comportamento em tubo de ensaio alterando o nucleótido usado durante a montagem. Com uma molécula semelhante ao GTP que estabiliza o estado de crescimento, a tubulina do parasita favoreceu naturalmente microtúbulos com 15 protofilamentos. Os autores resolveram a estrutura desses tubos mais grossos e mostraram como acomodam os protofilamentos extras com um leve desvio da rede, mantendo-se quase perfeitamente cilíndricos. Ao comparar esses tubos de 15 protofilamentos feitos em laboratório com os observados dentro de células do parasita, a correspondência na forma e nas dimensões foi notavelmente próxima, indicando que propriedades intrínsecas da tubulina — e não uma multidão de proteínas auxiliares — são suficientes para gerar as arquiteturas distintivas do parasita.
Pistas para futuros fármacos específicos do parasita
A conclusão do estudo é que a evolução afinou a tubulina do parasita por pequenas mudanças de sequência dispersas que, coletivamente, alteram a mecânica dos microtúbulos, a arquitetura e a sensibilidade a drogas. Esses ajustes tornam os microtúbulos do parasita mais rígidos e capazes de formar tamanhos de tubo não padronizados que atendem ao seu exigente ciclo de vida, mantendo ainda o desenho básico da tubulina reconhecível. Importante para a medicina, alguns bolsões de ligação a fármacos parecem quase idênticos entre parasita e hospedeiro (como ocorre com o fármaco contra o câncer paclitaxel), sugerindo que são alvos pobres para antimaláricos seletivos. Outros, como a região que se pensa ligar ao composto semelhante a herbicida orizalin, mostram tanto deslocamentos de sequência quanto deslocamentos estruturais sutis que podem explicar por que os microtúbulos do parasita são mais vulneráveis ali do que os humanos. Mapear essas diferenças nuançadas fornece um roteiro para projetar fármacos futuros que desorganizem o esqueleto do parasita da malária enquanto deixam nossas próprias células largamente intactas.
Citação: Bangera, M., Wu, J., Beckett, D. et al. Adaptations in Plasmodium tubulin determine distinct microtubule architectures, mechanics and drug susceptibility. Nat Commun 17, 2275 (2026). https://doi.org/10.1038/s41467-026-70181-0
Palavras-chave: parasita da malária, microtúbulos, estrutura da tubulina, direcionamento de fármacos, crio-microscopia eletrônica