Clear Sky Science · pt
Catalisadores monoatômicos assimétricos Zn-N2O2 inspirados na biologia via esqueleto natural para N-alquilação eficiente de nitroarenos com álcoois
Transformando cascas descartadas em ferramentas químicas úteis
Muitos medicamentos importantes, agentes de proteção de culturas e materiais especializados contêm uma característica estrutural simples: um átomo de nitrogênio ligado a uma pequena cadeia carbônica. Produzir essas moléculas “N‑alquiladas” em escala industrial costuma exigir produtos químicos agressivos, altas temperaturas e metais caros. Este estudo apresenta uma alternativa mais verde inspirada pela própria natureza, usando átomos de zinco ancorados em um suporte feito de quitossana — um material derivado de cascas de frutos do mar descartadas — para realizar essas reações de forma mais eficiente e com menos resíduos.
Por que uma química do nitrogênio mais verde importa
Métodos convencionais de ligar cadeias carbônicas ao nitrogênio dependem de reagentes halogenados reativos e aditivos fortes que geram grandes quantidades de subprodutos. Além disso, frequentemente exigem metais preciosos raros e onerosos, como paládio ou platina, como catalisadores. Em contraste, uma abordagem mais recente chamada estratégia do “emprestando hidrogênio” usa álcoois comuns tanto como fonte da cadeia carbônica quanto do hidrogênio, com água como principal subproduto. Embora o conceito seja atraente, os catalisadores à base de metais não nobres existentes geralmente funcionam apenas sob condições severas ou com tipos limitados de materiais iniciais. O desafio tem sido projetar um catalisador de baixo custo e reciclável que possa conduzir essa reação de forma eficiente sob condições mais brandas.
Emprestando hidrogênio com átomos únicos de zinco
Os pesquisadores abordaram esse problema usando catálise monoatômica, na qual átomos metálicos isolados, em vez de partículas maiores, são ancorados numa superfície sólida. Eles dissolveram quitossana, um polímero biodegradável rico em grupos oxigenados e nitrogenados, e o transformaram em microesferas porosas tridimensionais usando um processo sol‑gel. Íons de zinco foram então introduzidos e aquecidos suavemente, fixando átomos isolados de zinco na estrutura da quitossana em um arranjo que os autores descrevem como Zn‑N2O2: cada átomo de zinco fica cercado por dois átomos de nitrogênio e dois de oxigênio vindos do suporte. Esse ambiente local inspirado na biologia imita a coordenação metálica em muitas enzimas naturais e maximiza o número de sítios ativos disponíveis para a reação.
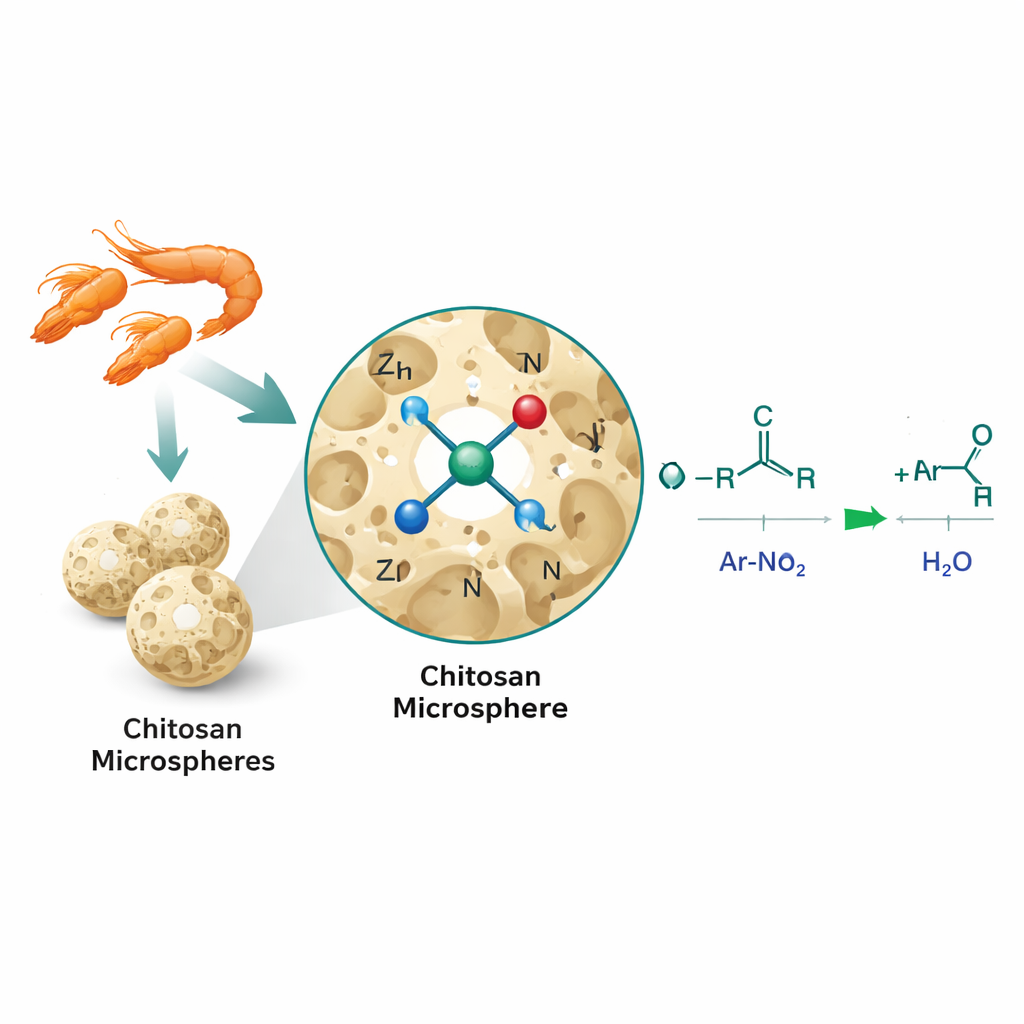
Comprovando a estrutura e o desempenho
Para confirmar que o zinco realmente existia como átomos isolados em vez de partículas maiores, a equipe combinou vários métodos avançados de imagem e espectroscopia. Microscópios eletrônicos mostraram esferas porosas de quitossana, mas sem aglomerados visíveis de zinco, enquanto imagens de alta sensibilidade (HAADF) revelaram pequenos pontos brilhantes correspondendo a átomos individuais de zinco espalhados uniformemente pela superfície. Técnicas baseadas em raios X indicaram ainda que o zinco estava ligado principalmente a nitrogênio e oxigênio, sem ligações zinco–zinco detectáveis, apoiando o cenário de átomos únicos. Essas características estruturais se traduziram em desempenho notável: em uma reação modelo entre nitrobenzeno e álcool benzílico, o catalisador de zinco sobre quitossana (Zn/CS) forneceu rendimentos muito altos com carregamento metálico excepcionalmente baixo e superou zinco comercial em carvão, nanopartículas de zinco e sais solúveis de zinco. Também funcionou para 56 combinações diferentes de nitrocompostos e álcoois, incluindo blocos de construção complexos usados em descoberta de fármacos, e pôde ser reutilizado pelo menos cinco vezes com perda mínima de atividade.
Como o catalisador realmente funciona
No nível molecular, o processo de emprestar‑hidrogênio segue uma sequência de etapas. Primeiro, o álcool é temporariamente oxidado a um aldeído enquanto transfere hidrogênio para o sítio de zinco. Esse hidrogênio é então usado para reduzir o grupo nitro a uma amina. O aldeído e a nova amina se combinam para formar uma imina, que é finalmente reduzida ao produto N‑alquilado desejado, fechando o ciclo. Ressonância magnética nuclear em tempo‑resolvido, cromatografia gasosa e reações de controle cuidadosamente projetadas confirmaram a presença de intermediários-chave ao longo dessa rota. Experimentos com marcação por deutério, nos quais hidrogênios selecionados foram substituídos por um isótopo mais pesado, mostraram que a espécie zinco–hidrogênio desempenha o papel dominante nas etapas de redução. Simulações computacionais ajudaram a explicar por que esse catalisador é tão eficaz: o ambiente assimétrico Zn‑N2O2 puxa densidade eletrônica para longe do átomo de zinco, tornando‑o um pouco pobre em elétrons. Esse ajuste eletrônico torna o zinco melhor em ligar e ativar o intermediário derivado do álcool, reduzindo a barreira de energia para a etapa mais difícil — a remoção inicial de hidrogênio do álcool.
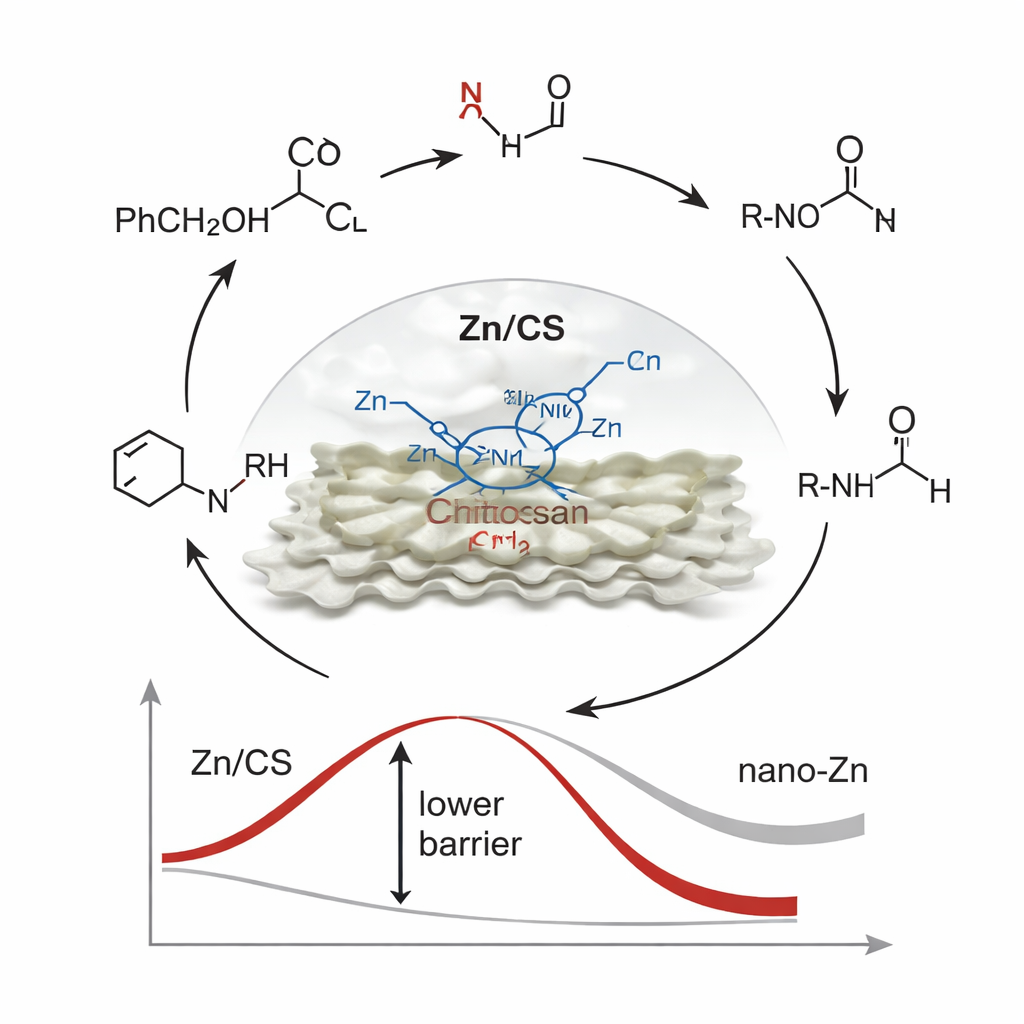
Do desperdício marinho a catalisadores inteligentes
Em termos acessíveis, este trabalho mostra como átomos individuais de zinco, arranjados com precisão sobre um suporte natural e esponjoso feito de resíduos de frutos do mar, podem superar muitos catalisadores metálicos tradicionais em uma classe importante de reações químicas. Ao usar álcoois em vez de reagentes tóxicos e gerar principalmente água como subproduto, o sistema oferece uma maneira mais limpa e potencialmente mais econômica de produzir uma ampla gama de moléculas contendo nitrogênio, incluindo motivos farmacêuticos. A combinação de um suporte de biopolímero renovável com sítios monoatômicos finamente ajustados ilustra uma rota promissora para uma química mais sustentável, em que reações industrialmente úteis emprestam princípios de design — e alguns de seus matérias‑primas — da natureza.
Citação: Huang, Y., Li, Y., Yin, X. et al. Bio-inspired asymmetric Zn-N2O2 single-atom catalysts via natural skeleton for efficient N-alkylation of nitroarenes with alcohols. Nat Commun 17, 2242 (2026). https://doi.org/10.1038/s41467-026-70172-1
Palavras-chave: catálise monoatômica, química verde, emprestando hidrogênio, quitina/quitossana, catalisador de zinco