Clear Sky Science · pt
Montagem do grupo covalente em biossíntese de fostriecina envolve malonilação-lactonização por uma tioesterase bifuncional e desmalonilação enzimática
Como a natureza constrói um pequeno grupo reativo
Medicamentos contra o câncer e antibióticos frequentemente dependem de alguns átomos arranjados de forma precisa — um pequeno “grupo reativo” que se prende a uma proteína e a desativa. O composto natural fostriecina é uma dessas moléculas, com forte atividade contra enzimas envolvidas no crescimento celular. Mas sua estrutura complexa dificulta a fabricação ou modificação em laboratório. Este estudo revela, passo a passo, como bactérias montam o grupo reativo crucial da fostriecina, expondo truques enzimáticos que químicos agora podem aproveitar para projetar novos medicamentos.
O gancho especial em fármacos naturais potentes
Muitos fármacos promissores derivados de bactérias do solo pertencem à família dos poliquetídeos. Dentro dessa família, um subgrupo carrega um anel reativo, conhecido pelos químicos como uma δ-lactona α,β-insaturada, que age como um anzol molecular. Ele pode formar uma ligação permanente com certos aminoácidos em proteínas, desligando interruptores biológicos chave. Na fostriecina e em moléculas relacionadas, esse gancho vem acompanhado de um grupo fosfato que os ajuda a focalizar enzimas específicas que controlam a divisão celular. Essas características os tornam atraentes como candidatos anticâncer, mas a mesma reatividade e complexidade estrutural os tornam difíceis de sintetizar e instáveis durante o armazenamento.
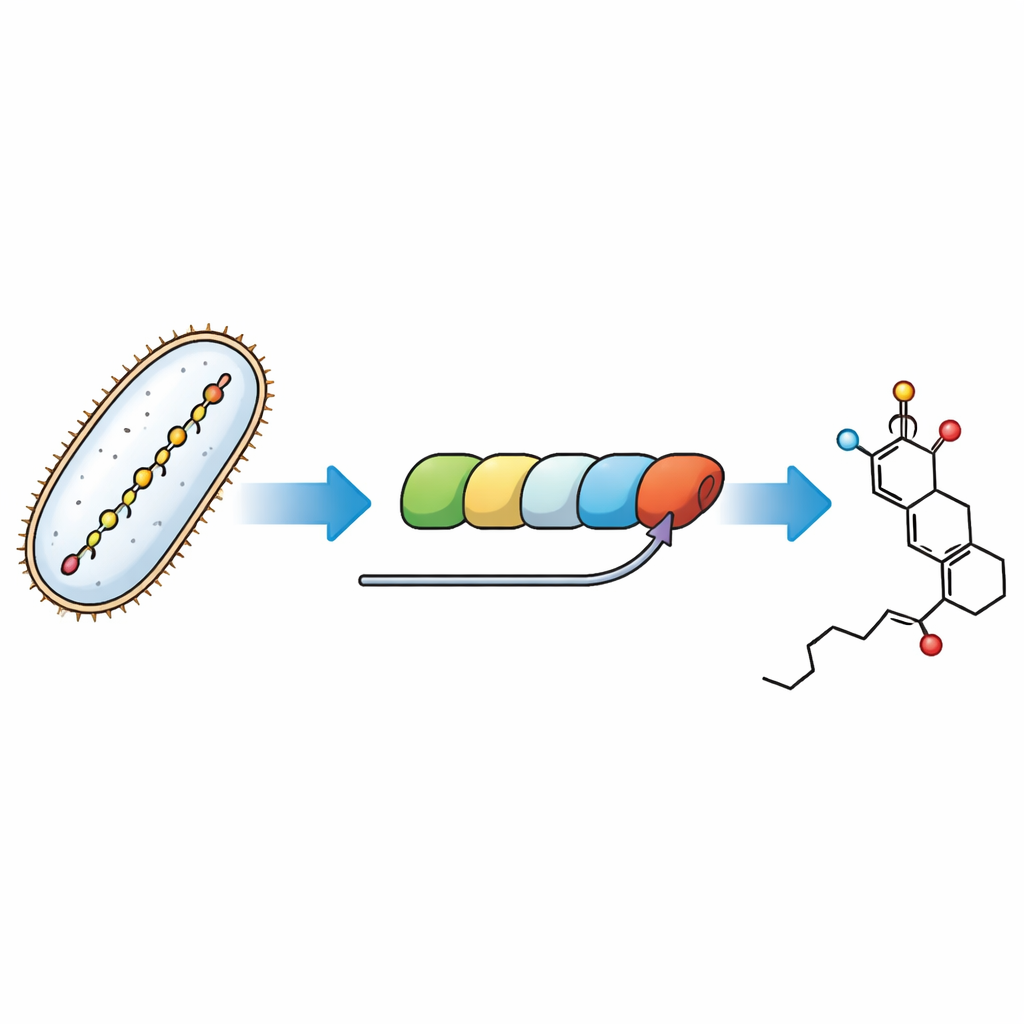
Rastreando as etapas finais de uma linha de montagem molecular
Bactérias constroem a fostriecina usando uma máquina proteica modular massiva chamada poliquetídeo sintetase — uma linha de montagem onde cada estação alonga e modela uma cadeia carbônica em crescimento. O enigma abordado aqui é como o último módulo dessa máquina forja o anel do grupo reativo e instala uma “alça” temporária chamada grupo malonil, que depois precisa ser removida. Ao recriar a via em tubos de ensaio com enzimas purificadas e análogos de pequenas moléculas cuidadosamente desenhados para imitar os intermediários naturais, os pesquisadores puderam observar passos individuais e atribuí-los a partes específicas da linha de montagem.
Uma enzima multitarefa com um talento inesperado
A equipe descobriu que a estação final da linha de montagem, um domínio chamado FosTE, comporta-se de maneira inédita. Versões típicas desse domínio simplesmente cortam produtos finalizados da linha. FosTE, em contraste, primeiro captura um fragmento malonil de um bloco de construção celular comum e o transfere para um oxigênio preciso na cadeia em crescimento, e então ajuda a cadeia a se dobrar para fechar o anel do grupo reativo. A mutação de uma única serina reativa em FosTE interrompe ambas as atividades. Modelagem estrutural aponta para dois resíduos de arginina positivamente carregados no sítio ativo que sustentam o fragmento malonil e o posicionam para transferência — funções normalmente desempenhadas por outro tipo de enzima. Trocar essas argininas por resíduos neutros apaga a etapa de transferência do malonil enquanto deixa a formação básica do anel largamente intacta, confirmando seu papel crítico.
Fixando o grupo reativo e evitando desperdício
Uma vez que o anel é formado e carrega seu grupo malonil temporário, outra enzima, FosM, deve remover esse grupo para revelar o grupo reativo totalmente armado. O estudo mostra que FosM trabalha eficientemente somente depois que outra enzima, uma quinase de ampla especificidade chamada FosH, adiciona um fosfato em uma posição próxima na molécula. Quando os pesquisadores forneceram o anel malonilado somente à FosM, ocorreu apenas conversão modesta. Adicionar FosH primeiro levou à remoção quase completa do grupo malonil e à formação da unidade reativa final. Importante, FosH também pode fosforilar intermediários “desviantes” relacionados que surgem de reações laterais, resgatando-os para que possam ser processados corretamente em vez de serem perdidos como produtos sem saída.
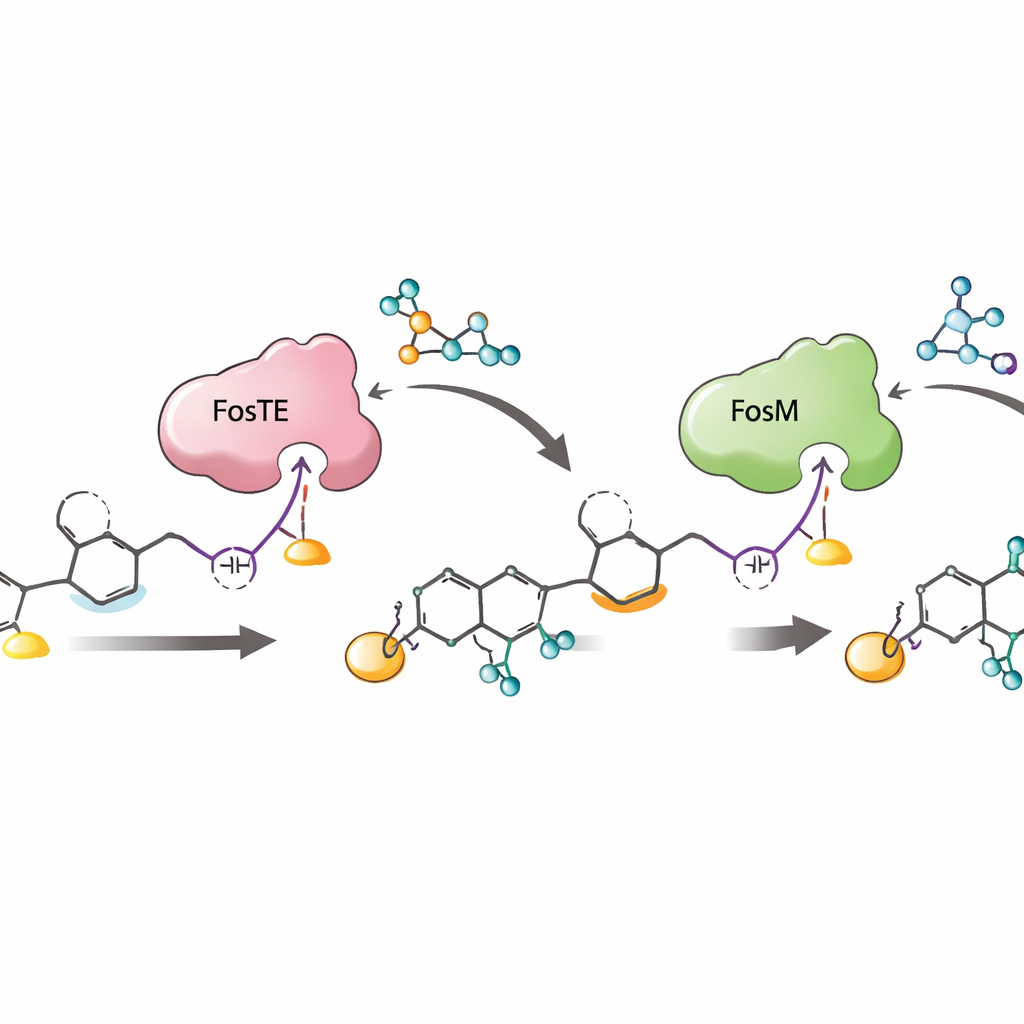
Por que essa coreografia enzimática importa
Em conjunto, o trabalho revela uma sequência estritamente coreografada: extensão da cadeia na linha de montagem, adição de malonil e fechamento do anel catalisados por FosTE, fosforilação por FosH e, finalmente, remoção do malonil desencadeada por FosM. Essa ordem não apenas constrói o delicado grupo reativo de maneira eficiente, como também protege intermediários instáveis de se desmontarem e maximiza a produção da forma desejada e fosforilada, que é a mais ativa como candidato farmacológico. Ao expor como um único domínio enzimático pode tanto decorar quanto liberar uma molécula em crescimento — e como enzimas parceiras afinam e salvam intermediários reativos — o estudo oferece um roteiro para projetar novos poliquetídeos com grupos reativos e para construir rotas sintéticas mais curtas e eficientes para agentes anticâncer complexos como a fostriecina.
Citação: Nguyen, L.N.K.T., Schlotte, L., Hoffmann, J. et al. Covalent warhead assembly in fostriecin biosynthesis involves malonylation-lactonisation by a bifunctional thioesterase and enzymatic demalonylation. Nat Commun 17, 2365 (2026). https://doi.org/10.1038/s41467-026-70144-5
Palavras-chave: fostriecina, biossíntese de poliquetídeos, engenharia de enzimas, grupos ativos de produtos naturais, síntese quimioenzimática