Clear Sky Science · pt
Regulação translacional pela desulfuração oxidativa de modificações em tRNA
Como as células ajustam a produção de proteínas sob estresse
Cada célula precisa decidir quais proteínas produzir, com que velocidade e quando reduzir a produção. Este estudo revela um interruptor químico sutil em moléculas de RNA de transferência (tRNA) que ajuda as células a diminuir a síntese proteica quando o ambiente celular fica mais oxidante, como durante inflamação ou estresse metabólico. Ao observar como esse interruptor se comporta em células de mamíferos e em sistemas de ensaio in vitro, os pesquisadores descobrem uma nova forma pela qual alterações semelhantes a danos no RNA podem, na verdade, atuar como um sinal regulatório.
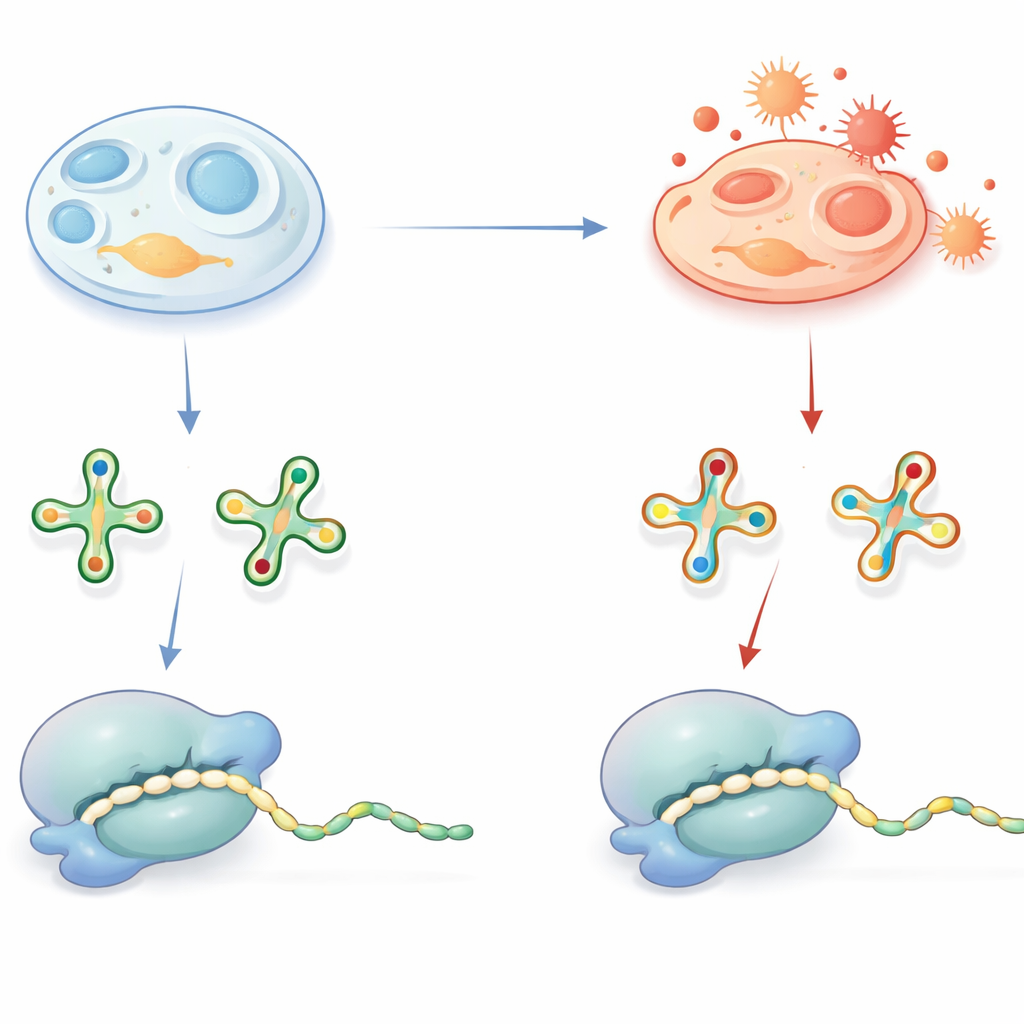
Pequenas marcas no tRNA com grandes consequências
Os tRNAs funcionam como adaptadores que leem “palavras” de três letras no RNA mensageiro e entregam os aminoácidos correspondentes durante a síntese proteica. Para desempenhar essa função com precisão e eficiência, muitos tRNAs carregam decorações químicas especiais, especialmente numa posição-chave que contata a terceira letra de cada códon. Uma decoração difundida é um grupo contendo enxofre em uma base uridina, frequentemente escrito como um derivado de 2-tio-uridina. Em condições saudáveis, esse grupo de enxofre ajuda o tRNA a reconhecer códons corretos que terminam em A ou G e favorece uma tradução rápida e sem erros. Defeitos nessas decorações já são conhecidos por causar doenças humanas, ressaltando sua importância.
Quando o estresse oxidativo reescreve o tRNA
O grupo de enxofre que melhora o pareamento traz um lado negativo: é quimicamente vulnerável à oxidação. A equipe investigou se, dentro das células, esse grupo é efetivamente removido sob condições oxidativas e o que isso significaria para a síntese proteica. Usando espectrometria de massa sensível, identificaram versões oxidadas e livres de enxofre dessas bases de tRNA — chamadas de derivados h2U — em tecidos de camundongo, mitocôndrias de porco, bactérias, leveduras e diversas linhagens celulares humanas. Um experimento astuto com spike-in usando um traçador de tRNA bacteriano mostrou que essas marcas h2U não são artefatos gerados durante a preparação das amostras, mas são formadas dentro de células vivas. Embora as versões oxidadas estivessem presentes apenas em uma fração dos tRNAs, sua abundância variou entre tecidos e tipos celulares, sugerindo que o estado redox celular e a capacidade antioxidante influenciam com que frequência essa conversão ocorre.
Como tRNAs oxidados freiam a linha de montagem
Os pesquisadores testaram em seguida como esses tRNAs alterados atuam durante a síntese proteica. Converteram quimicamente a forma contendo enxofre para a forma oxidada h2U em tRNA total e usaram um sistema de tradução humana totalmente reconstituído in vitro. Uma proteína repórter cuja produção depende fortemente desses tRNAs modificados apresentou produção fortemente reduzida quando os tRNAs foram desulfurizados, enquanto um repórter controle que evita os códons afetados traduziu normalmente. Ensaios bioquímicos revelaram o porquê: tRNAs oxidados para lisina, glutamina e glutamato foram aminoacilados com muito menos eficiência, enquanto os tRNAs correspondentes à arginina foram, em grande parte, preservados. Importante, tRNAs que carregavam h2U ainda apareciam em frações ligadas a ribossomos (polissômicas) de células, indicando que eles participam da tradução, mas o fazem de forma ineficaz.
Uma visão estrutural do pareamento enfraquecido
Para ver exatamente como a oxidação altera o pareamento, a equipe usou microscopia crioeletrônica de alta resolução para imagear ribossomos bacterianos programados com tRNA humano para lisina e códons específicos. No estado normal, contendo enxofre, a base modificada na posição de “wobble” do tRNA formava ou um pareamento padrão com um códon terminando em A, ou um pareamento de wobble especial com um códon terminando em G, ambos firmemente acomodados no centro de decodificação do ribossomo. Após a desulfuração, a mesma base pôde fazer apenas um contato fraco com o códon terminando em A e formou um pareamento de wobble menos estável com o códon terminando em G. Ensaios de ligação corresponderam a essas estruturas: o tRNA de lisina oxidado perdeu essencialmente a capacidade de reconhecer o códon AAA e reconheceu o códon AAG com muito menos eficiência. Em conjunto, esses achados mostram que um ajuste químico aparentemente pequeno pode se traduzir em desacelerações específicas por códon na síntese proteica.
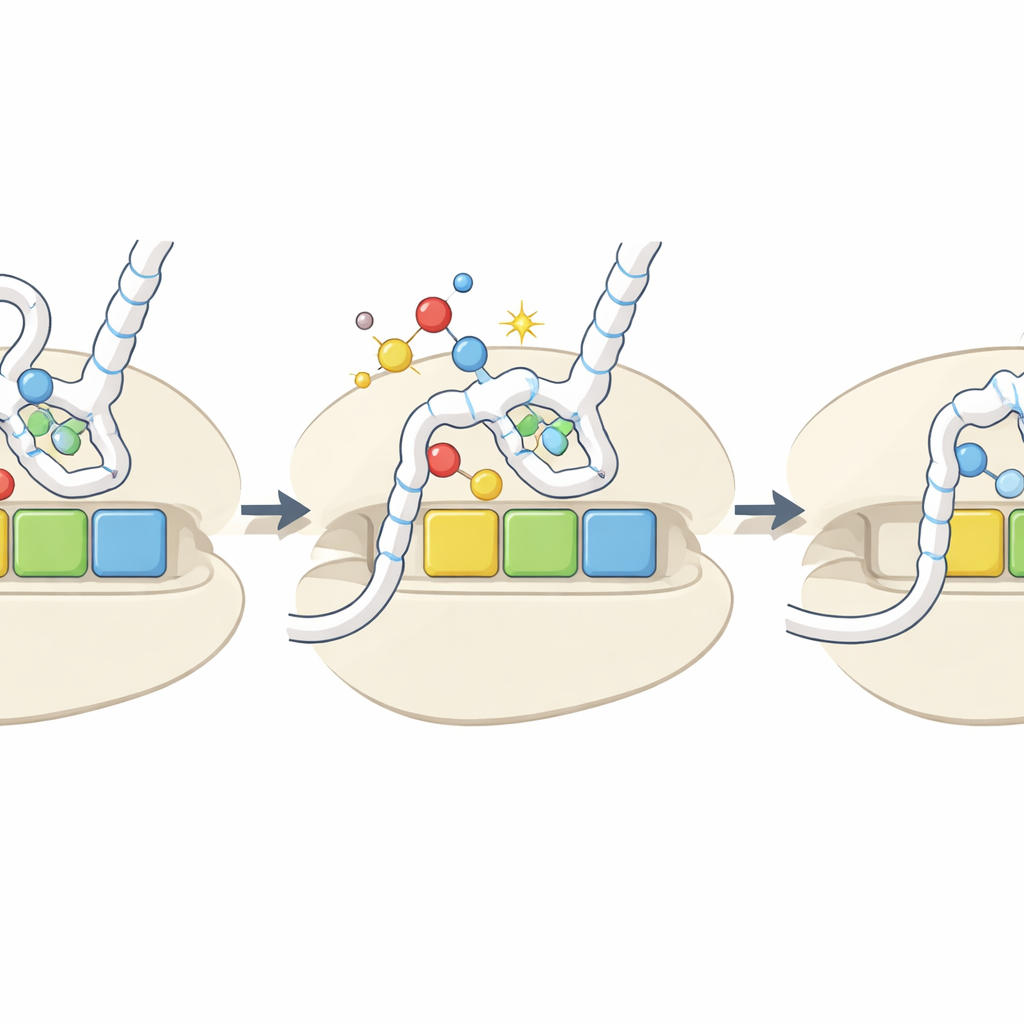
Um sinal de dano que vira botão regulatório
No conjunto, o estudo propõe que a remoção oxidativa do enxofre de bases-chave do tRNA atua como um sensor integrado do ambiente redox da célula. Sob estresse oxidativo, mais tRNAs são convertidos para a forma h2U, que são mal carregados e se ligam fracamente a certos códons. Isso desacelera seletivamente a tradução nesses códons, potencialmente alterando a estabilidade dos RNAs mensageiros afetados, modificando o modo como as proteínas se dobram e acionando vias de resposta ao estresse quando ribossomos travam. Embora as marcas oxidadas sejam relativamente raras e seus níveis nem sempre aumentem fortemente sob estresse experimental, seus efeitos específicos por códon e por aminoácido significam que até mudanças modestas podem remodelar quais proteínas são produzidas e com que rapidez durante condições desafiadoras.
Citação: Mo, Y., Ishiguro, K., Miyauchi, K. et al. Translational regulation by oxidative desulfuration of tRNA modifications. Nat Commun 17, 2125 (2026). https://doi.org/10.1038/s41467-026-70126-7
Palavras-chave: modificação de tRNA, estresse oxidativo, síntese de proteínas, regulação da tradução, danos em RNA