Clear Sky Science · pt
Mirando o uso dependente de tRNA da tirosina revela uma vulnerabilidade metabólica no carcinoma hepatocelular
Privando células cancerígenas de um bloco construtor comum
As células do câncer de fígado, como todas as células que se dividem rapidamente, precisam de um suprimento constante de aminoácidos — os pequenos blocos construtores das proteínas. Este estudo revela que o carcinoma hepatocelular, a forma mais comum de câncer de fígado, tem uma fraqueza inesperada: depende fortemente do aminoácido tirosina tanto para a produção de energia quanto para a sobrevivência. Ao limitar seletivamente como as células cancerosas usam a tirosina, os pesquisadores conseguiram retardar o crescimento tumoral, danificar as usinas de energia das células cancerosas e desencadear uma forma de morte celular que pode ser aproveitada para novos tratamentos.
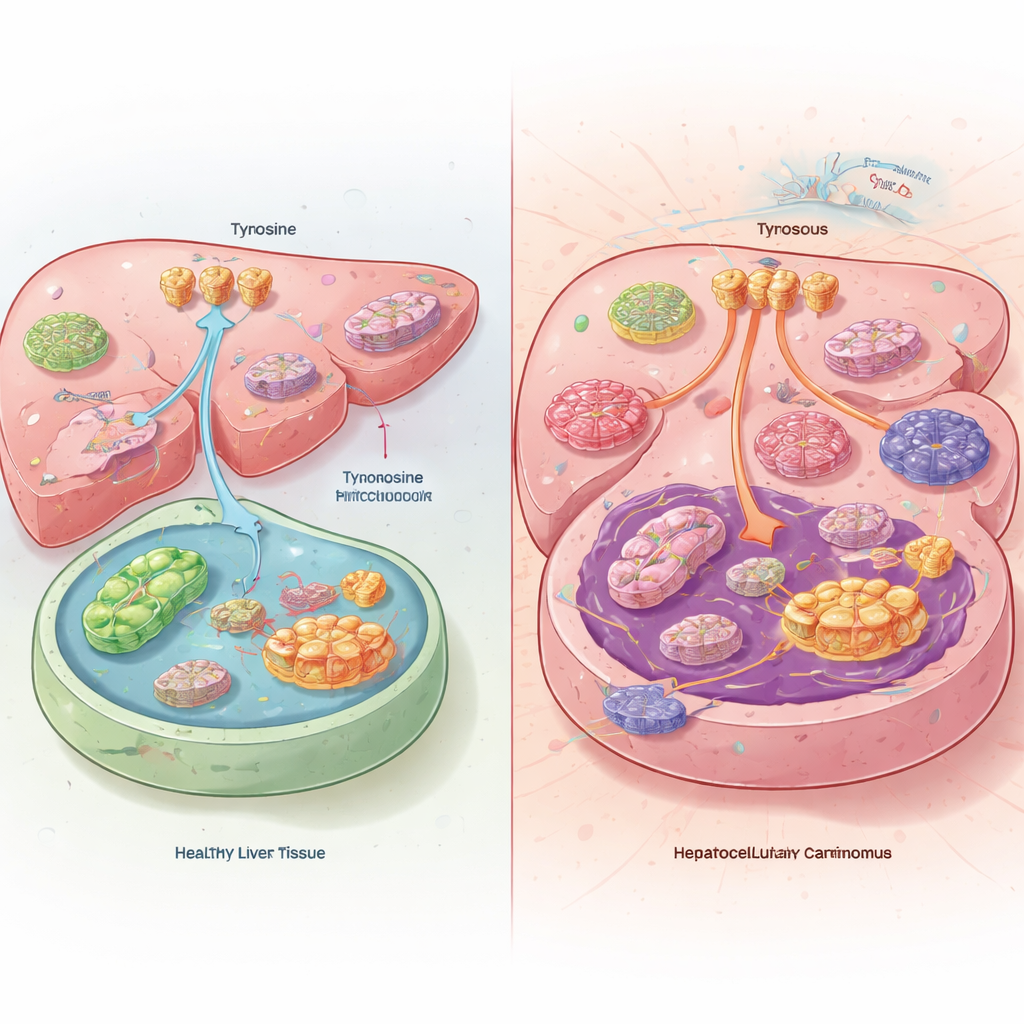
Um desequilíbrio oculto nos tumores do fígado
Quando a equipe comparou tumores hepáticos com tecido hepático saudável de pacientes e de camundongos, encontrou algo surpreendente. Dentro das células cancerosas, os níveis de tirosina eram na verdade baixos, apesar de os tumores estarem captando mais tirosina da corrente sanguínea e degradando menos desse aminoácido. Em vez de queimar a tirosina como combustível, os tumores hepáticos a redirecionaram para a produção de proteínas. Os cânceres conseguiram isso aumentando a atividade dos transportadores de tirosina na superfície celular e reduzindo as enzimas que normalmente degradam a tirosina no fígado. Camundongos alimentados com dieta sem tirosina desenvolveram tumores menores e viveram mais, enquanto tirosina adicional na dieta fez com que seus cânceres crescessem mais rápido.
Como o câncer reconecta a produção de proteínas
Os pesquisadores rastrearam essa fome por tirosina até um gene potente que dirige o câncer chamado MYC. Em tumores hepáticos, o MYC ativa uma proteína chamada YARS1, que liga tirosina a um RNA de transferência específico (tRNA-TyrGUA). Esse tRNA carregado é o que os ribossomos precisam para construir proteínas ricas em tirosina. O estudo mostrou que os cânceres do fígado aumentam tanto YARS1 quanto seu tRNA correspondente, garantindo um fluxo privilegiado de tirosina para a síntese proteica. Destruir essa via — seja reduzindo os níveis de tirosina, silenciando YARS1 ou o tRNA-TyrGUA, ou bloqueando a carga de tirosina — tornou as células de câncer de fígado muito menos viáveis em placas e em camundongos, revelando uma vulnerabilidade metabólica intimamente ligada às suas altas necessidades de produção proteica.
Comprometendo as usinas e o equilíbrio lipídico
Ao combinar medidas genômicas de RNA, produção proteica e metabólitos, a equipe identificou dois alvos especialmente sensíveis à restrição de tirosina. Um, NDUFB8, é um componente do complexo I mitocondrial, uma parte central da maquinaria geradora de energia celular. O outro, SCD1, ajuda a converter gorduras saturadas em gorduras monoinsaturadas que são mais seguras para armazenar em membranas e gotículas celulares. Quando a tirosina para tradução foi restringida, a produção de NDUFB8 e SCD1 caiu, enquanto seus níveis de RNA permaneceram em grande parte inalterados — evidência clara de que a tradução, e não a expressão gênica, estava sendo afetada. Isso levou a um complexo I mal montado, respiração celular reduzida, excesso de espécies reativas de oxigênio e uma mudança nas gorduras de monoinsaturadas para formas poli-insaturadas mais frágeis e facilmente oxidadas.
Forçando as células cancerosas a uma morte dependente de ferro
O dano mitocondrial combinado e as gorduras instáveis empurraram as células do câncer de fígado em direção à ferroptose, uma forma de morte celular dependente de ferro impulsionada pela peroxidação lipídica. Os tumores tentaram reagir aumentando bloqueadores naturais da ferroptose, como GPX4 e moléculas relacionadas, mas uma grande triagem por CRISPR mostrou que desabilitar esses protetores tornava a restrição de tirosina ainda mais letal. Em modelos celulares e em camundongos, combinar estratégias de limitação de tirosina com fármacos que inibem GPX4 ou BCL2 — ou com medicamentos já usados no câncer de fígado como sorafenibe e venetoclax — produziu controle tumoral mais forte, menor carga tumoral e maior sobrevida.
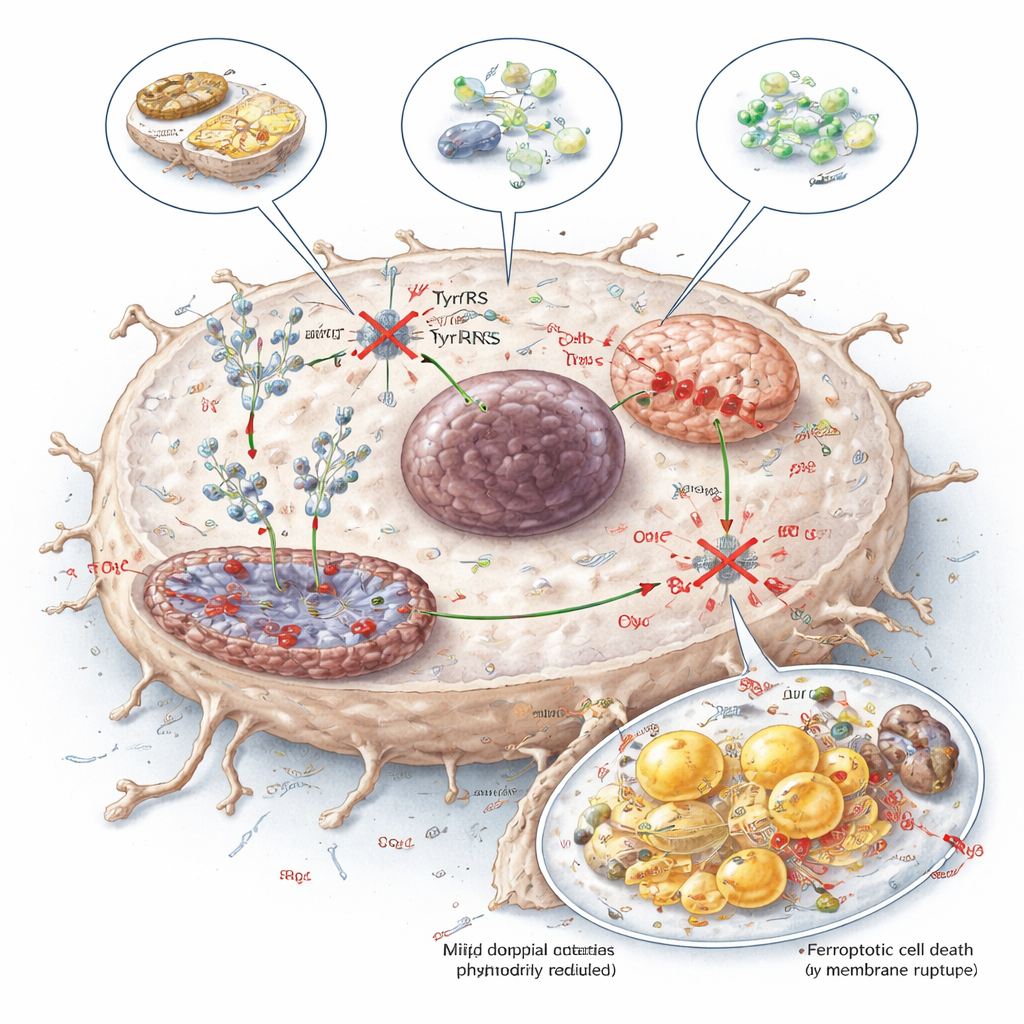
Transformando uma fraqueza metabólica em terapia
Para explorar maneiras práticas de explorar essa fraqueza, os pesquisadores testaram três abordagens: uma dieta restrita em tirosina, uma enzima (TAL) que degrada tirosina enzimaticamente, e uma pequena molécula chamada tirosinol que compete com a tirosina pela ligação à YARS1. Todas as três reduziram a disponibilidade de tirosina para a síntese proteica, diminuíram os níveis de NDUFB8 e SCD1, prejudicaram a função mitocondrial e aumentaram a ferroptose nos tumores hepáticos, enquanto mostraram efeitos manejáveis nos tecidos normais dos camundongos. Para o leitor não especializado, a mensagem é que os cânceres do fígado parecem estar viciados em tirosina não apenas como nutriente, mas como um combustível preciso para sua maquinaria de produção de proteínas. Alvejar essa dependência — por dieta, enzimas ou fármacos — oferece uma maneira promissora de enfraquecer tumores e aumentar o impacto de tratamentos existentes.
Citação: Zhang, H., Wang, Z., Zhao, Y. et al. Targeting tRNA-dependent tyrosine usage unveils a metabolic vulnerability in hepatocellular carcinoma. Nat Commun 17, 2244 (2026). https://doi.org/10.1038/s41467-026-70112-z
Palavras-chave: câncer de fígado, metabolismo de aminoácidos, tirosina, mitocôndria, ferroptose