Clear Sky Science · pt
Identificação sistemática de interações entre estruturas de RNA específicas de variantes e pequenas moléculas exemplificada por G-quadruplexes de RNA
Por que pequenas alterações no RNA importam para medicamentos do futuro
A maioria de nós herda pequenas diferenças em nosso DNA que nos tornam únicos. Essas mudanças sutis podem remodelar delicadamente as dobras das moléculas de RNA dentro de nossas células. O novo estudo apresenta uma maneira de observar como esses ajustes genéticos alteram a afinidade de fármacos experimentais que têm o RNA como alvo. Isso importa porque o mesmo medicamento pode agir de forma muito diferente de uma pessoa para outra, especialmente em cânceres ou doenças genéticas.
Nova forma de ver onde os fármacos tocam o RNA
Muitos desenvolvedores de fármacos estão agora olhando para o RNA, e não apenas para proteínas, como alvos terapêuticos. Pequenas moléculas podem se prender a formas especiais de RNA e influenciar como os genes são lidos, mas até agora a maioria dos métodos funcionava apenas em uma sequência de RNA “referência”. Eles ignoravam em grande parte as incontáveis alterações de uma única letra encontradas em pacientes reais. Os autores criaram uma abordagem de alto rendimento chamada BIVID-MaP que pode testar simultaneamente milhares de variantes de RNA e identificar onde uma pequena molécula se liga a cada uma, com resolução de um único nucleotídeo. 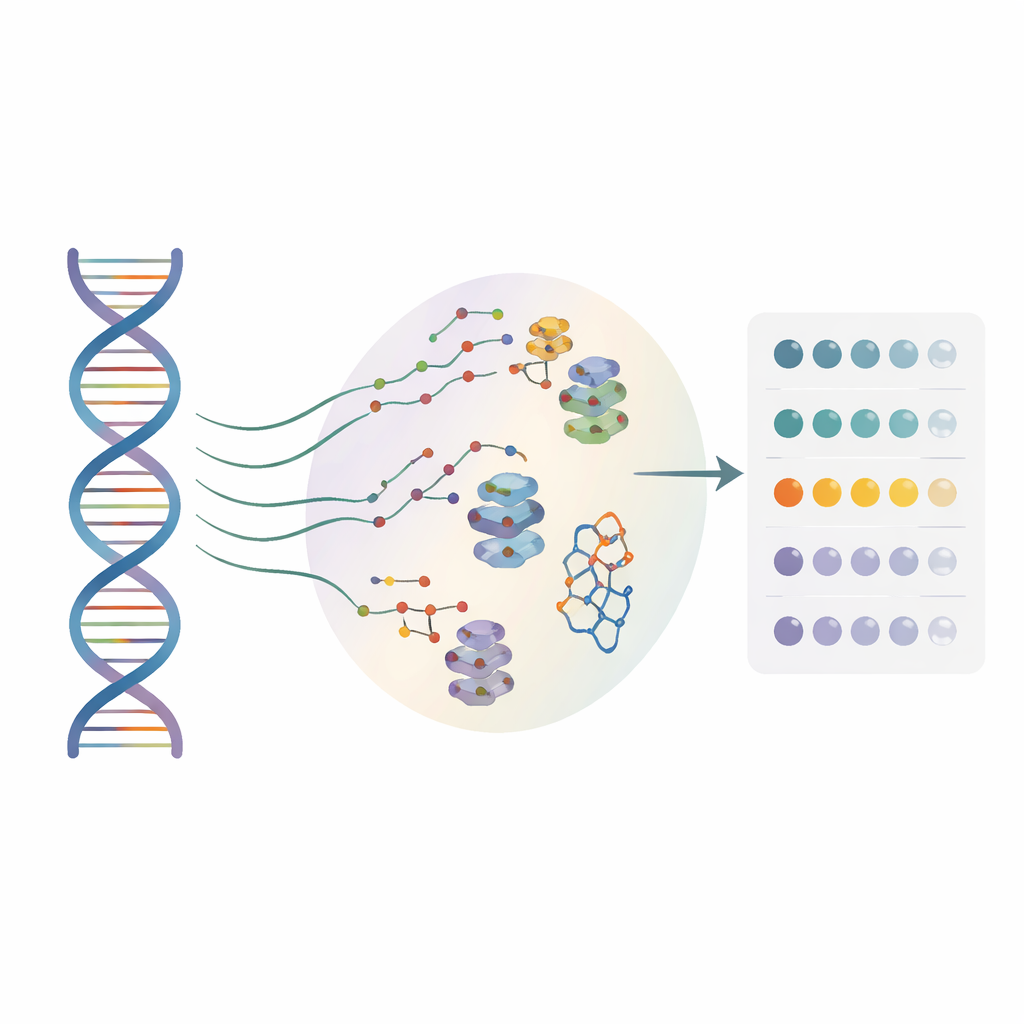
Transformando marcas químicas em um sinal legível
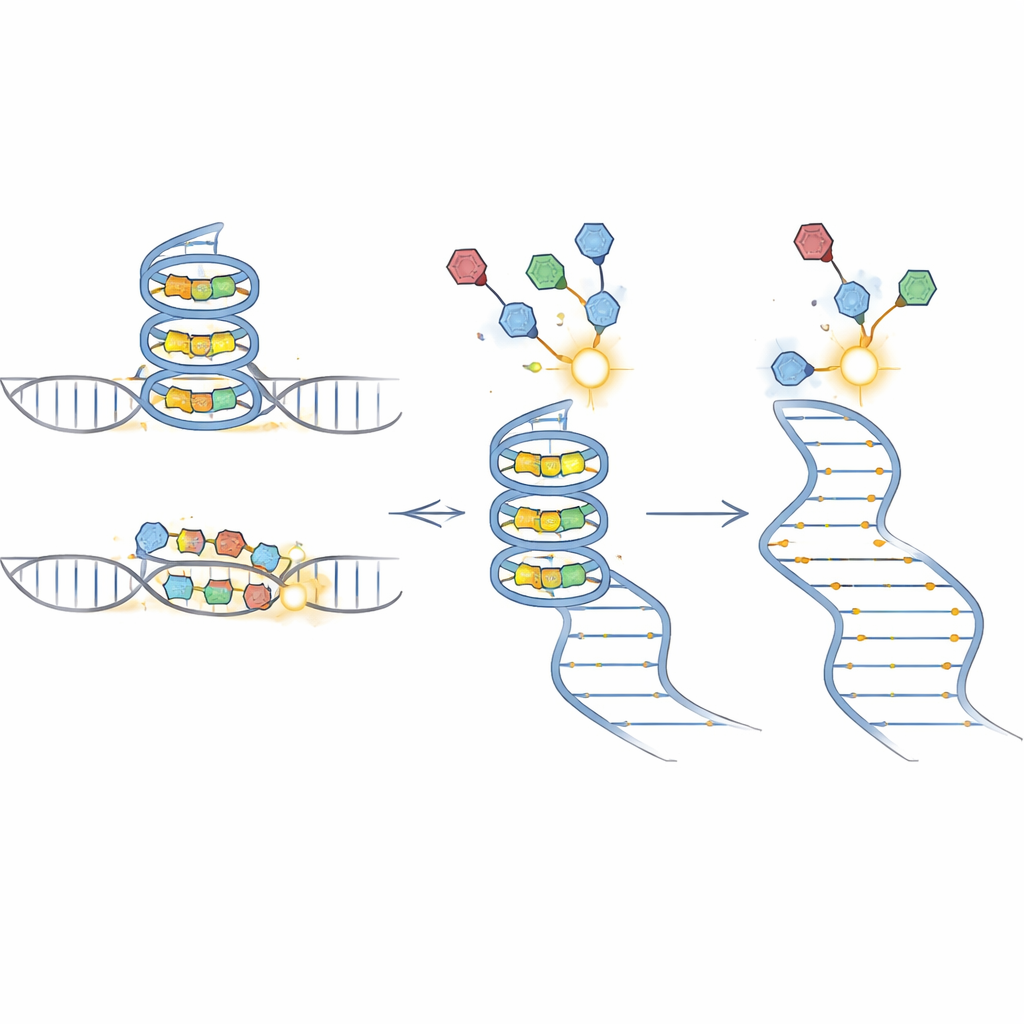
O BIVID-MaP funciona em três etapas principais. Primeiro, a equipe anexa uma etiqueta reativa a uma pequena molécula que se liga ao RNA. Quando esse composto marcado se acomoda em sua estrutura de RNA preferida, como um G-quadruplex compacto formado por sequências ricas em guanina, a etiqueta forma uma ligação química permanente com uma base de RNA próxima. Segundo, uma enzima especial copia o RNA modificado em DNA. Ao encontrar uma dessas marcas químicas, ela tende a “pular” uma base, criando uma pequena deleção na cópia. Terceiro, o sequenciamento profundo lê essas assinaturas de deleção em milhões de moléculas. Como quase toda a sequência circundante é preservada, as deleções podem ser atribuídas com precisão a variantes genéticas específicas em uma mistura.
Comprovando o método em um caso de teste controlado
Para confirmar que o BIVID-MaP realmente detecta ligações específicas de variantes, os pesquisadores estudaram um segmento de RNA do gene CD44 que normalmente forma um G-quadruplex. Uma única mudança de G para A desestabiliza essa estrutura. Em uma mistura contendo ambas as versões, apenas a forma intacta exibiu fortes sinais de deleção perto da região dobrada quando exposta a uma sonda à base de berberina, e ensaios independentes verificaram uma ligação mais forte ali. O mutante, que não pode formar a mesma conformação, produziu muito menos deleções e ligação mais fraca. Outras técnicas comuns de mapeamento ou perderam essa diferença ou produziram ruído confuso, ressaltando a sensibilidade e especificidade superiores da nova abordagem.
Escaneando mutações associadas ao câncer em muitos genes
A equipe então ampliou a escala. Eles construíram uma biblioteca de RNA de regiões não traduzidas 5′ (5′ UTRs) de 283 genes relacionados ao câncer, cada uma pareada com mutações somáticas reais relatadas em tumores. Usando uma sonda que reconhece estruturas do tipo G-quadruplex, o BIVID-MaP revelou numerosas mutações que ou reforçaram ou enfraqueceram a ligação de pequenas moléculas. Em genes como DAXX e ING2, mudanças de uma única letra em trechos ricos em guanina alteraram marcadamente a ligação, em concordância com testes biofísicos independentes de formação de G-quadruplex e medidas diretas de ligação por espectrometria de massa. Em alguns casos, mutações fora dos tratos óbvios de G ainda deslocaram a ligação ao alterar sutilmente a probabilidade de pareamento das bases vizinhas, remodelando o “conjunto” estrutural sem alterar grosseiramente a dobra prevista global.
Vendo o que previsões computacionais deixam passar
É importante notar que as ferramentas existentes de predição de estrutura de RNA e de G-quadruplex frequentemente falharam em prever as mudanças que o BIVID-MaP revelou. Algumas variantes que mal alteravam as pontuações computacionais produziram grandes diferenças reais na ligação. Outras pareciam afetar a ligação em uma família de compostos que visam G-quadruplexes, enquanto certas mutações tiveram efeitos específicos para um dado fármaco. Isso mostra que variantes de um único nucleotídeo podem ajustar a paisagem das dobras do RNA e dos contatos com fármacos de maneiras difíceis de inferir apenas a partir da sequência.
O que isso significa para fármacos personalizados que visam RNA
Os autores concluem que o BIVID-MaP oferece uma rota poderosa para mapear como diferenças genéticas individuais remodelam estruturas de RNA e suas interações com pequenas moléculas. Ao converter modificações químicas locais em assinaturas precisas de deleção, o método pode examinar milhares de variantes em paralelo e destacar aquelas que alteram de forma relevante a ligação de fármacos. A longo prazo, tais mapas poderiam orientar o desenho de medicamentos que visam RNA mais eficazes e seguros para uma população diversa de pacientes, além de revelar estruturas de RNA previamente ocultas que podem servir como novos alvos farmacológicos.
Citação: Miyashita, E., Onizuka, K., Chen, Y. et al. Systematic identification of variant-specific RNA structure-small molecule interactions exemplified by RNA G-quadruplexes. Nat Commun 17, 2243 (2026). https://doi.org/10.1038/s41467-026-70097-9
Palavras-chave: fármacos que visam RNA, G-quadruplex, variantes genéticas, ligação de pequenas moléculas, mutações no câncer