Clear Sky Science · pt
Otimização da organização espacial dos anéis de FtsZ para constrição em grande escala em células sintéticas
Por que anéis minúsculos importam para construir células sintéticas
Imagine construir uma célula artificial simples que possa crescer e se dividir sozinha. Para isso, os cientistas precisam aprender a beliscar uma membrana macia, parecida com uma bolha de sabão, de forma controlada, usando apenas algumas peças biológicas. Este estudo mostra como uma proteína bacteriana pode ser auxiliada a formar anéis grandes e estáveis em grandes bolhas de gordura, permitindo que essas “células” modelo se contraiam quase até a divisão. Revela que tipo de arquitetura proteica é necessária para dobrar e remodelar uma membrana na escala de uma célula inteira.
Tomando emprestado o kit de divisão da natureza
Muitas bactérias se dividem usando uma proteína chamada FtsZ, parente distante da tubulina que constrói o esqueleto interno das nossas células. O FtsZ monta filamentos que se reúnem em um anel no ponto médio da célula, marcando onde ela vai se partir. Em bactérias vivas, um conjunto de proteínas auxiliares prende esse anel à membrana interna, o posiciona no meio da célula e o liga a enzimas que remodelam a parede celular. Tentativas anteriores em laboratório de recriar essa maquinaria em vesículas do tamanho celular conseguiram formar anéis e causar pequenas depressões na membrana, mas não uma constrição suave e progressiva que remodelasse uma vesícula gigante em duas metades quase separadas.
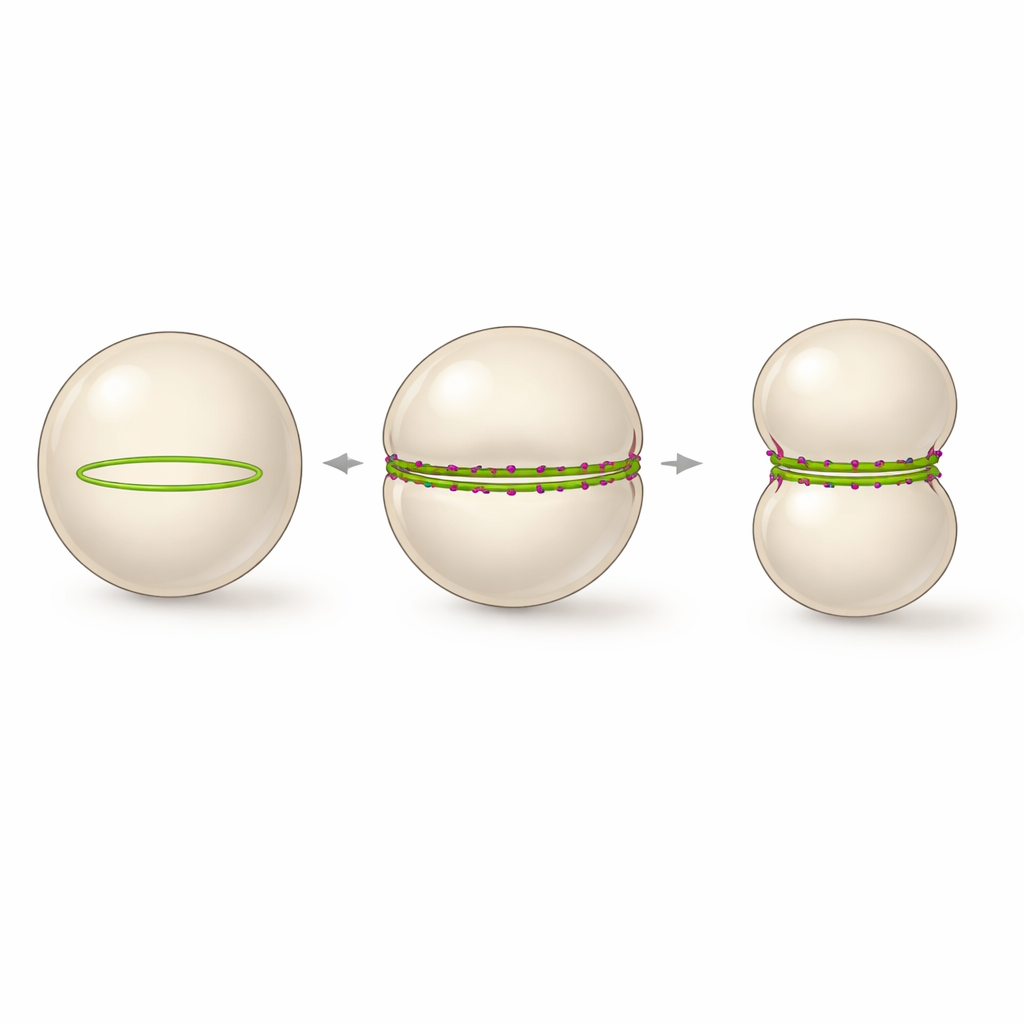
Uma abordagem minimalista para uma casca em divisão
Os autores perguntaram-se se poderiam reduzir esse sistema a apenas duas peças: uma versão do FtsZ capaz de aderir diretamente às membranas, e uma cauda curta carregada positivamente de outra proteína de divisão, FtsN. Eles encapsularam esses componentes dentro de vesículas unilamelares gigantes — esferas ocas de lipídio que se assemelham a células simplificadas — e forneceram a molécula de energia GTP e um análogo de GTP de ação lenta para ajustar a dinâmica proteica. Sem a cauda de FtsN, o FtsZ formou muitos anéis e manchas pequenos que só provocavam amassados locais. Com excesso do fragmento de FtsN (chamado cytoFtsN), esses pequenos anéis se reorganizaram em um único anel grande que envolveu a vesícula perto do equador e foi capaz de se contrair ao longo de várias horas.
De uma rede emaranhada a um anel contrátil único
Para entender como esse pequeno peptídeo altera tanto o comportamento, a equipe observou filamentos de FtsZ em membranas suportadas e planas com microscopia de alta resolução. Normalmente, o FtsZ nessas superfícies forma vórtices curvos e turbulentos. A adição de quantidades crescentes de cytoFtsN apagou gradualmente esses redemoinhos e os substituiu por feixes mais retos e alinhados. A análise quantitativa de imagem confirmou que a rede se tornou mais coerente e ordenada à medida que a concentração de peptídeo aumentava. Experimentos de recuperação de fluorescência mostraram que as subunidades dentro desses feixes trocavam mais lentamente, indicando que o peptídeo estabiliza os filamentos e reduz sua dinâmica de reciclagem.

"Velcro" eletrostático que tranca os filamentos juntos
Medidas bioquímicas revelaram que cytoFtsN e FtsZ interagem principalmente por cargas elétricas opostas: o FtsZ tem carga global negativa, enquanto o peptídeo carrega aglomerados de cargas positivas. Em níveis mais baixos de sal, o peptídeo se ligou mais fortemente, promoveu a formação de feixes mais espessos de FtsZ em solução e retardou a quebra dos filamentos ao amortecer a atividade de hidrólise de GTP da proteína. Quando os pesquisadores alteraram resíduos positivamente carregados chave no peptídeo, ou aumentaram a concentração de sal para cancelar a atração eletrostática, os efeitos de emaranhamento e reorganização desapareceram. Isso aponta para um mecanismo físico simples em que o peptídeo carregado positivamente atua como um "Velcro" molecular, reduzindo a repulsão entre filamentos de FtsZ para que possam se agrupar lado a lado em feixes rígidos.
Como um único anel remodela uma vesícula gigante
Dentro das vesículas, esse empacotamento estabilizado pelo peptídeo tem uma consequência marcante. Em vez de muitos anéis curvos pequenos, os feixes de FtsZ endireitados são forçados a seguir a grande curvatura da vesícula, montando-se em um anel contínuo que percorre toda a circunferência. Imagens em lapso de tempo mostraram que sempre que um anel completamente fechado se formava, a vesícula deformava-se de esfera para uma forma de haltere, com uma cintura apertada onde o anel se situava. O processo pôde ser acompanhado em tempo real conforme o diâmetro da vesícula encolhia e a constrição se aprofundava, quase dividindo o compartimento em dois, embora a cisão final não tenha sido alcançada. Os autores propõem que um anel estável de FtsZ atravessando o equador, com turnover mais lento mas ainda ativo, é a arquitetura mínima necessária para conduzir a constrição de membrana em grande escala em uma célula sintética.
O que isso significa para a vida sintética futura
Ao mostrar que uma variante de FtsZ ancorada na membrana mais um peptídeo catiônico curto podem remodelar vesículas lipídicas gigantes quase até a divisão, este trabalho define uma regra de projeto clara para células artificiais: um único anel proteico coerente que corresponda ao tamanho da célula e seja mecanicamente estável ao longo do tempo é suficiente para beliscar uma fronteira macia na escala celular. Fatores mais complexos podem ainda ser necessários para cortar a membrana completamente, mas o estudo demonstra que a constrição controlada em grande escala não exige todo o elenco de proteínas de divisão bacterianas. Em vez disso, o ajuste cuidadoso da organização e da dinâmica dos filamentos pode transformar um andaime proteico simples em um anel contrátil eficaz, aproximando um passo a mais as células sintéticas verdadeiramente autônomas que se dividem.
Citação: Panevska, A., Šakanović, A., Paccione, G. et al. Optimizing spatial organization of FtsZ rings for large-scale constriction in synthetic cells. Nat Commun 17, 2320 (2026). https://doi.org/10.1038/s41467-026-70091-1
Palavras-chave: divisão de células sintéticas, anel de FtsZ, constrição de membrana, divisoma minimal, auto-organização do citoesqueleto