Clear Sky Science · pt
Proteômica subcelular revela um plano para a integração de endossimbiontes em Angomonas deanei, um tripanossomatídeo
Parceiros ocultos dentro da vida unicelular
Muitos organismos unicelulares não estão realmente sozinhos. Alguns abrigam bactérias que vivem dentro deles como inquilinos permanentes, trocando alimento e serviços em relações que ecoam a origem de nossas próprias mitocôndrias. Este estudo explora tal parceria em Angomonas deanei, um parasita microscópico de insetos, para revelar como uma bactéria antes livre se tornou profundamente entrelaçada com as funções internas da célula hospedeira.
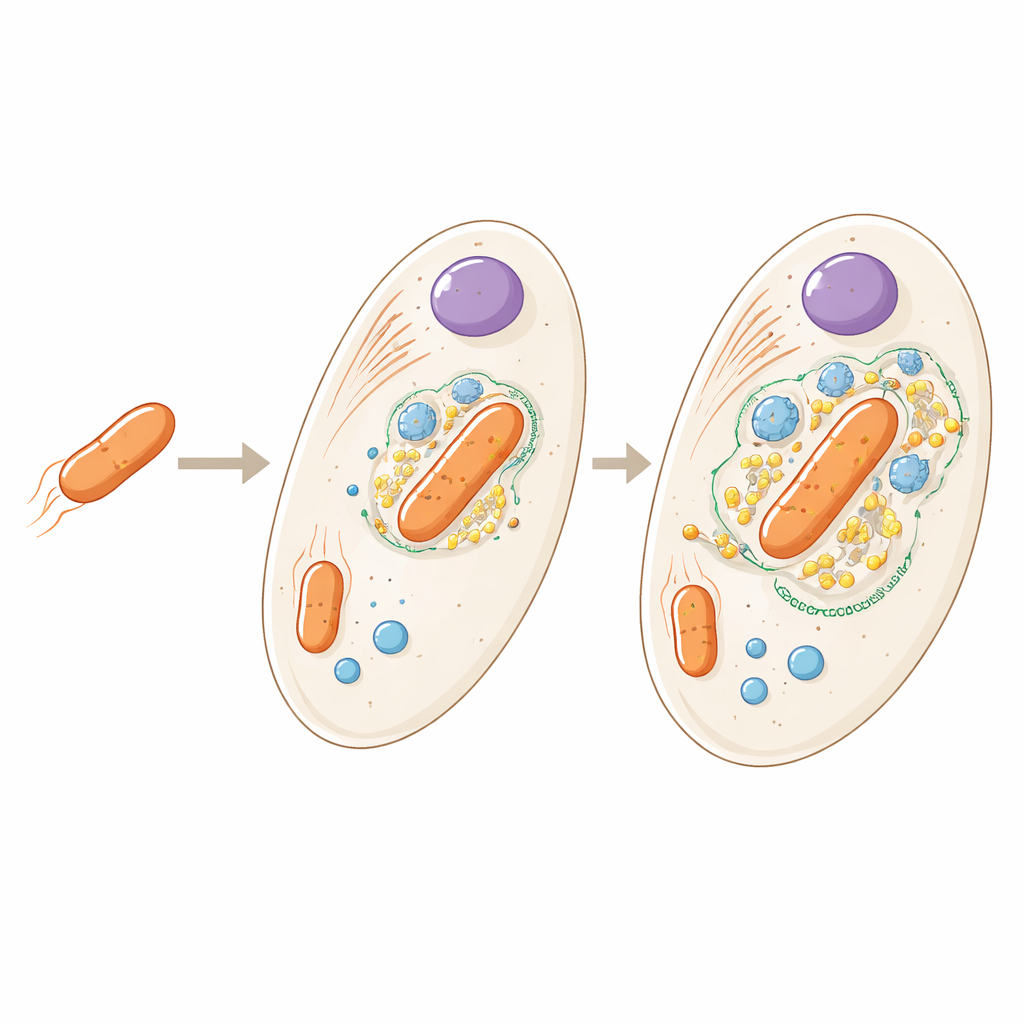
De hóspede a peça incorporada
A bactéria que vive dentro de Angomonas deanei é parente distante de microrganismos do solo que vivem livremente, mas aqui existe em cópia única por célula hospedeira e já não consegue sobreviver por conta própria. Trabalhos anteriores mostraram que o hospedeiro produz proteínas especiais que viajam para dentro da bactéria e até ajudam a controlar quando ela se divide. O novo estudo faz uma pergunta mais ampla: se examinarmos toda a célula, onde exatamente estão localizadas todas as proteínas do hospedeiro e da bactéria, e o que isso nos diz sobre o grau de integração entre os dois parceiros?
Mapeando o centro urbano da célula
Para responder, os pesquisadores romperam um grande número de células de forma muito suave, para que as estruturas internas permanecessem em grande parte intactas. Em seguida, separaram esses fragmentos girando-os em diferentes velocidades e identificaram milhares de proteínas em cada fração usando espectrometria de massas de alta resolução. Ao comparar como as proteínas se agrupavam entre as frações e checar com marcadores conhecidos e microscopia fluorescente, eles criaram um “livro de endereços” detalhado da célula, atribuindo quase 3.000 proteínas a 21 regiões distintas, como núcleo, mitocôndria, corpúsculos de armazenamento especializados e o próprio endossimbionte bacteriano.
Ferramentas do hospedeiro direcionadas à bactéria residente
Dentro desse atlas, a equipe descobriu um conjunto de proteínas produzidas pelo hospedeiro que consistentemente viajam com o endossimbionte, ampliando a coleção conhecida de proteínas direcionadas ao endossimbionte. Um exemplo recém-confirmado, chamado ETP10, reveste a bactéria de modo semelhante a uma proteína identificada anteriormente, sugerindo um arcabouço de fatores do hospedeiro envolvendo o parceiro microbiano. Outro pequeno grupo de proteínas compartilhou um comportamento físico incomum com uma proteína do tipo dinamina já conhecida por beliscar a bactéria durante a divisão. Juntos, esses achados apontam para uma maquinaria especializada construída pelo hospedeiro dedicada a posicionar, moldar e reproduzir o endossimbionte dentro da célula.
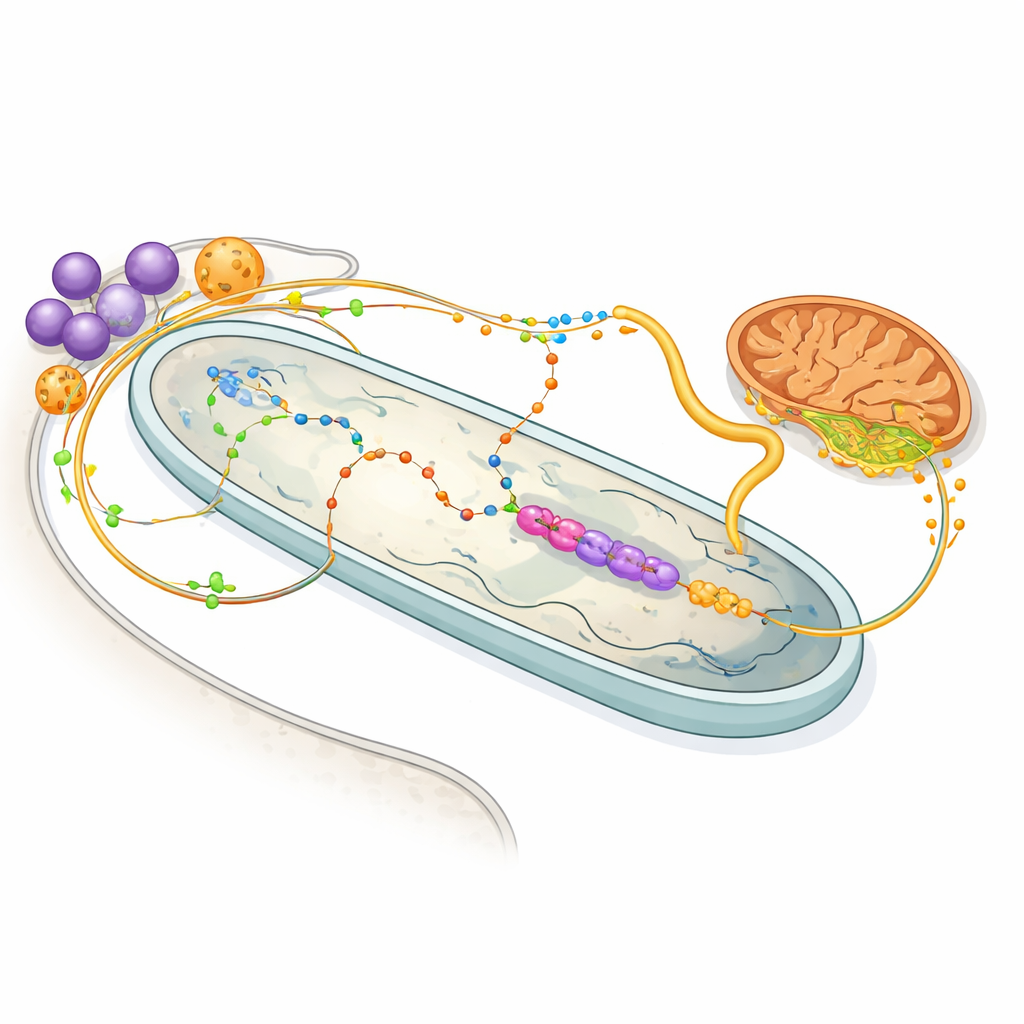
Compartilhamento de energia e rotas químicas de troca
O mapa proteico também ilumina o vibrante comércio de moléculas entre hospedeiro e bactéria. Enzimas nas glicossomas do hospedeiro — organelas que lidam com o metabolismo de açúcares e aminoácidos — parecem ajustadas para alimentar a bactéria com o aminoácido prolina e o composto 2‑oxoglutarato, ambos valiosos como fontes de energia. Dentro da bactéria, um conjunto enxuto de enzimas usa 2‑oxoglutarato para gerar NADH, que alimenta uma cadeia respiratória mínima, e então devolve succinato para a mitocôndria do hospedeiro. Outras vias mostram que a bactéria realiza a maioria das etapas da síntese de heme, um pigmento vital necessário ao hospedeiro, enquanto também contribui com blocos de construção cruciais para nucleotídeos. Em efeito, cada parceiro delegou tarefas metabólicas específicas ao outro, criando um sistema compartilhado e interdependente.
Novas vias de comunicação dentro da célula
Além do metabolismo, o estudo revela ligações físicas e provavelmente sinalizadoras entre o endossimbionte e outras organelas. Um grupo distinto de proteínas do hospedeiro forma o que os autores chamam de cluster de “sítio de contato”, enriquecido em componentes do envelope nuclear e do retículo endoplasmático que co-sedimentam fisicamente com a bactéria. Dois tipos de organelas de armazenamento — glicossomas e acidocalcissomas — aparecem em duas populações: algumas permanecem livres no citoplasma, enquanto outras consistentemente viajam com a bactéria. A microscopia confirma que subgrupos dessas organelas se aninham firmemente contra o endossimbionte. Acidocalcissomas são reservatórios conhecidos de cálcio e fosfato, de modo que sua aproximação sugere uma via bidirecional de sinalização e tráfego iônico conectando a bactéria, essas reservas e o retículo endoplasmático próximo.
Um projeto para a vida fundida dentro da vida
Em conjunto, este trabalho fornece um rico plano, em escala celular, de como uma bactéria pode tornar-se funcionalmente fundida ao seu hospedeiro sem (ainda) se transformar em uma organela completa como as mitocôndrias. Angomonas deanei depende do seu endossimbionte para nutrientes-chave, enquanto a bactéria, por sua vez, depende de proteínas produzidas pelo hospedeiro e de moléculas ricas em energia, além de estar ligada a organelas do hospedeiro para comunicação e controle. Para não especialistas, a conclusão é que a evolução pode gradualmente consolidar a cooperação entre formas de vida muito diferentes, passo a passo, até que separá-las se torne impossível. Este sistema oferece um instantâneo vivo desse processo em ação, ajudando os cientistas a entender melhor como células complexas como as nossas emergiram de começos mais simples.
Citação: Hammond, M., Chmelová, Ľ., van Geelen-Kuenzel, N.A. et al. Subcellular proteomics reveals a blueprint for endosymbiont integration in trypanosomatid Angomonas deanei. Nat Commun 17, 2241 (2026). https://doi.org/10.1038/s41467-026-70084-0
Palavras-chave: endossimbiose, metabolismo celular, evolução de organelas, biologia de protistas, interações hospedeiro-microrganismo