Clear Sky Science · pt
O estilo de vida de Acinetobacter baumannii inclui colonização do solo de material vegetal em decomposição e disseminação pelo ar
Por que o lado selvagem desse germe hospitalar importa para você
Acinetobacter baumannii é mais conhecido como um germe hospitalar difícil de eliminar que resiste a muitos antibióticos. Este estudo mostra que o mesmo microrganismo também vive uma vida rica ao ar livre — no solo, em plantas em decomposição, em animais e até no ar. Ao revelar de onde ele vem e como se desloca, o trabalho ajuda a explicar por que essa bactéria é tão resistente e por que ela reaparece repetidamente em hospitais ao redor do mundo.

Vida oculta em campos, rios e ninhos de aves
Os pesquisadores partiram de uma pista inesperada: filhotes de cegonha-branca na Polônia frequentemente carregavam A. baumannii nas vias aéreas superiores, longe de qualquer hospital. Ao seguir a dieta e o ambiente das aves, a equipe rastreou a bactéria não até insetos ou peixes, mas principalmente até pequenos mamíferos, minhocas e — mais importante — solos úmidos ricos em matéria vegetal em decomposição ao longo de rios e em pilhas de compostagem. Solos florestais, mesmo às margens de riachos, raramente abrigavam a bactéria, enquanto margens de rios fora de áreas florestadas às vezes atuavam como “pontos quentes” onde muitas linhagens diferentes coexistiam lado a lado.
Das plantas em decomposição ao ar livre
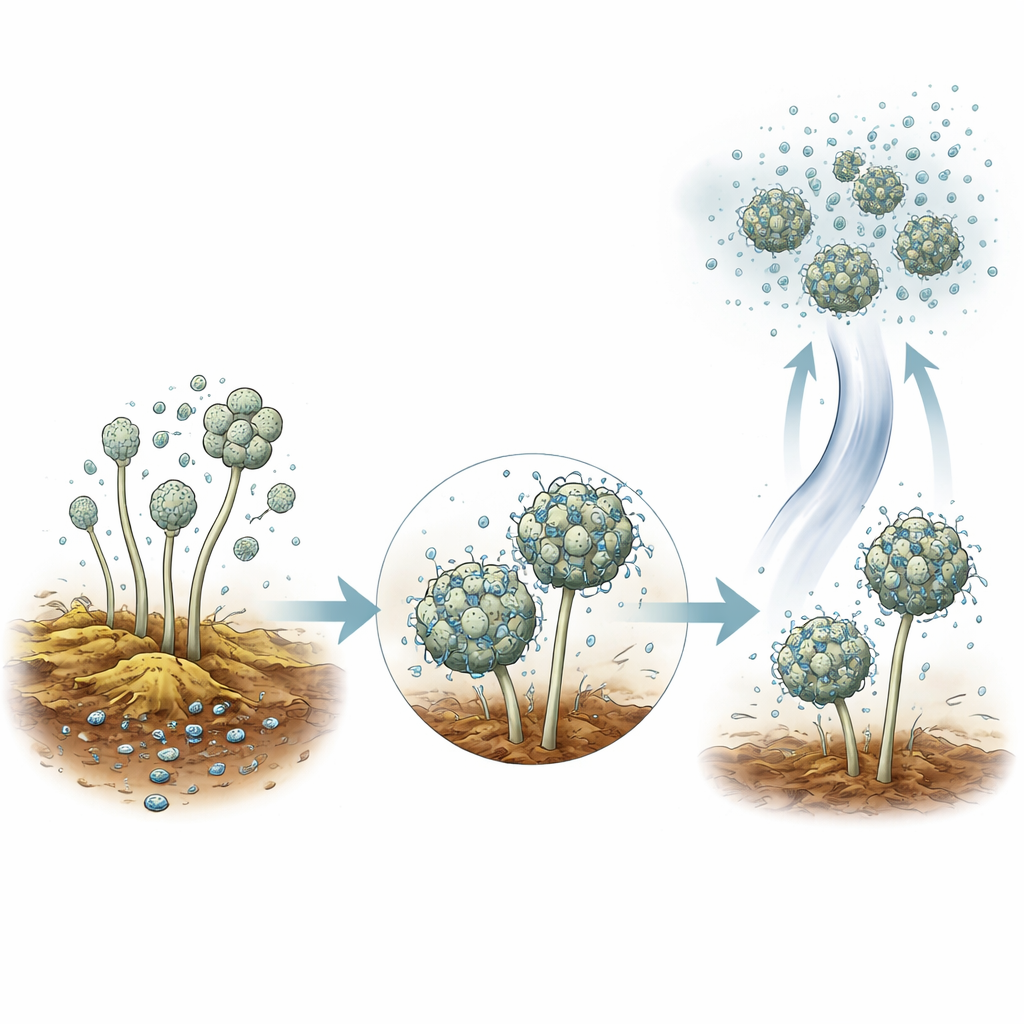
Experimentos de campo cuidadosos mostraram que A. baumannii é atraída por material vegetal em decomposição. Quando os autores colocaram restos de plantas esterilizados em jardins, o material foi colonizado em poucas semanas — mesmo quando foi elevado acima do solo e acessível apenas pelo ar. Armadilhas de ar colocadas logo acima de pilhas de composto ativas também coletaram a bactéria. Em trabalho de laboratório, a equipe descobriu que A. baumannii adere facilmente a esporos de fungos comuns como Aspergillus e Penicillium. As bactérias gradualmente revestiam os esporos e até retardavam sua capacidade de germinar. Como os esporos fúngicos se tornam facilmente aerossóis a partir do composto e dos solos, essa parceria próxima oferece um modo simples para a bactéria pegar carona na atmosfera.
Viajantes globais com raízes antigas
Para ver como essas linhagens selvagens se relacionam com as linhagens hospitalares, a equipe sequenciou 401 novos genomas de cegonhas, solo, plantas, minhocas, roedores e outras fontes, e os comparou com centenas de genomas disponíveis publicamente. A árvore genealógica resultante revelou uma dispersão notável: isolados ambientais, de animais e clínicos humanos estavam distribuídos pelos mesmos ramos, frequentemente diferindo por apenas algumas alterações no DNA. Alguns parentes quase idênticos foram encontrados em diferentes continentes, o que implica que as mesmas linhagens cruzaram oceanos em apenas algumas décadas. Com base na taxa de acúmulo de mutações, os autores estimam que A. baumannii como espécie é surpreendentemente jovem — na ordem de 15.000 anos — e passou por rápida diversificação por volta do período em que os humanos começaram a praticar agricultura em grande escala e a desmatar florestas.
Um vasto arsenal genético, mas pouca marca humana na natureza
Ao combinar todos os genomas, os pesquisadores estimaram que o conjunto gênico combinado da espécie — ou pangenoma — contém cerca de 51.000 famílias gênicas distintas, mais do que o dobro das estimativas anteriores. Essa enorme caixa de ferramentas genética provavelmente sustenta sua capacidade de se adaptar a secura extrema, radiação, desinfetantes e antibióticos. Ainda assim, a maioria dos isolados de vida selvagem e de solo carregava apenas um pequeno número de genes de resistência reconhecidos e poucos elementos de DNA móveis, em contraste com as linhagens hospitalares repletas desses recursos. Esse padrão sugere que as populações naturais amostradas ainda estão relativamente pouco impactadas pelo uso moderno de antibióticos, oferecendo uma visão de “linha de base” da espécie antes da adaptação completa ao ambiente hospitalar.
O que isso significa para hospitais e saúde pública
O estudo descreve A. baumannii não como um problema puramente criado pelo homem, mas como uma bactéria naturalmente aerotransportada, associada a plantas e solo, que só recentemente começou a explorar hospitais e instalações pecuárias como novos habitats. Sua parceria com fungos, tolerância a condições adversas e vasta diversidade genética a tornam bem adaptada para viagens atmosféricas de longa distância e evolução rápida. Para o público em geral, a conclusão é que o controle de infecções não pode focar apenas na transmissão entre pacientes dentro dos hospitais. Picos sazonais, ambientes internos contaminados por bolores, instalações de compostagem e mudanças mais amplas no uso da terra moldam quando e como esse germe resiliente entra em ambientes humanos — e entender seu estilo de vida ao ar livre é fundamental para se antecipar a futuras linhagens resistentes a medicamentos.
Citação: Wilharm, G., Skiebe, E., Michalska, A. et al. Acinetobacter baumannii’s lifestyle includes soil-dwelling colonization of decaying plant material and airborne spread. Nat Commun 17, 2316 (2026). https://doi.org/10.1038/s41467-026-70072-4
Palavras-chave: Acinetobacter baumannii, bactérias aerotransportadas, microbioma do solo, resistência a antibióticos, One Health