Clear Sky Science · pt
A distribuição dinâmica de ampliações em tandem genéticas em uma população heterorresistente de Escherichia coli revelada por sequenciamento de leituras longas ultra-profundo
Bolsões ocultos de sobrevivência
Quando médicos tratam infecções bacterianas com antibióticos, presumem que todo o conjunto de micróbios reagirá da mesma forma. Mas, às vezes, uma fração minúscula da população resiste silenciosamente, sobrevive ao tratamento e prepara o terreno para falha ou recidiva. Este estudo revela como esses raros sobreviventes surgem e mudam ao longo do tempo em Escherichia coli, e apresenta uma forma poderosa de acompanhar essas mudanças genéticas desdobrando-se célula a célula.
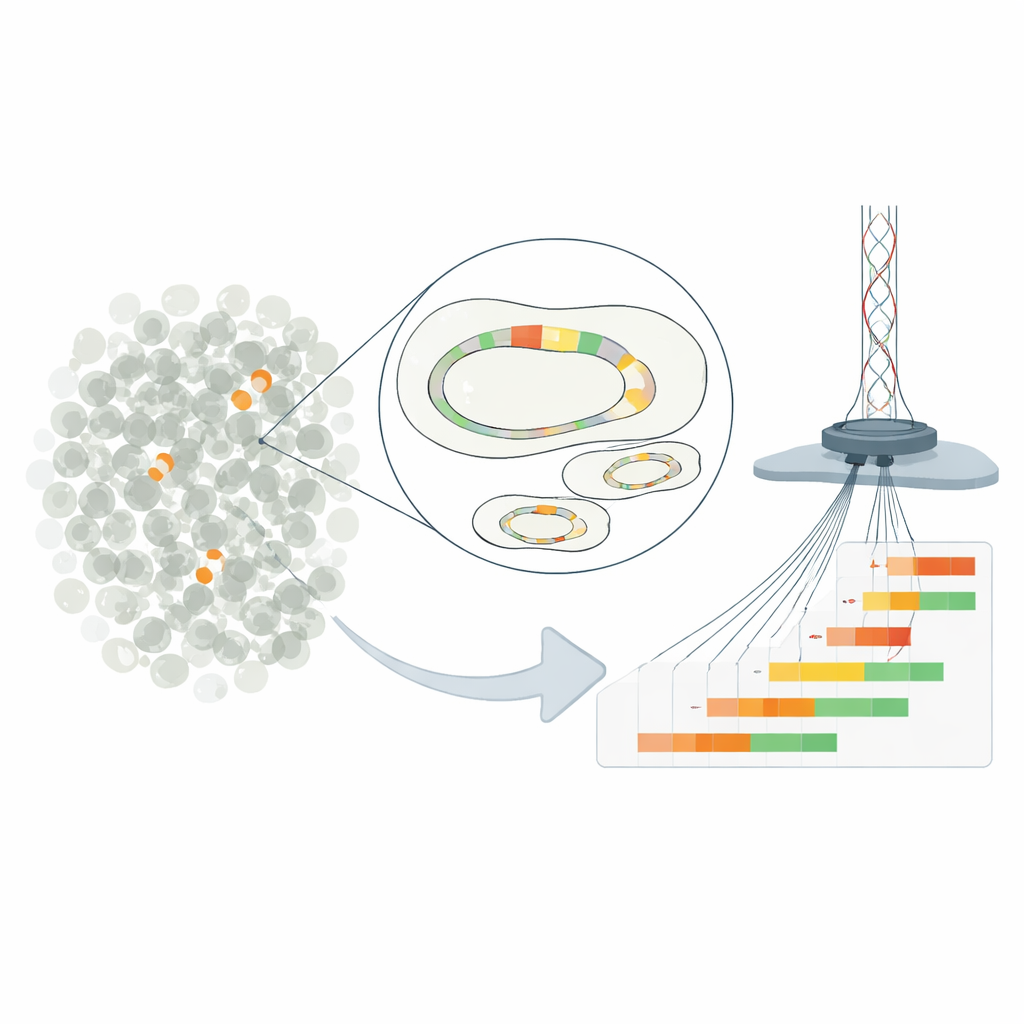
Pequenos repetições genéticas, grandes consequências
O trabalho concentra-se na “heterorresistência”, uma situação em que a maioria das bactérias em uma amostra parece suscetível a um fármaco, mas uma pequena minoria pode suportar doses muito mais altas. Na linhagem de E. coli estudada, esse comportamento decorre de cópias repetidas de um gene de resistência carregado em um plasmídeo — um pequeno círculo de DNA separado do cromossomo principal. Ao duplicar um segmento curto de DNA que contém um gene de beta-lactamase, as bactérias podem aumentar a produção de uma enzima que degrada o antibiótico piperacilina-tazobactam. Quanto mais repetições uma célula carrega, mais enzima ela produz e maiores suas chances de sobrevivência na presença do fármaco.
Lendo círculos de DNA em detalhe sem precedentes
Métodos tradicionais só conseguem estimar o número médio de cópias gênicas em toda uma população bacteriana, ocultando a rica diversidade entre células individuais. Para superar isso, os pesquisadores modificaram o plasmídeo clínico para que pudesse ser cortado em um ponto preciso e então isolado do resto do genoma. Eles usaram sequenciamento Nanopore de leituras longas ultra-profundo para ler moléculas plasmidiais completas de ponta a ponta, contando exatamente quantas unidades repetidas de resistência cada uma continha. Essa abordagem alcançou resolução de uma célula em 100.000, revelando plasmídeos com zero até mais de uma dúzia de cópias do gene coexistindo na mesma cultura. Verificações com outras técnicas confirmaram que, em média, o novo método reportou números de cópias precisos.
Como os antibióticos remodelam a população
Com essa ferramenta em mãos, a equipe acompanhou o que aconteceu quando expôs culturas de E. coli a doses crescentes de piperacilina-tazobactam e, em seguida, retirou o fármaco. À medida que os níveis de antibiótico aumentaram, a distribuição geral deslocou-se para plasmídeos com mais cópias do gene de resistência, mas células com menos cópias nunca desapareceram completamente. Quando a droga foi retirada e as bactérias foram cultivadas por centenas de gerações, a população apenas gradualmente voltou para números de cópias mais baixos e nunca retornou totalmente ao estado inicial. Testes de crescimento separados mostraram que cada cópia gênica extra conferia um aumento mensurável na tolerância ao fármaco, ligando de forma estreita as distribuições genéticas observadas ao padrão visível de heterorresistência em ensaios laboratoriais padrão.

Proteção dos vizinhos e custos silenciosos
Para explicar por que células de baixa cópia persistiam mesmo sob tratamento intenso, os autores construíram um modelo matemático que combinava crescimento bacteriano, degradação do antibiótico e eventos estocásticos que adicionam ou removem cópias gênicas. As simulações mostraram que a “resistência indireta” desempenha um papel central: células altamente resistentes liberam beta-lactamase suficiente para reduzir a concentração do fármaco no ambiente compartilhado, protegendo incidentalmente vizinhos menos resistentes. Contanto que as cópias extras imponham apenas um pequeno custo de crescimento na ausência do fármaco, esse efeito protetor ajuda a manter uma ampla variação no número de cópias, retardando o retorno a uma população totalmente suscetível. O modelo também mostrou como a adaptação ordinária ao meio de crescimento — mutações não relacionadas que melhoram o crescimento — pode cristalizar estados particulares de número de cópias, tornando algumas subpopulações mais aptas que outras.
Por que isso importa para pacientes e além
Para não especialistas, a mensagem é que uma cultura bacteriana não é um inimigo uniforme: é uma mistura em constante mudança de indivíduos com diferentes capacidades de sobreviver a antibióticos. Ao contar diretamente cópias gênicas em milhares de moléculas de DNA únicas, este estudo liga essa diversidade oculta à resistência relevante para o tratamento de forma quantitativa. Tais insights podem aprimorar o uso do sequenciamento genômico para prever heterorresistência de difícil detecção, ajudar a identificar cepas bacterianas com maior probabilidade de causar falha terapêutica e orientar melhores testes diagnósticos. Como ampliações gênicas em tandem também impulsionam adaptação rápida em vírus, tumores e outros organismos, a mesma estratégia pode ser adaptada muito além de E. coli, oferecendo uma nova janela sobre como trechos repetidos de DNA ajudam a vida a contornar ameaças.
Citação: Jonsson, S., Guliaev, A., Berryhill, B.A. et al. The dynamic distribution of genetic tandem amplifications in a heteroresistant Escherichia coli population revealed by ultra-deep long read sequencing. Nat Commun 17, 2113 (2026). https://doi.org/10.1038/s41467-026-70044-8
Palavras-chave: heterorresistência a antibióticos, amplificação gênica, Escherichia coli, sequenciamento de leitura longa, beta-lactamase