Clear Sky Science · pt
Dinamicamente de molécula única revelam que apenas a ligação de ATP impulsiona a translocação de substrato por um transportador ABC
Por que bombas celulares minúsculas importam
Cada célula do seu corpo depende de máquinas microscópicas que movem moléculas através de membranas, moldando desde a captura de nutrientes até a defesa imune. Uma classe importante dessas máquinas, chamada transportadores ABC, usa o combustível químico da célula, o ATP, para empurrar cargas contra gradientes naturais. Ainda assim, durante décadas os cientistas debateram uma questão básica: o simples ato de ligar o ATP fornece a energia para a etapa de transporte, ou a energia só é liberada quando o ATP é quebrado? Este estudo aproxima-se de um único transportador, molécula por molécula, para dirimir essa controvérsia.
Observando um transportador por vez
Em vez de medir o comportamento combinado de milhões de moléculas, os pesquisadores construíram um sistema que lhes permitiu seguir eventos de transporte individuais em tempo real. Eles se concentraram no TmrAB, um parente bacteriano do transportador humano TAP que carrega peptídeos imunes para exposição a células T citotóxicas. O TmrAB fica em uma membrana e transporta fragmentos curtos de proteína (peptídeos) de um lado para o outro usando ATP. Para visualizar cada passo do transporte, a equipe aprisionou uma única molécula de TmrAB em uma bolha de membrana artificial (um lipossomo) e colocou dentro dessa bolha uma proteína "sensor" especialmente projetada que muda sua fluorescência quando captura um peptídeo. Usando um microscópio altamente sensível, eles puderam então ver, como saltos breves no sinal de luz, os momentos exatos em que um peptídeo após outro chegava dentro da bolha.
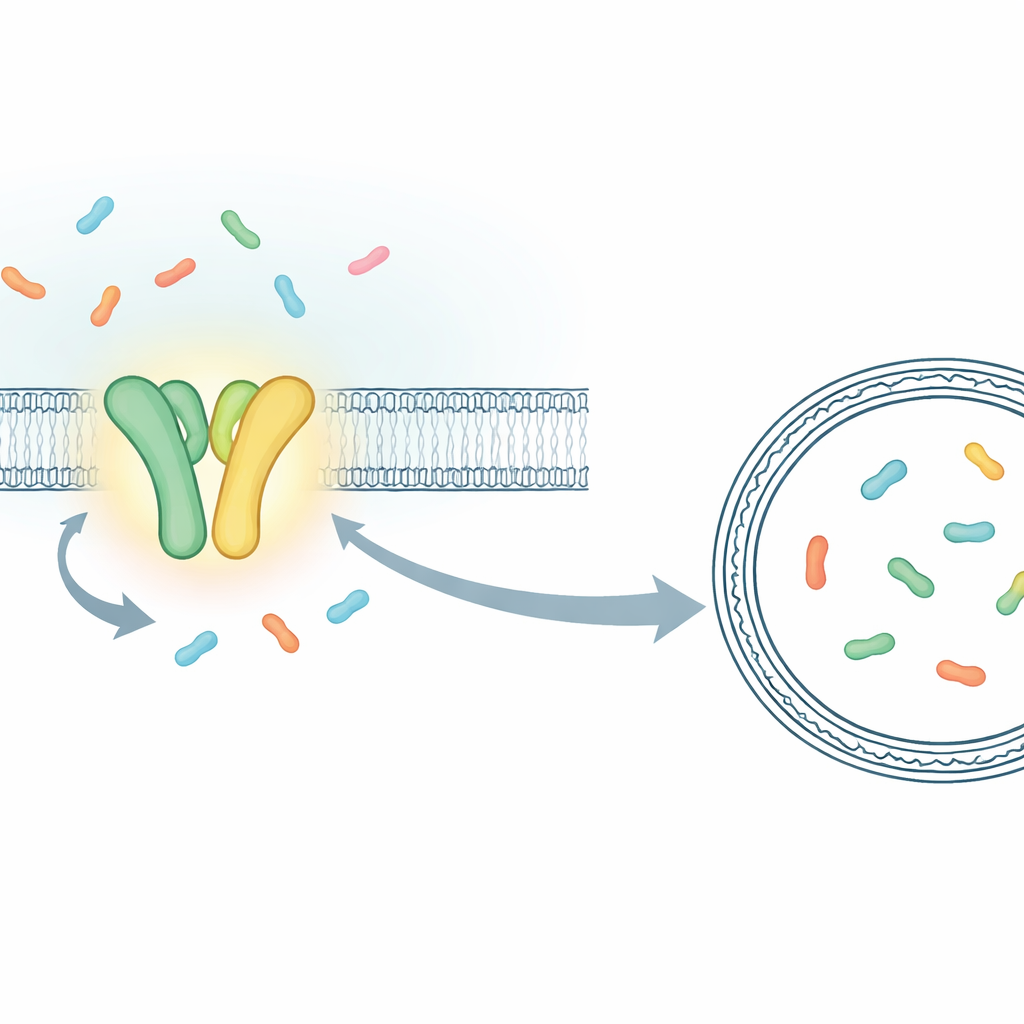
Provando que uma ligação de ATP move um peptídeo
Com esse ensaio de molécula única em mãos, os pesquisadores compararam o TmrAB normal com uma versão modificada de baixa velocidade, cujos ciclos são estendidos no tempo. A variante lenta tornou possível distinguir eventos individuais que de outra forma se misturariam. Eles mostraram que, quando ATP e peptídeos estavam presentes juntos, o sensor dentro do lipossomo passava de seu estado "vazio" para o estado "carregado" em passos discretos, cada um consistente com um único peptídeo sendo transportado. Ao analisar quão rápido o sensor se fechava ao redor dos peptídeos e estimar o volume minúsculo dentro de cada lipossomo, eles puderam até traduzir essas mudanças de luz em concentrações aproximadas de peptídeo. Os números correspondiam ao que se esperaria se um, depois dois peptídeos se acumulassem em bolhas de cerca de 100 nanômetros de diâmetro, confirmando que eles estavam contando eventos de transporte um a um.
A ligação de ATP sozinha aciona o interruptor molecular
A controvérsia central diz respeito aos íons magnésio (Mg2+), que normalmente acompanham o ATP nas células e são conhecidos por ser necessários para a hidrólise eficiente do ATP. Alguns modelos sugeriam que o Mg2+ também poderia ser necessário para o ATP se ligar ou para o transportador se fechar. Para separar esses papéis, os pesquisadores removeram Mg2+ usando um agente quelante, mas ainda forneceram ATP. Nessas condições, tanto o transportador normal quanto o lento puderam realizar exatamente um passo de transporte de peptídeo por molécula, e então pararam. Esse comportamento indica que o ATP ainda pode se ligar e forçar o transportador a alternar de uma conformação voltada para o interior para uma voltada para o exterior e mover um peptídeo, mesmo sem Mg2+. Contudo, sem Mg2+ o transportador não consegue dividir o ATP de forma eficiente e, portanto, não consegue se reiniciar para outra rodada.
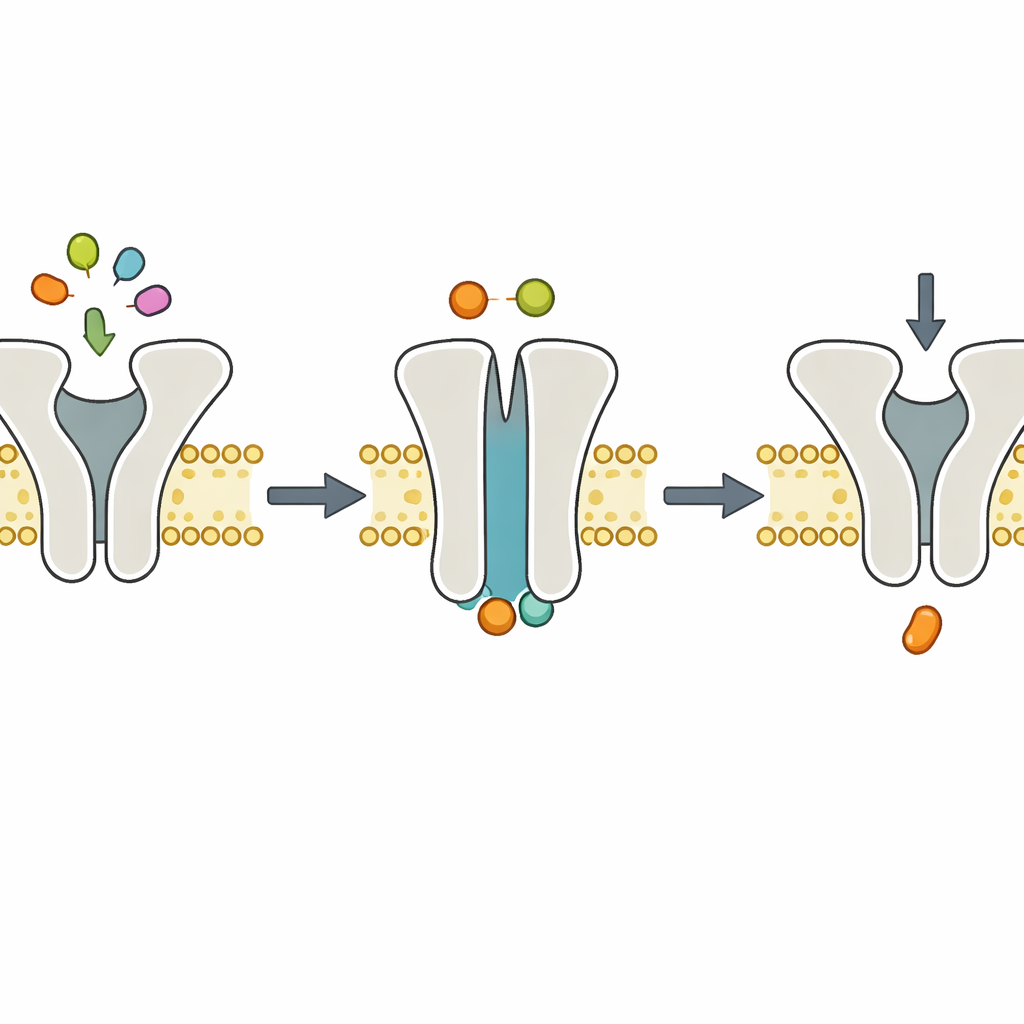
Instantâneos estruturais corroboram a dinâmica
Para ver como a máquina se apresenta durante essa etapa sem Mg2+, a equipe recorreu à crio–microscopia eletrônica, que imagina moléculas congeladas a temperaturas muito baixas com detalhe quase atômico. Eles reconstituíram TmrAB em nanodiscos lipídicos, adicionaram ATP sem Mg2+ e congelaram os complexos. As estruturas resultantes mostraram o TmrAB em uma conformação voltada para fora, "ocluída", com ATP encaixado em ambas as suas cavidades de ligação internas, mas sem Mg2+ visível. Esses instantâneos eram essencialmente indistinguíveis de estruturas anteriores obtidas com ATP e Mg2+ presentes. Juntamente com ensaios bioquímicos que mostraram que a hidrólise do ATP paralisa completamente sem Mg2+, as imagens sustentam uma divisão simples de tarefas: a ligação do ATP aciona a mudança conformacional que move o peptídeo, enquanto a hidrólise do ATP dependente de Mg2+ realiza a etapa de recuperação.
Uma imagem mais clara de como as bombas celulares funcionam
Ao observar transportadores individuais e resolver suas estruturas, este trabalho resolve uma questão de longa data sobre transportadores ABC: o impulso mecânico que move um peptídeo é desencadeado pela própria ligação do ATP, e não pela posterior quebra química do ATP. O Mg2+ entra na história principalmente para permitir que o ATP seja dividido, o que por sua vez reinicia o transportador para que ele possa funcionar novamente. Além de esclarecer um pedaço fundamental da biologia celular, essa abordagem de molécula única oferece um roteiro para dissecar outras máquinas de membrana que sustentam a imunidade, resistência a drogas e muitas doenças — uma molécula e um passo de transporte por vez.
Citação: Nocker, C., Pečak, M., Nocker, T. et al. Single-molecule dynamics reveal ATP binding alone powers substrate translocation by an ABC transporter. Nat Commun 17, 3038 (2026). https://doi.org/10.1038/s41467-026-70021-1
Palavras-chave: Transportadores ABC, Ligação de ATP, FRET de molécula única, Transporte de membrana, TAP e TmrAB