Clear Sky Science · pt
Nanopartículas de azul da Prússia direcionadas a múltiplos PANoptossomos mediadores de PANoptose para terapia da lesão por isquemia-reperfusão miocárdica
Por que proteger o coração em recuperação é importante
Quando uma pessoa tem um ataque cardíaco, os médicos trabalham para reabrir a artéria bloqueada e restaurar o fluxo sanguíneo. Esse passo que salva vidas, no entanto, tem um custo oculto: o retorno súbito de oxigênio pode ferir o coração, matar células e preparar o terreno para insuficiência cardíaca. Este estudo explora uma nanomedicina inventiva que pretende proteger o coração durante essa janela vulnerável, bloqueando várias vias interligadas de morte celular ao mesmo tempo e potencialmente levando a recuperações mais suaves após ataques cardíacos.
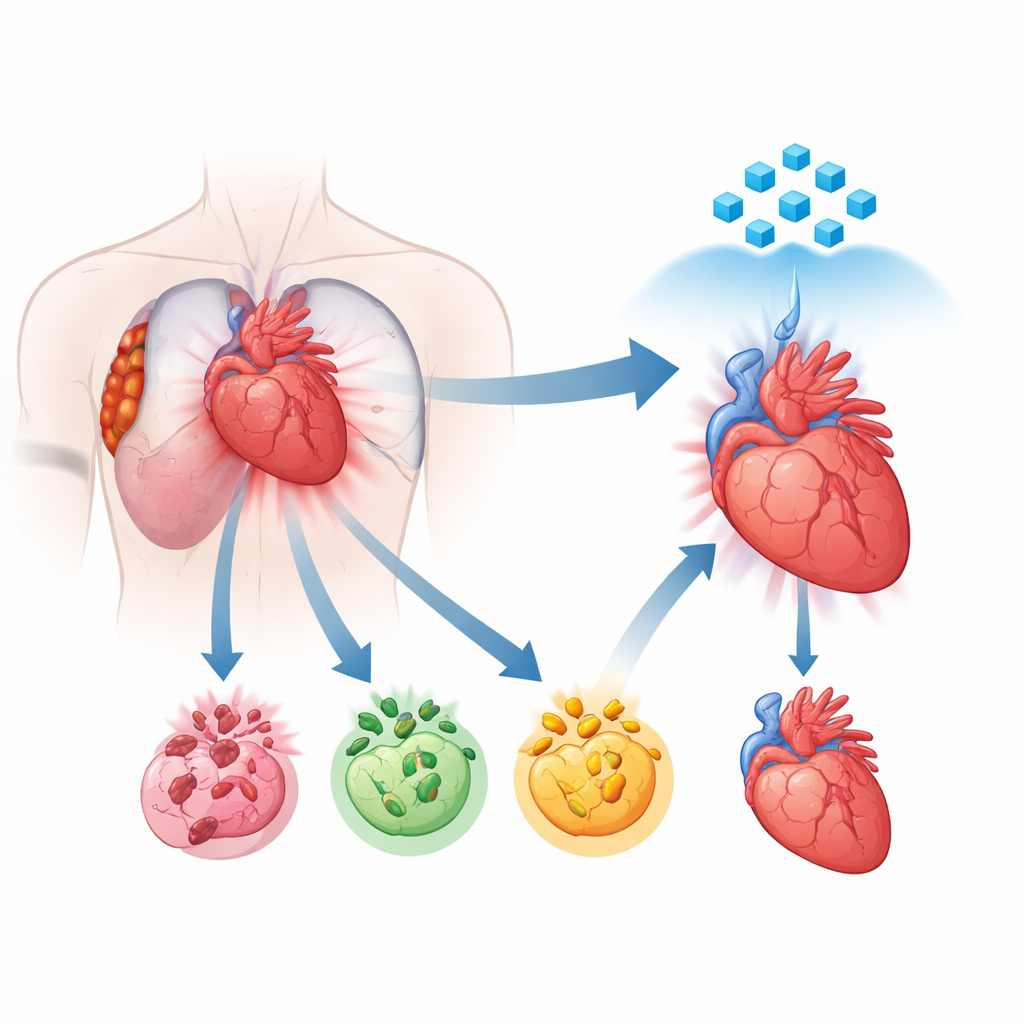
Uma nova visão de como as células cardíacas morrem
Por anos, cientistas souberam que células cardíacas danificadas podem morrer por diferentes rotas programadas, incluindo apoptose, necroptose e piroptose. Cada uma segue seu próprio roteiro molecular, mas evidências crescentes mostram que essas rotas não operam isoladamente. Em vez disso, elas se comunicam e podem se unir em um processo combinado e descontrolado chamado PANoptose. Nesse estado, vários programas de morte são ativados simultaneamente, tornando terapias que bloqueiam apenas uma via frustrantemente fracas. Os autores usaram sequenciamento de RNA de núcleo único em tecido cardíaco humano de pacientes com ataques cardíacos recentes para mapear onde e com que intensidade esses programas de morte estavam ativados. Eles descobriram que, nas regiões mais danificadas, as células do músculo cardíaco apresentavam uma mudança poderosa em direção a esse modo de morte combinado, apontando a PANoptose como um motor central da lesão.
Projetando uma pequena ferramenta multifuncional para o coração lesionado
Para enfrentar um processo tão complexo, a equipe recorreu ao azul da Prússia, um composto médico aprovado há muito tempo, mais conhecido como antídoto para certos envenenamentos por metais. Em escala nanométrica, partículas de azul da Prússia comportam-se como pequenos robôs catalíticos que podem neutralizar moléculas nocivas e influenciar o comportamento celular. Por meio de simulações computacionais, os pesquisadores mostraram que essas nanopartículas poderiam se ligar diretamente a três centros proteicos-chave — RIPK1, ZBP1 e AIM2 — que ajudam a montar a maquinaria molecular da PANoptose. Ao ligar-se a esses centros de diferentes maneiras, as partículas foram previstas para interferir na construção dos complexos indutores de morte que coordenam as três vias de morte celular.
Guiando nanopartículas diretamente ao tecido cardíaco danificado
Nanopartículas só funcionam se chegarem ao lugar certo, então a equipe envolveu as partículas de azul da Prússia em membranas naturais derivadas de plaquetas, as células sanguíneas que se dirigem a vasos lesionados. Esse revestimento criou PB@PM, um transportador biomimético que circula como uma plaqueta, mas entrega uma carga terapêutica. Em camundongos submetidos a um infarto controlado seguido de reabertura da artéria, imagens mostraram que PB@PM se acumulou muito mais fortemente na região cardíaca lesionada do que partículas não revestidas, ao mesmo tempo que evitou em grande parte órgãos saudáveis. Importante, as partículas revestidas foram bem toleradas: exames de sangue e análises de tecidos não revelaram toxicidade óbvia, apoiando seu potencial para desenvolvimento posterior.
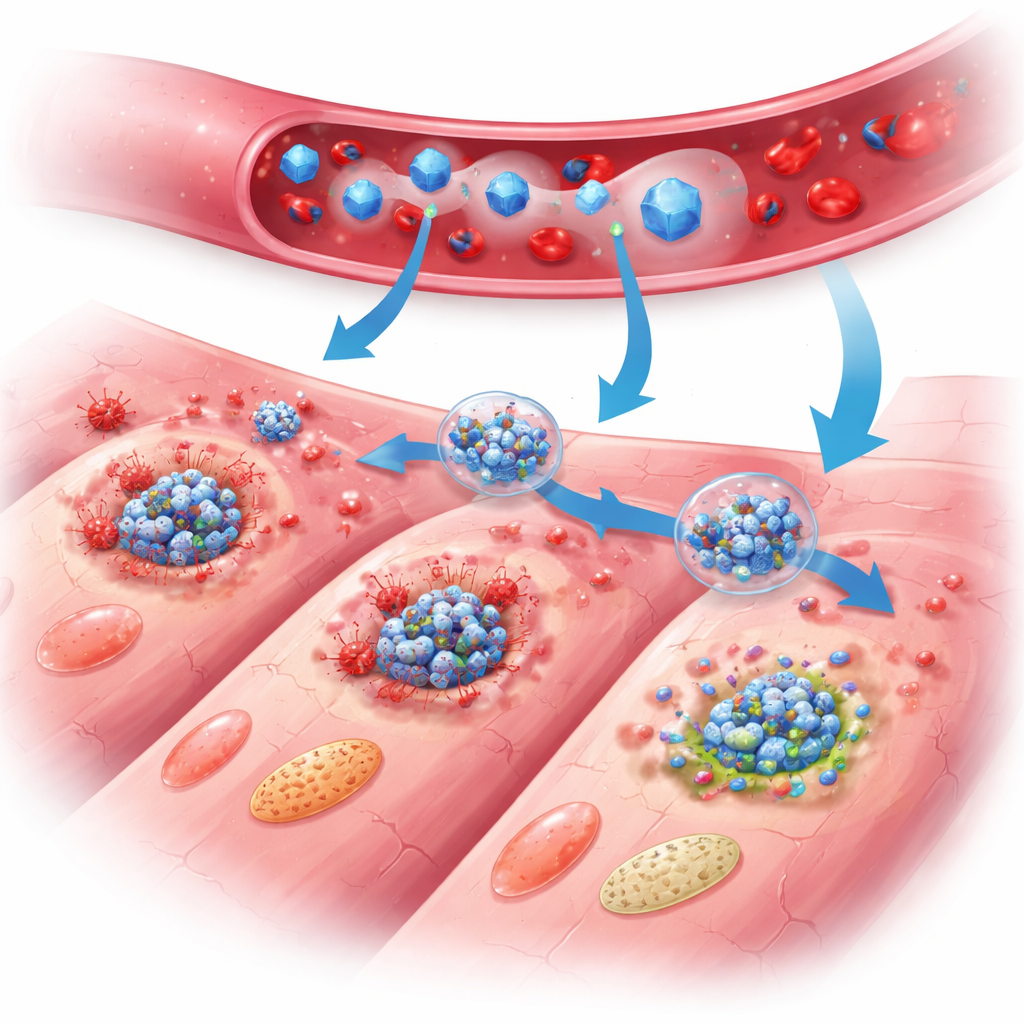
Como o nano-escudo protege o coração
Em camundongos tratados, os benefícios de PB@PM tornaram-se evidentes ao longo de dias e semanas. A função de bombeamento do coração melhorou, o tamanho da cicatriz diminuiu e a parede cardíaca afinou menos em comparação com animais não tratados. Estudos detalhados de tecido revelaram menos células cardíacas morrendo, células inflamatórias mais calmas e tecido de reparo melhor estruturado com crescimento vascular mais saudável e menos aumento anômalo das células sobreviventes. No nível molecular, perfis amplos de expressão gênica e medidas de proteínas mostraram que PB@PM silenciou as três principais vias de morte programada ao mesmo tempo, interrompeu a montagem dos complexos multiproteicos da PANoptose e reduziu os níveis de moléculas sinalizadoras que alimentam a inflamação. As partículas também eliminaram espécies reativas de oxigênio prejudiciais, estabilizaram as mitocôndrias — as usinas de energia da célula — e restauraram um metabolismo energético mais normal, removendo gatilhos chave que de outra forma empurrariam as células para a autodestruição.
O que isso pode significar para o atendimento de ataques cardíacos no futuro
Em termos simples, este trabalho mostra que uma nanopartícula engenhosamente projetada pode agir como um escudo multifacetado para o coração, atenuando um emaranhado de sinais destrutivos de morte em vez de perseguir uma via por vez. Ao se direcionar ao tecido cardíaco lesionado, ligar-se a proteínas de controle centrais e aliviar o estresse oxidativo e inflamatório, PB@PM reduziu drasticamente a reação em cadeia de perda celular e formação de cicatriz que frequentemente segue a reabertura de uma artéria bloqueada. Embora muitos testes ainda sejam necessários antes que essa estratégia possa chegar a pacientes, o estudo oferece uma prova de conceito de que direcionar a PANoptose como um todo — e fazê-lo com partículas inteligentes e inspiradas biologicamente — pode abrir um novo capítulo na proteção do coração após um ataque cardíaco.
Citação: Xu, L., Jiang, L., Wu, R. et al. Prussian blue nanoparticles targeting multiple PANoptosome-mediated PANoptosis for myocardial ischemia-reperfusion injury therapy. Nat Commun 17, 2329 (2026). https://doi.org/10.1038/s41467-026-70012-2
Palavras-chave: isquemia-reperfusão miocárdica, terapia com nanopartículas, morte celular programada, inflamação cardíaca, proteção mitocondrial