Clear Sky Science · pt
RPA estimula diretamente a processividade da helicase Mer3 para garantir a formação normal de crossovers na meiose
Como as células embaralham o DNA para produzir óvulos e espermatozoides saudáveis
Cada vez que uma planta, animal ou humano produz óvulos ou espermatozoides, suas células precisam reorganizar os cromossomos para que cada descendente receba uma combinação nova de DNA parental. Esse rearranjo genético depende de trocas de DNA cuidadosamente posicionadas, ou crossovers, entre pares de cromossomos. O estudo em destaque desvenda como duas proteínas-chave, Mer3 e RPA, atuam em conjunto como uma máquina microscópica para garantir que esses crossovers se formem de maneira eficiente e segura — um processo com implicações para a fertilidade, a evolução e possivelmente até o câncer.
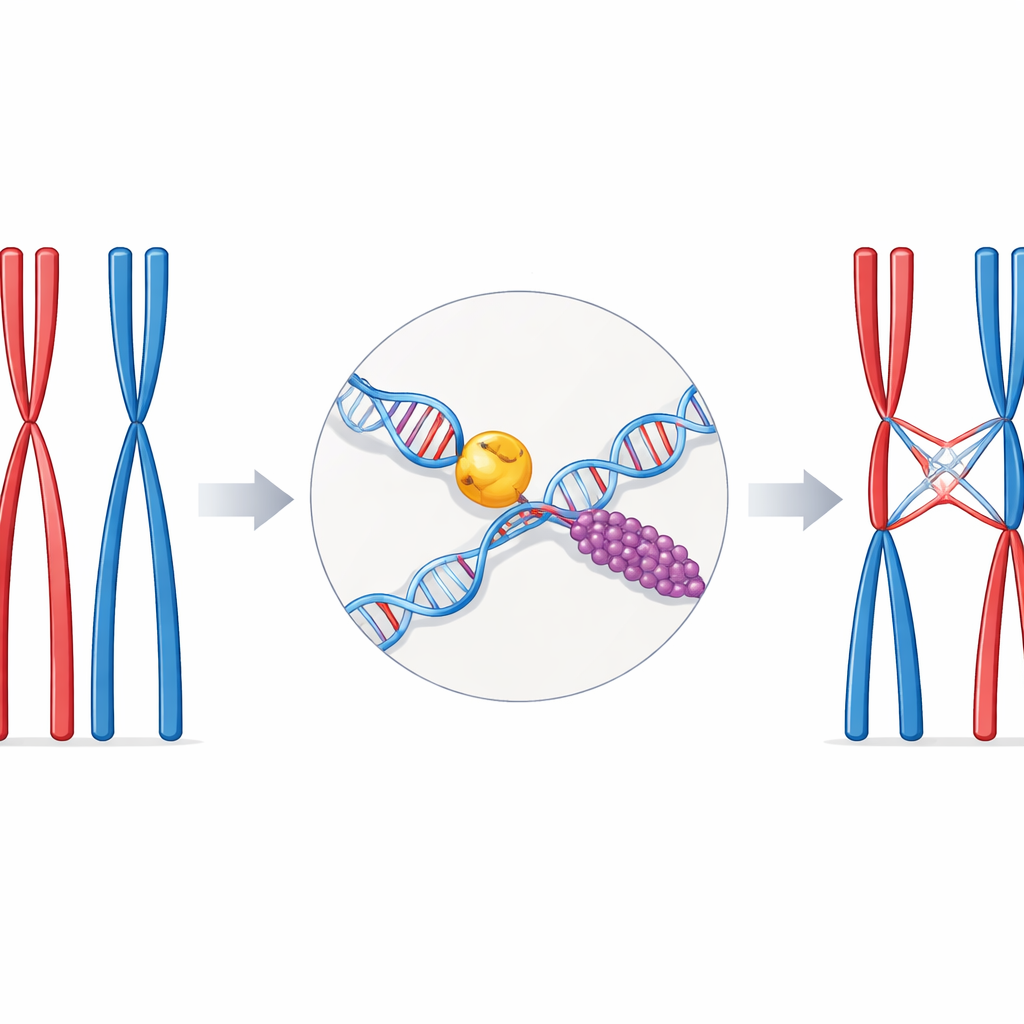
Um equilíbrio delicado na reprodução sexual
Durante a divisão celular especial chamada meiose, os cromossomos aparecem em pares correspondentes, um de cada progenitor. Para que esses pares se separem corretamente, eles devem ficar fisicamente ligados em alguns pontos bem escolhidos ao longo de seu comprimento. Essas ligações são os crossovers — trechos onde as fitas de DNA de um cromossomo são trocadas pelas do seu parceiro. Ter poucos crossovers aumenta o risco de má segregação cromossômica e infertilidade; ter muitos ou posicionados de forma inadequada pode danificar o genoma. As células, portanto, dependem de vias especializadas de reparo e proteínas auxiliares para transformar uma quebra perigosa de DNA em um crossover controlado.
Conheça Mer3 e RPA, uma dupla que desembrulha DNA
Os pesquisadores concentraram-se em Mer3, um motor molecular que desenrola DNA e promove a formação de crossovers. O equivalente humano, HFM1, é conhecido por ser importante para a fertilidade. Eles descobriram que Mer3 se liga diretamente à RPA, um complexo proteico que normalmente reveste o DNA de fita simples exposto para protegê‑lo e recrutar outros fatores de reparo. Usando testes bioquímicos, modelagem estrutural e ensaios de interação, a equipe mapeou um sítio específico de encaixe onde uma cauda curta de Mer3 se ajusta a um sulco em uma subunidade da RPA. Essa interface é conservada de leveduras a mamíferos, sugerindo ser uma solução evolutiva antiga reutilizada para controlar o reparo do DNA durante a meiose.
Observando um motor de DNA individual em ação
Para ver o que essa parceria realmente faz, os cientistas usaram pinças magnéticas de molécula única — um instrumento que segura um hairpin de DNA como uma pequena mola e mede como uma única molécula de Mer3 o desenrola ao longo do tempo. Eles descobriram que Mer3 se locomove ao longo do DNA a uma velocidade constante mesmo sozinho. Mas em condições que imitam a tensão física relativamente baixa dentro das células, Mer3 tende a descolar do DNA após desenrolar apenas um trecho curto. Quando uma pequena quantidade de RPA está presente, Mer3 torna‑se subitamente muito mais persistente: ele pode desenrolar trechos de DNA muito mais longos sem se desprender, especialmente quando o DNA tende a dobrar sobre si mesmo. Uma versão mutante de Mer3 projetada para interromper a cauda que se liga à RPA não ganha esse poder de permanência extra, revelando que o contato direto com a RPA é o que aumenta a processividade de Mer3.
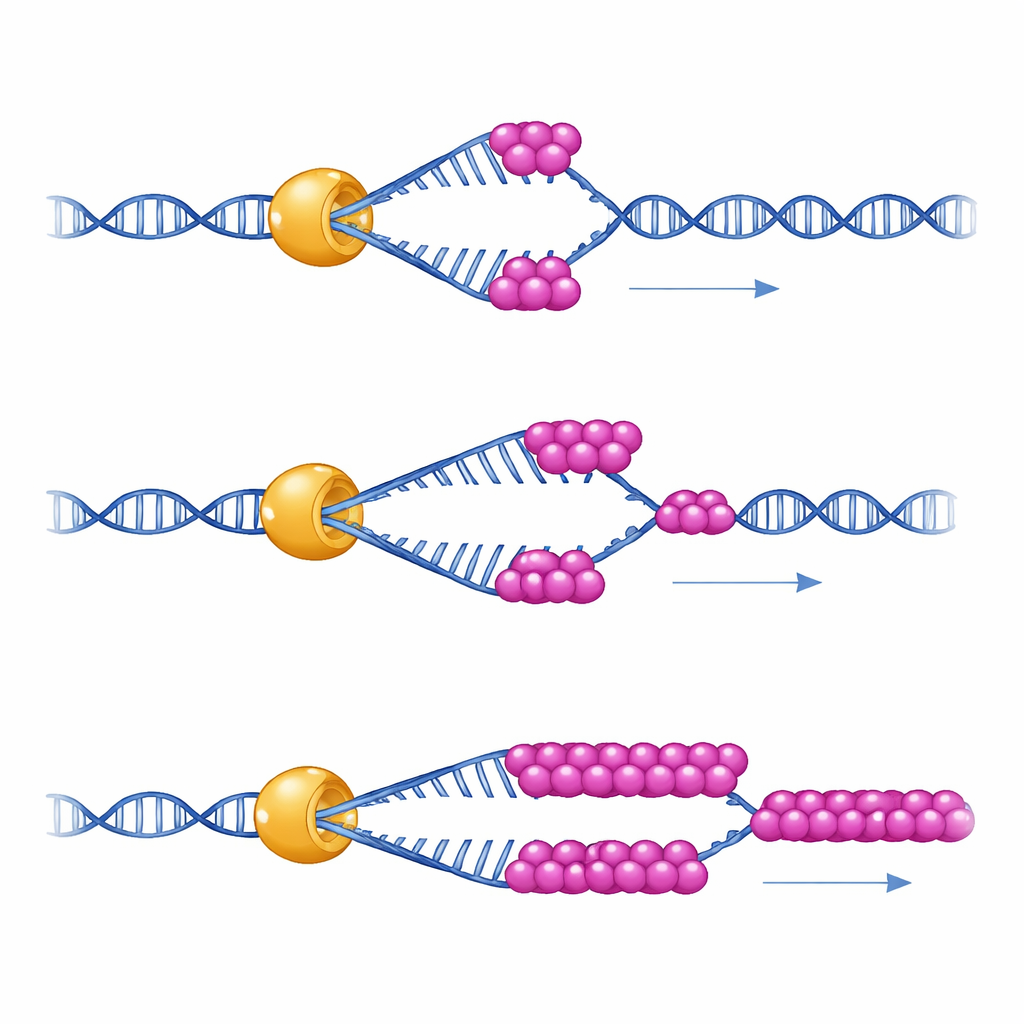
Consequências para os crossovers em células vivas
A equipe então perguntou o que acontece em células reais de levedura quando Mer3 não consegue se ligar bem à RPA. Eles substituiram o gene MER3 normal pelo mutante que não se liga à RPA e monitoraram a meiose. Essas células ainda conseguiam se dividir e formar esporos, mas sua fertilidade caiu e o número total de crossovers em certas regiões cromossômicas diminuiu. Análises detalhadas do DNA mostraram mais eventos de reparo terminando como non‑crossovers e um acúmulo de intermediários de recombinação não resolvidos. O mapeamento genômico da localização de Mer3 revelou que a proteína mutante era recrutada de forma menos estável nos locais onde ocorrem quebras de DNA programadas, embora sua associação inicial aos eixos cromossômicos parecesse normal. Em outras palavras, sem uma ligação forte à RPA, Mer3 não permanece tempo suficiente nos sítios de quebra para conduzi‑los de forma confiável a resultados de crossover.
O que isso significa para fertilidade e estabilidade do genoma
Em conjunto, o estudo mostra que a RPA faz mais do que simplesmente revestir o DNA exposto; ela ajusta diretamente o comportamento de uma helicase meiótica crucial. Ao se acoplar à RPA, Mer3 torna‑se um desembrulhador de DNA mais determinado, capaz de estender e estabilizar as estruturas conjuntas de DNA que amadurecem em crossovers. Quando essa interação é enfraquecida, as células migram para caminhos de reparo mais seguros, porém menos úteis, e deixam mais intermediários sem resolver, comprometendo sutilmente a segregação cromossômica. Como os mesmos componentes moleculares existem em humanos — e mutações em HFM1 estão ligadas à infertilidade — este trabalho fornece um quadro mecanicista de como pequenas mudanças em uma interface proteica podem repercutir na saúde reprodutiva e na diversidade genética das gerações futuras.
Citação: Altmannova, V., Orlić, L., Carrasco, C. et al. RPA directly stimulates Mer3 helicase processivity to ensure normal crossover formation in meiosis. Nat Commun 17, 2621 (2026). https://doi.org/10.1038/s41467-026-69985-x
Palavras-chave: meiose, recombinação genética, helicase de DNA, fertilidade, crossing-over cromossômico