Clear Sky Science · pt
Desregulação da resposta ao dano no DNA por oligonucleotídeos antissenso fosfotiolados
Quando terapias genéticas úteis confundem a equipe de reparo da célula
Oligonucleotídeos antissenso, ou ASOs, são uma classe emergente de medicamentos de precisão projetados para ligar ou desligar genes individuais. Eles já são usados para tratar algumas doenças genéticas raras e estão sendo testados para muitas outras. Este estudo revela uma desvantagem inesperada de um ajuste químico comum usado para tornar esses fármacos mais estáveis: nas condições certas, ele pode enganar a célula fazendo‑a acreditar que o DNA está danificado, travando a maquinaria de reparo e colocando em risco a integridade do genoma a longo prazo.
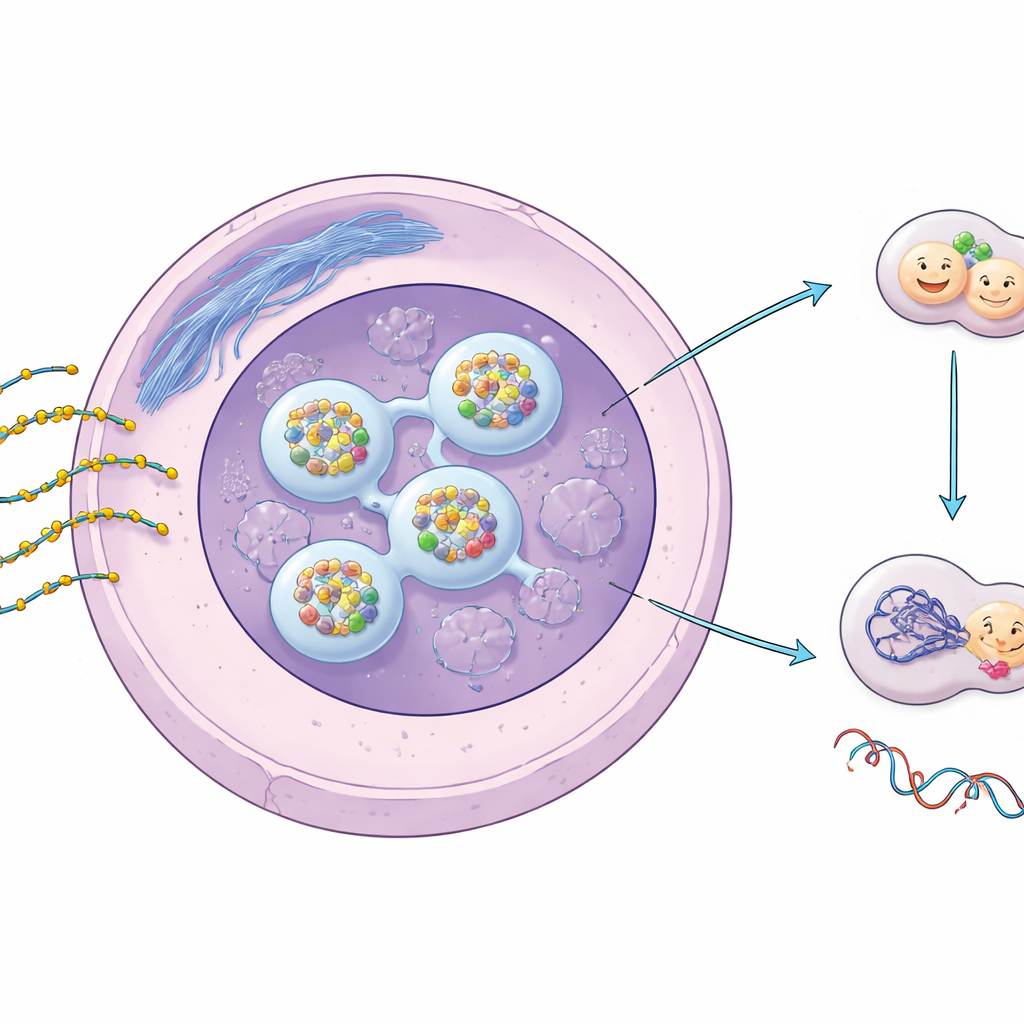
Interruptores gênicos desenhados e sua melhoria química
Os ASOs são fitas curtas e simples de material genético construídas para reconhecer e ligar‑se a mensagens de RNA específicas dentro de nossas células, silenciando‑as ou alterando‑as. Para sobreviver no organismo e entrar eficientemente nas células, a maioria dos ASOs terapêuticos carrega uma modificação fosfotiolada (PS), na qual um átomo de enxofre substitui um átomo de oxigênio na espinha dorsal da fita. Essa pequena mudança aumenta dramaticamente sua estabilidade e sua tendência a interagir com proteínas. Trabalhos anteriores mostraram que PS‑ASOs se agrupam em pontos distintos no núcleo celular e podem estressar certas estruturas nucleares, mas o que isso significava para a reparação do DNA e a segurança a longo prazo permanecia incerto.
Gotas artificiais que imitam locais reais de reparo do DNA
Os autores acompanharam PS‑ASOs marcados com fluorescência em células humanas e descobriram que, nas doses experimentais comumente usadas, eles se acumulam rapidamente no núcleo e semeiam novas estruturas esféricas chamadas corpos PS. Esses corpos se formam de maneira dependente da concentração e comportam‑se como gotas líquidas que se fundem, se dissolvem e dependem de forças moleculares fracas — características típicas da separação de fase líquido–líquido. Crucialmente, elas não estão localizadas onde ocorrem quebras reais do DNA e não contêm os marcadores usuais de DNA rompido. Em vez disso, o estudo mostra que enzimas-chave de reparo do DNA — incluindo DNA‑PKcs, ATM, ATR e PARP1 — ligam‑se diretamente aos PS‑ASOs e ficam altamente enriquecidas dentro dessas gotas artificiais, apesar do DNA subjacente estar intacto.
Alarmes falsos que ativam os sinais de dano da célula
Uma vez montadas, as gotas semeadas por ASOs fazem mais do que aprisionar proteínas passivamente: elas ativam as enzimas de reparo. Dentro de uma hora após a entrada dos ASOs, as enzimas nessas gotas são ativadas e começam a modificar a cromatina próxima, decorando proteínas histonas com marcas químicas normalmente vistas após danos genuínos ao DNA. Isso dispara a resposta completa ao dano no DNA — recrutando fatores adicionais de reparo, ligando a sinalização de pontos de checagem e reduzindo a atividade de motores do ciclo celular chamados CDKs. Como resultado, as células desaceleram ou interrompem sua progressão por fases chave do ciclo celular, particularmente no ponto em que normalmente verificam se o DNA está íntegro antes de se dividir. Em cérebros de camundongos expostos a uma entrega de ASO com relevância clínica, os pesquisadores também observaram aumento da sinalização de dano no DNA em regiões com maior captação de ASO, indicando que esses efeitos não se limitam a culturas celulares.
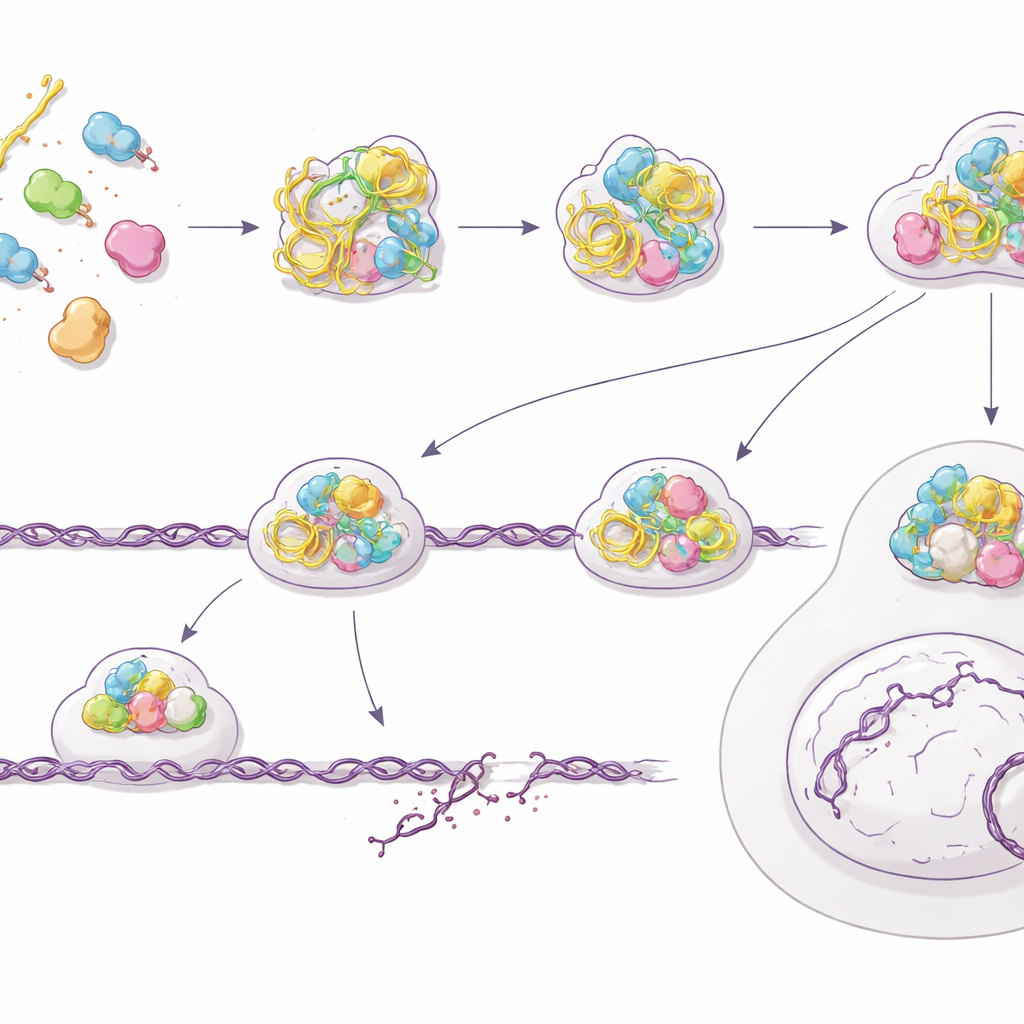
Reparo falho e aumento das quebras de DNA
Paradoxalmente, enquanto o sistema de alarme da célula dispara, sua capacidade real de consertar quebras perigosas no DNA piora. A equipe demonstrou que células pré‑tratadas com PS‑ASOs têm dificuldade para eliminar danos após irradiação e até acumulam mais quebras espontâneas, medidas por ensaios cometa e por focos de reparo persistentes. Um exame mais atento de uma das vias de reparo mais precisas da célula — a recombinação homóloga — revelou o problema: componentes essenciais como BRCA2 e RAD51 deixam de se montar corretamente nas extremidades do DNA quebrado, enquanto marcadores iniciais de processamento nessas extremidades ainda aparecem. Usando um sistema repórter genético, os autores quantificaram uma queda de aproximadamente 60% na eficiência da recombinação homóloga após exposição a PS‑ASOs. As células tornam‑se menos viáveis no geral e marcadamente mais sensíveis à radiação, consistente com um sistema de reparo que é sinalizado mas não implantado corretamente.
O que isso significa para o futuro dos fármacos que visam genes
Em conjunto, o estudo sugere que ASOs modificados por PS podem nucleear gotas líquidas artificiais no núcleo que concentram e ativam enzimas de reparo do DNA mesmo quando não há dano a ser corrigido. Esse alarme falso crônico desregula as escolhas normais de reparo, particularmente a recombinação homóloga precisa, levando a lesões persistentes no DNA, ativação de pontos de checagem e morte celular. Embora os efeitos mais fortes sejam observados em níveis nucleares altos de ASO típicos de experimentos de transfecção, a ativação sutil da sinalização de dano é detectável mesmo em doses mais baixas, semelhantes às usadas clinicamente. Para pacientes e desenvolvedores de medicamentos, a mensagem é clara: as próprias características químicas que tornam os ASOs medicamentos eficazes podem, em alguns contextos, interferir no mecanismo de proteção mais fundamental da célula — sua capacidade de manter um genoma estável — ressaltando a necessidade de projetar espinhas dorsais mais seguras e monitorar as vias de reparo do DNA durante a terapia.
Citação: Hjelmgren, L., Zhou, Q., Schmidli, S. et al. Dysregulation of the DNA damage response by phosphorothioate antisense oligonucleotides. Nat Commun 17, 2111 (2026). https://doi.org/10.1038/s41467-026-69980-2
Palavras-chave: oligonucleotídeos antissenso, resposta ao dano no DNA, separação de fase líquida, recombinação homóloga, estabilidade genômica