Clear Sky Science · pt
Imitações quirais de peptidoglicano miram a biossíntese da parede bacteriana para intervenção contra patógenos
Uma nova forma de caçar germes nocivos
Infecções resistentes a antibióticos estão aumentando no mundo todo, mas os médicos ainda carecem de ferramentas que identifiquem e ataquem com precisão bactérias perigosas sem prejudicar nossas próprias células. Este estudo apresenta um “ispinho” molecular inteligente que imita um bloco de construção essencial das paredes celulares bacterianas. Essas moléculas projetadas podem tanto iluminar infecções para imageamento quanto transportar antibióticos diretamente para os microrganismos, oferecendo uma estratégia nova para combater patógenos de difícil tratamento.
Imitando a armadura bacteriana
As bactérias são envolvidas por uma malha resistente chamada parede celular, construída a partir de açúcares e de aminoácidos espelhados incomuns que nossas próprias células, em grande parte, não utilizam. Os pesquisadores aproveitaram essa diferença criando longas cadeias à base de açúcar decoradas com uma forma espelhada específica da alanina, um aminoácido comum. Essas cadeias, chamadas imitações quirais de peptidoglicano, foram projetadas para se assemelhar de perto aos ingredientes naturais que as bactérias usam para construir suas paredes, mas são ausentes nos tecidos de mamíferos. Ao ajustar finamente quanto dessa alanina em forma D estava ligada, a equipe produziu versões que favoreciam fortemente as bactérias em vez das células humanas.
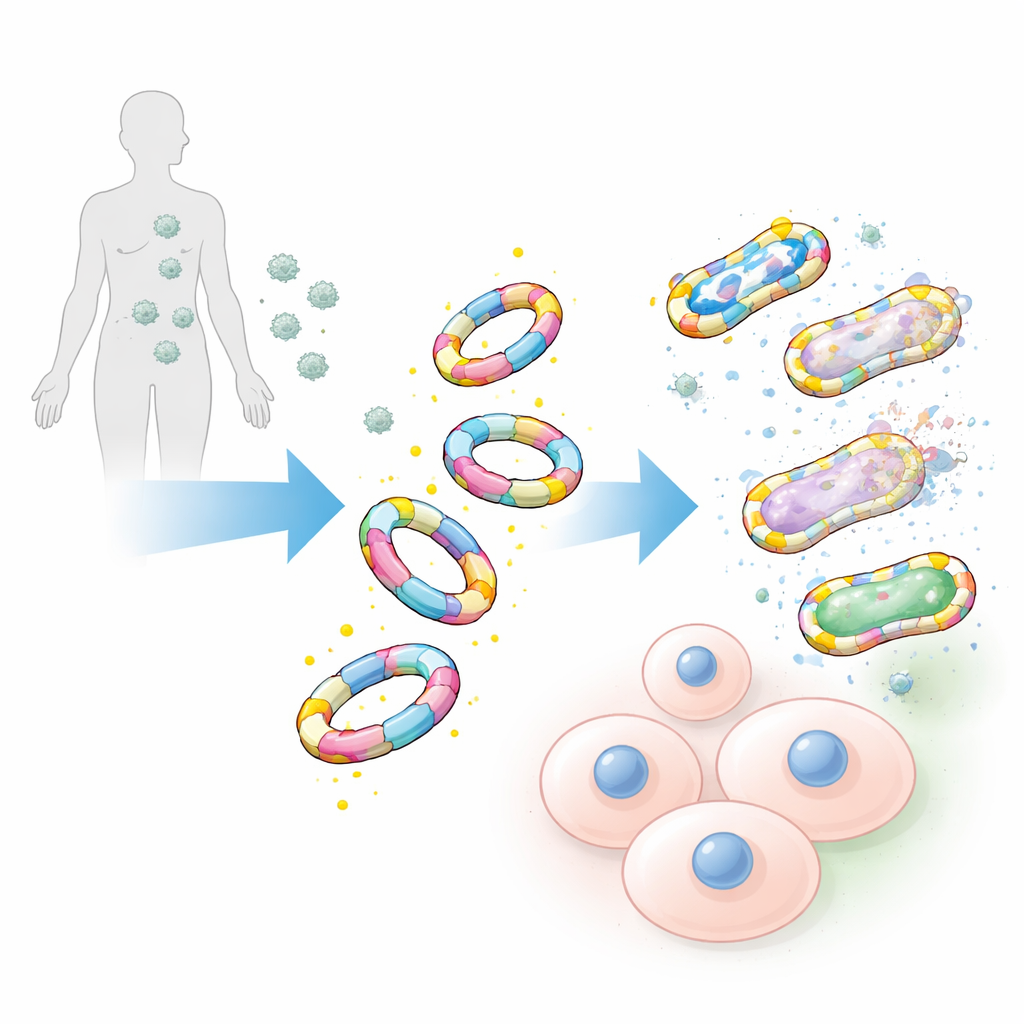
Focando nas bactérias, não em nossas células
Quando testadas contra uma ampla gama de patógenos, incluindo cepas hospitalares notórias como Staphylococcus aureus resistente à meticilina e outras bactérias ESKAPE, as imitações decoradas com D-alanina ligaram-se às superfícies bacterianas com eficiência impressionante. Seus correspondentes em imagem espelhada construídos com a forma L da alanina, assim como as cadeias de açúcar originais isoladas, mostraram ligação fraca ou negligenciável. A equipe também comparou essas grandes imitações com sondas químicas tradicionais pequenas baseadas em moléculas isoladas de D-alanina. Mesmo quando as sondas pequenas foram tornadas extremamente brilhantes, ainda rotularam muito menos bactérias e produziram sinais mais fracos, evidenciando a vantagem do desenho maior e mais realista.
Sequestrando a linha de montagem da parede celular
Para entender por que o reconhecimento se torna tão forte, os cientistas examinaram como as imitações interagem com a maquinaria bacteriana de construção da parede. Eles descobriram que as cadeias baseadas em D-alanina não apenas aderem externamente; elas são incorporadas como se fossem blocos de construção genuínos e alimentadas nas mesmas etapas enzimáticas que normalmente unem os componentes da parede celular. Análises químicas detectaram novos intermediários que surgem somente na presença dessas imitações, e simulações por computador mostraram que enzimas-chave de construção da parede agarram as imitações ainda mais firmemente do que os substratos naturais. Ao longo de várias rodadas de crescimento bacteriano, as imitações se acumularam na parede, distorcendo gradualmente sua estrutura e tornando-a permeável.
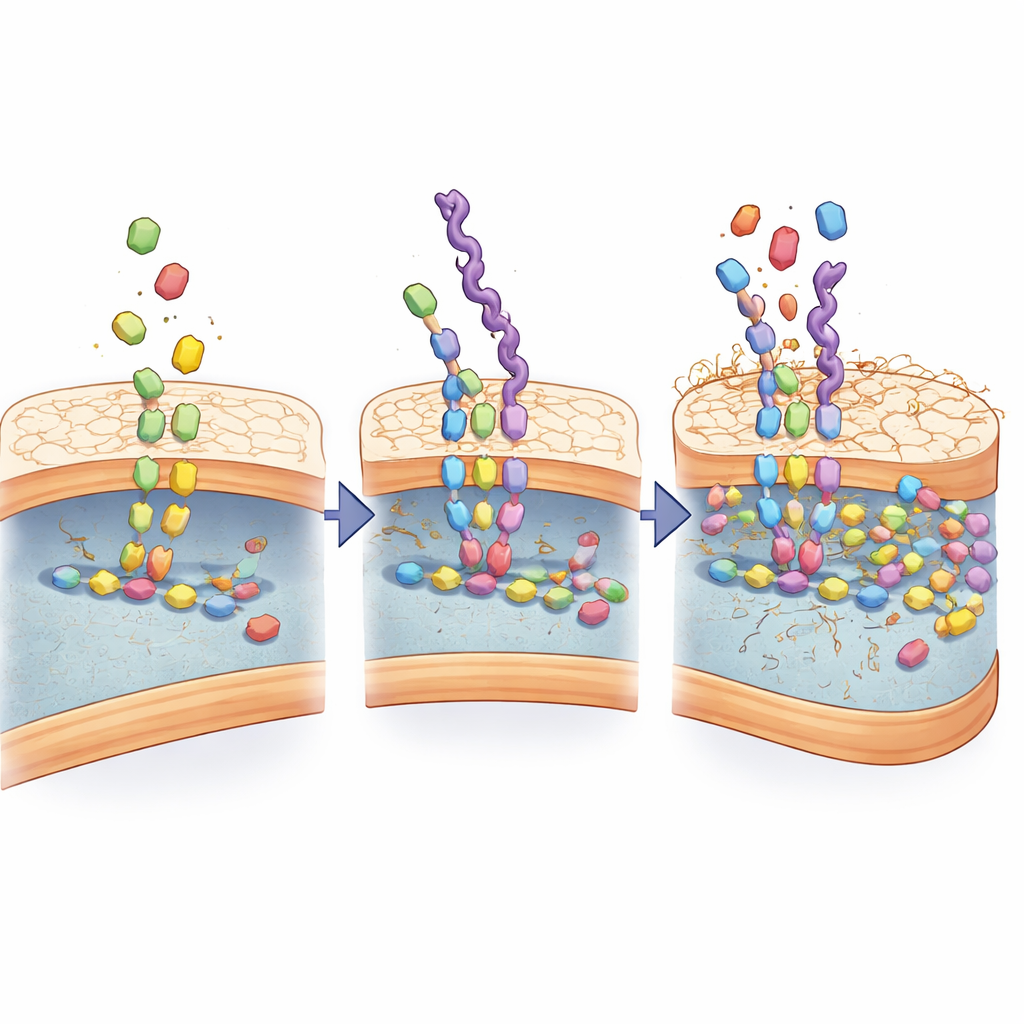
Transformando imitações em transportadores inteligentes de fármacos
Como essas cadeias se agregam naturalmente em pequenas partículas em água e carregam muitas “alças” químicas, a equipe as utilizou como andaimes para corantes de imageamento e antibióticos. Versões fluorescentes delinearam claramente as bactérias em culturas celulares, enquanto interagiam pouco com células de mamíferos cultivadas ao lado. Os pesquisadores então carregaram o antibiótico tetraciclina nas partículas baseadas nas imitações. Em testes de laboratório, esse encapsulamento tornou a tetraciclina várias vezes mais eficaz, matando até cepas resistentes em doses muito menores do que o fármaco livre. A microscopia revelou que as imitações carregadas de antibiótico se aglomeravam sobre as bactérias, penetravam seus envelopes e provocavam morte celular extensa em comparação com formulações não direcionadas.
Combatendo infecções dentro do organismo
Os testes mais exigentes ocorreram em modelos murinos de feridas cutâneas localizadas e infecções abdominais potencialmente fatais. Em feridas infectadas, as imitações fluorescentes localizaram bactérias em profundidade no tecido e, quando transportavam tetraciclina, praticamente eliminaram os micróbios. Isso levou a cicatrização mais rápida, pele nova mais espessa, deposição de colágeno mais ordenada e maior crescimento de pequenos vasos sanguíneos. Em modelos de infecção sistêmica, as imitações se acumularam especificamente em órgãos infectados, como baço e pulmões, onde reduziram drasticamente a contagem bacteriana quando carregadas com antibiótico. Importante, doses altas das imitações isoladas mostraram boa segurança, sem danos óbvios a órgãos principais ou alterações na química sanguínea.
O que isso pode significar para tratamentos futuros
Ao construir um análogo químico muito próximo dos próprios ingredientes da parede bacteriana, este trabalho demonstra uma nova forma de “misturar-se” ao metabolismo do patógeno em vez de apenas atacar de fora. Essas imitações quirais funcionam tanto como faróis de alta precisão para imageamento quanto como veículos inteligentes que direcionam antibióticos diretamente aos seus alvos microbianos, incluindo cepas resistentes, enquanto poupam células de mamíferos. Se traduzidas em ferramentas clínicas, plataformas biomiméticas assim poderiam ajudar médicos a ver exatamente onde as infecções se escondem e tratá-las de forma mais eficaz com doses menores de fármacos, oferecendo uma arma promissora contra o desafio crescente da resistência antimicrobiana.
Citação: Deng, K., Zou, D., Zeng, Z. et al. Chiral peptidoglycan mimics target bacterial wall biosynthesis for pathogen intervention. Nat Commun 17, 3258 (2026). https://doi.org/10.1038/s41467-026-69967-z
Palavras-chave: resistência a antibióticos, parede celular bacteriana, liberação direcionada de fármacos, imagem molecular, nanomedicina