Clear Sky Science · pt
Dissecação multimodal da patologia específica por tipo celular de TDP-43 no córtex motor
Por que esta pesquisa importa para as pessoas
A esclerose lateral amiotrófica (ELA) e a demência frontotemporal (DFT) são doenças cerebrais devastadoras que tiram das pessoas a mobilidade, a fala e a personalidade. A maioria dos pacientes com ELA e muitos com DFT compartilham um marcador microscópico comum: agregados de uma proteína chamada TDP-43 acumulando-se onde não deveriam. Este estudo faz duas perguntas práticas com grandes implicações para tratamentos futuros: exatamente quais células cerebrais são mais afetadas pelos problemas com TDP-43, e o que dá errado dentro dessas células ao nível da regulação do DNA e da atividade gênica?
Seguindo o dano até o centro de movimento do cérebro
Os pesquisadores focaram no córtex motor primário, a faixa de tecido cerebral que controla o movimento voluntário. Usando amostras cerebrais doadas post-mortem de pessoas com ELA, ELA-DFT e controles neurologicamente saudáveis, eles isolaram núcleos celulares individuais e leram tanto quais genes estavam ativos quanto quão compactado estava o DNA local. Essa abordagem “multiômica”, aplicada a mais de 180.000 núcleos, permitiu classificar as células em tipos precisos: várias classes de neurônios excitatórios e inibitórios, além de células de suporte como astrócitos, oligodendrócitos e microglia. Em seguida, combinaram isso com mapas espaciais de expressão gênica de outro conjunto de dados humanos para reposicionar esses tipos celulares na estrutura em camadas familiar do córtex.
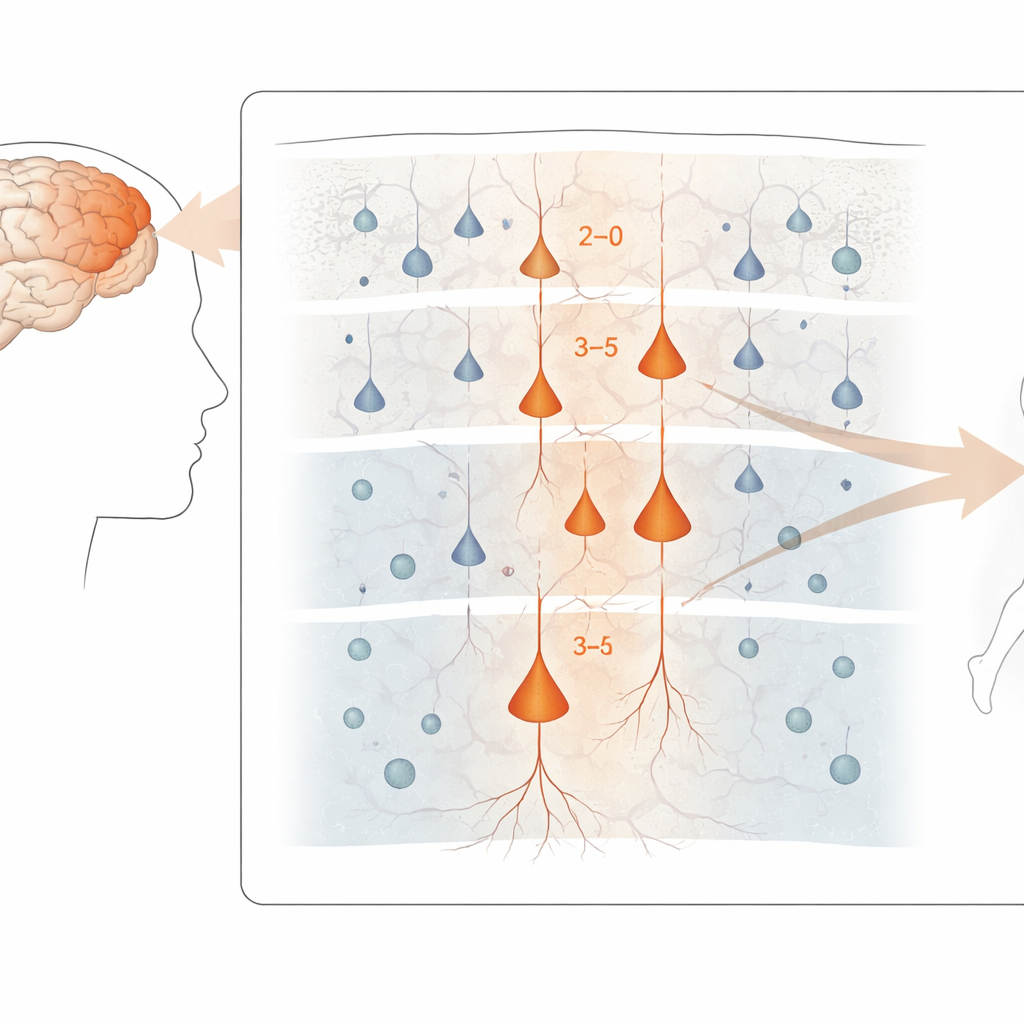
Localizando os neurônios mais vulneráveis
Ao longo do córtex motor, as alterações gênicas mais fortes relacionadas à doença apareceram em neurônios excitatórios, as células que impulsionam a atividade através dos circuitos cerebrais. Em particular, neurônios das camadas superiores e médias que fazem conexões dentro do córtex, assim como certos neurônios de camadas profundas que enviam sinais para fora do córtex — incluindo as grandes células “de Betz” que controlam os neurônios motores espinhais — mostraram as alterações mais pronunciadas. Em contraste, interneurônios inibitórios e muitas células gliais foram menos afetados ao nível da expressão gênica, embora alguns apresentassem mudanças mais sutis. Apesar desse turbilhão molecular, a composição geral dos principais tipos celulares no tecido foi surpreendentemente similar entre pacientes e controles, sugerindo que o dano tem mais a ver com o funcionamento das células do que simplesmente com quantas são perdidas.
Como TDP-43 remodela a atividade gênica de dentro
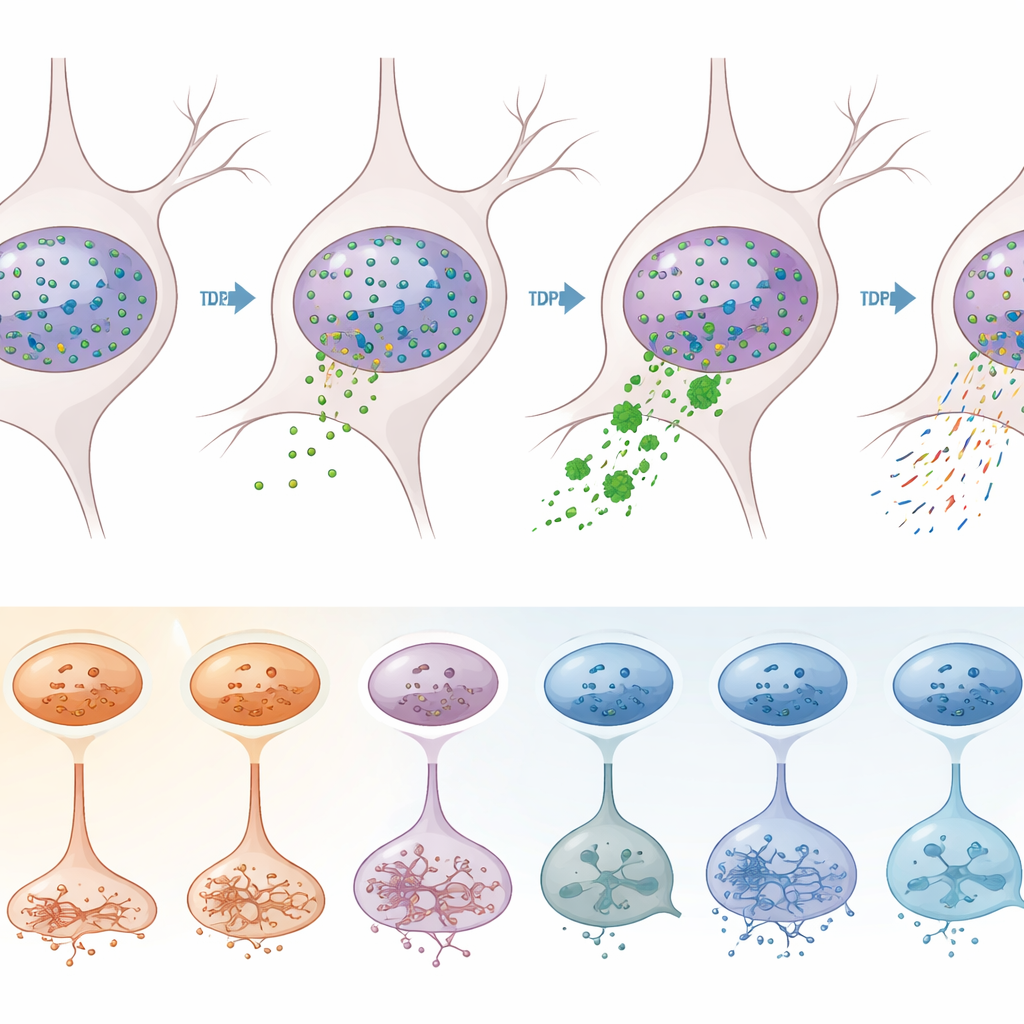
Para separar efeitos dirigidos diretamente pelo TDP-43 de outros processos da doença, a equipe usou uma estratégia de separação engenhosa. Eles marcaram núcleos com anticorpos contra TDP-43 e um marcador neuronal, e então usaram citometria de fluxo para separar neurônios cujos núcleos haviam perdido TDP-43 (um sinal de patologia) daqueles que o mantinham. O sequenciamento de mais de 12.000 desses núcleos revelou que a perda de TDP-43 ocorre esmagadoramente em neurônios excitatórios, especialmente subtipos específicos nas camadas 2–3, 3–5, 5 e 6. Naqueles neurônios vulneráveis, centenas de genes estavam desregulados, incluindo muitos já vinculados à ELA. Assinaturas moleculares clássicas do mau funcionamento do TDP-43 — como o aparecimento de trechos “crípticos” extras nos transcritos dos genes STMN2 e KALRN, e mudanças nos pontos de clivagem e poliadenilação dos RNAs — foram nitidamente enriquecidas nos núcleos deficientes em TDP-43.
Remodelação epigenética: nem toda mudança vem do TDP-43
Porque mediram tanto a atividade gênica quanto a acessibilidade da cromatina nos mesmos núcleos, os autores puderam investigar quais mudanças estavam associadas a alterações no empacotamento do DNA. Eles encontraram dezenas de milhares de locais no genoma onde a acessibilidade local da cromatina acompanhava a expressão gênica. Muitos dos genes alterados na ELA e na ELA-DFT situavam-se nessas regiões, indicando que parte da assinatura da doença reflete uma remodelação epigenética mais ampla em vez de consequências diretas da perda de TDP-43. Curiosamente, essas mudanças ligadas à cromatina frequentemente convergiam em vias de sinalização envolvidas na comunicação celular e orientação de axônios, e foram especialmente fortes em certos neurônios excitatórios e em oligodendrócitos. Quando a equipe comparou as alterações gênicas associadas à patologia do TDP-43 com aquelas ligadas às mudanças na cromatina, verificaram que eram parcialmente sobrepostas, mas em grande parte camadas distintas de disrupção.
O que isso significa para terapias futuras
Para o leitor leigo, a mensagem principal é que ELA e ELA-DFT não danificam o córtex motor de forma uniforme. Em vez disso, atingem tipos específicos de neurônios excitatórios e, em menor grau, certas células de suporte, alterando seus programas gênicos de maneiras que dependem tanto do mau funcionamento do TDP-43 quanto de mudanças mais amplas em como o DNA é empacotado e lido. Esses achados sugerem que tratamentos eficazes podem precisar ser específicos por tipo celular e por via — por exemplo, restaurar a função do TDP-43 ou corrigir seus erros de splicing nos neurônios mais vulneráveis, enquanto se direcionam separadamente alterações epigenéticas e de sinalização compartilhadas por múltiplos tipos celulares. Ao mapear esse panorama complexo em alta resolução, o estudo fornece um roteiro para projetar intervenções mais precisas destinadas a retardar ou prevenir a perda do controle do movimento na ELA e na ELA-DFT.
Citação: Ruf, W.P., Kühlwein, J.K., Meier, L. et al. Multi-modal dissection of cell-type specific TDP-43 pathology in the motor cortex. Nat Commun 17, 2406 (2026). https://doi.org/10.1038/s41467-026-69944-6
Palavras-chave: ELA, demência frontotemporal, TDP-43, neurônios do córtex motor, multiômica de núcleo único