Clear Sky Science · pt
As células Th17 requerem o sensor de reparo de DNA xeroderma pigmentosum grupo C para controlar dano oxidativo ao DNA em um modelo murino
Guardião dos nossos defensores imunes
As células T auxiliares 17, ou células Th17, são um tipo especial de glóbulo branco que patrulha as barreiras do nosso corpo, como o intestino e a pele, para defender contra bactérias e fungos. Mas também estão envolvidas em doenças autoimunes quando suas respostas saem do controle. Este estudo faz uma pergunta aparentemente simples: como essas células altamente ativas protegem seu próprio DNA do estresse químico que geram ao combater infecções? A resposta se concentra em um sensor de dano ao DNA chamado XPC, mais conhecido por proteger células da pele contra a luz solar. Aqui, os pesquisadores mostram que o XPC também é crítico para manter as células Th17 saudáveis, energéticas e eficazes.
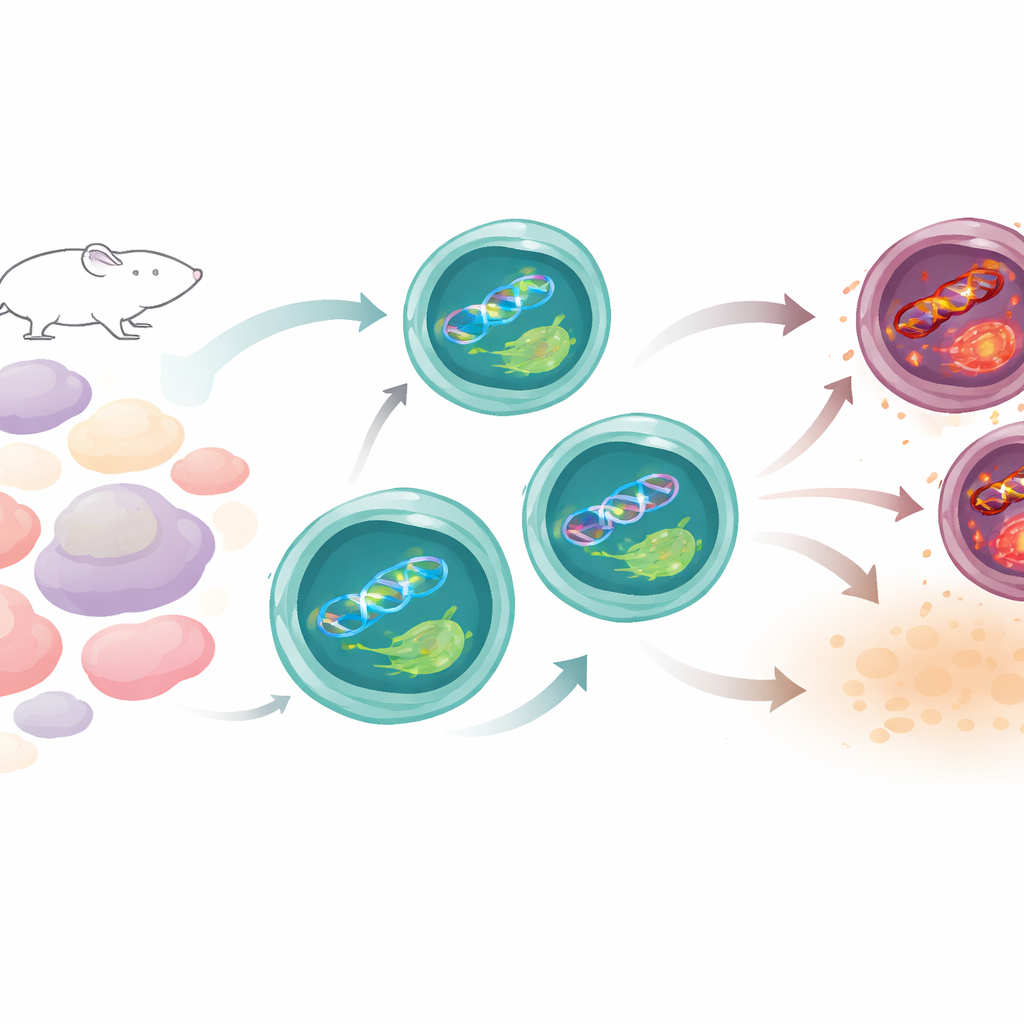
Como as células Th17 mantêm o equilíbrio normalmente
As células Th17 levam uma vida perigosa. Para funcionar, aumentam seu metabolismo e produzem espécies reativas de oxigênio—moléculas quimicamente reativas que podem danificar o DNA. A equipe comparou células Th17 com outros tipos de células T em camundongos e descobriu que, apesar de sua intensa atividade, as Th17 acumulam menos dano ao DNA do que muitas de suas congêneres. Uma pista chave foi que genes envolvidos no reparo do DNA, especialmente os de uma via que normalmente corrige lesões induzidas pelo sol, estavam mais fortemente ativados nas células Th17. Entre eles estava o XPC, uma proteína que varre o DNA em busca de danos estruturais. À medida que as células Th17 amadureciam, os níveis de XPC aumentavam e se localizavam em sítios danificados no núcleo, sugerindo que ele estava em patrulha constante para manter sua integridade genética.
O que acontece quando o sensor de DNA está ausente
Para avaliar a real importância do XPC, os pesquisadores usaram camundongos geneticamente modificados para não expressar essa proteína. À primeira vista, o sistema imune parecia em grande parte normal: o número total de células T e muitos subtipos de células T não se alteraram. Mas, ao focalizar nas células Th17, surgiu um defeito marcante. Sem XPC, bem menos células produziram a molécula característica Th17, IL-17, e marcadores de identidade e chaves de sinalização que dirigem o programa Th17 estavam reduzidos. Em culturas, células T naïve desses animais tiveram dificuldade em se diferenciar completamente em células Th17. Em um modelo padrão em que células T transferidas desencadeiam inflamação intestinal, as células T deficientes em XPC não induziram colite, refletindo uma capacidade inflamatória atenuada. Ao mesmo tempo, células T reguladoras, que acalmam respostas imunes, tornaram-se mais abundantes, indicando um deslocamento do equilíbrio entre agressão e contenção.
Dano ao DNA, usinas de energia e estresse químico
Aprofundando a investigação, a equipe constatou que células Th17 sem XPC apresentavam mais quebras na fita de DNA e mais bases de DNA oxidadas, uma assinatura de ataque por espécies reativas de oxigênio. Genes que normalmente detectam dano ao DNA e interrompem o ciclo celular também estavam reduzidos, sugerindo um sistema de alarme enfraquecido. O metabolismo energético das células foi remodelado: elas perderam parte da capacidade de usar vias rápidas de queima de açúcar e passaram a depender mais das mitocôndrias, as pequenas usinas de energia da célula. Ainda assim, essas mitocôndrias liberavam mais espécies reativas de oxigênio e mostravam sinais de sobrecarga, criando um ciclo vicioso de aumento do estresse químico e agravamento do dano ao DNA. Notavelmente, tratar as células com um antioxidante restaurou a produção de IL-17 e reduziu o dano ao DNA, ligando diretamente o estresse oxidativo ao defeito funcional observado.
Um esforço conjunto no reparo do DNA danificado
Além de seu papel clássico, o XPC também atuou em conjunto com outra proteína de reparo chamada OGG1, que reconhece uma base de DNA comumente oxidada. Os pesquisadores demonstraram que essas duas proteínas se associam fisicamente nas células Th17, ajudando a coordenar a remoção de bases danificadas. Quando o XPC estava ausente, a atividade de corte da OGG1 na verdade aumentou, como se tentasse compensar o excesso de dano. Mas essa hiperatividade ocorreu em um contexto de alto estresse oxidativo e redes de reparo perturbadas, e não foi suficiente para restaurar a função normal das Th17. Análises genéticas e estruturais sugeriram que o XPC atua como um hub conectando diferentes vias de reparo e controle redox, garantindo que o dano não apenas seja detectado, mas processado de modo a permitir que a célula continue se dividindo e produzindo moléculas protetoras.
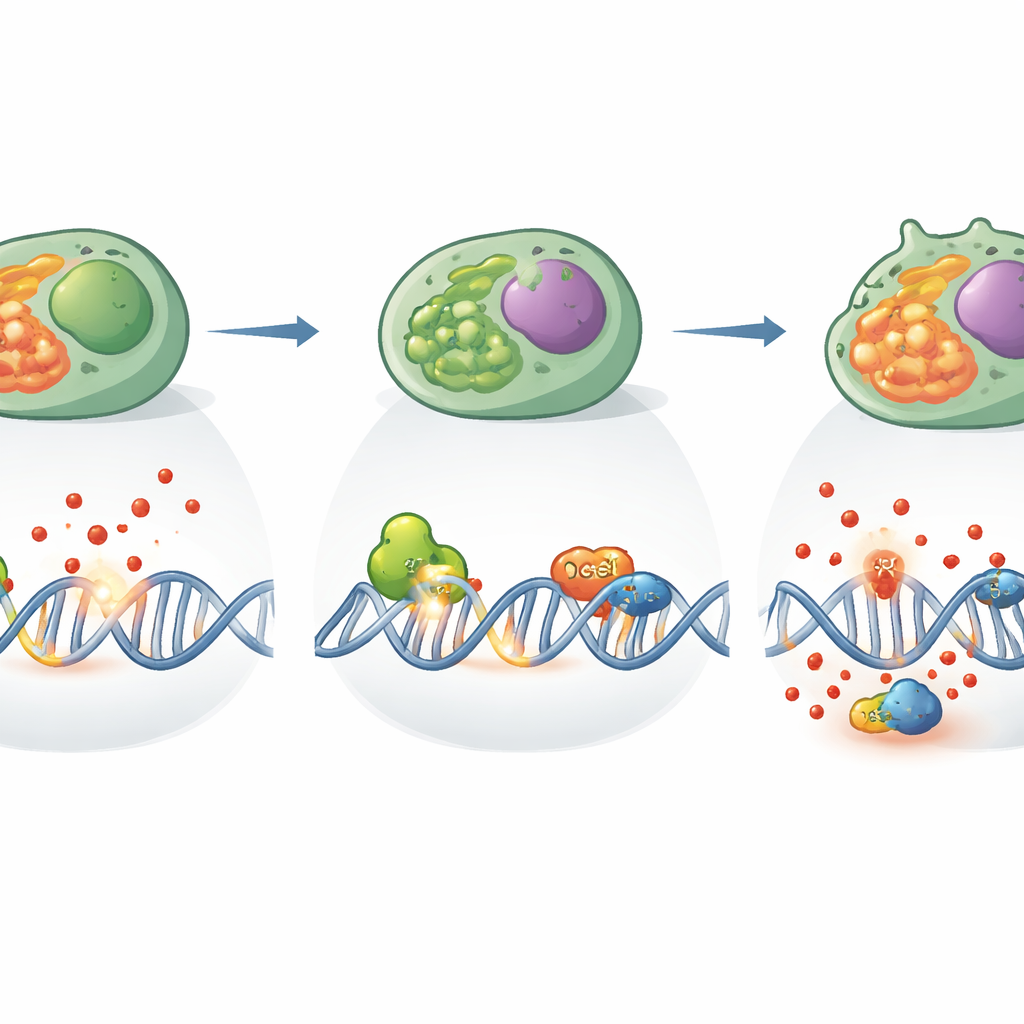
Por que isso importa para doença e terapia
Para o leitor leigo, a mensagem central é que as células imunes precisam de seus próprios guarda-costas internos para permanecerem aptas enquanto nos protegem. Este estudo revela que o XPC, antes famoso por proteger células da pele contra UV, também é um guardião vital das células Th17, mantendo seu DNA intacto e seus sistemas energéticos em equilíbrio sob estresse oxidativo. Quando o XPC está ausente, as Th17 tornam-se geneticamente e metabolicamente frágeis, produzem menos respostas inflamatórias e podem deslocar o equilíbrio imune em direção à regulação em vez do ataque. Como as células Th17 são centrais em condições como doença inflamatória intestinal, psoríase e esclerose múltipla, as vias controladas pelo XPC podem se tornar novos alvos para ajustar respostas imunes—seja para acalmar inflamação nociva ou para reforçar a defesa quando ela é fraca—modulando como essas células reparam seu DNA e lidam com o estresse oxidativo.
Citação: Leite, J.A., Bos, N.N., Menezes-Silva, L. et al. Th17 cells require the DNA repair sensor xeroderma pigmentosum complementation Group C to control oxidative DNA damage in a murine model. Nat Commun 17, 3157 (2026). https://doi.org/10.1038/s41467-026-69914-y
Palavras-chave: células Th17, reparo de DNA, estresse oxidativo, proteína XPC, doença autoimune