Clear Sky Science · pt
O fator de iniciação eucariótico 6 modula a plasticidade do carcinoma de pulmão de pequenas células via o eixo de sinalização integrina-FAK
Por que esta pesquisa sobre câncer de pulmão é importante
O carcinoma de pulmão de pequenas células (CPPC) é uma das formas mais letais de câncer de pulmão. Geralmente responde bem à quimioterapia inicialmente, mas quase sempre recorre, de forma rápida e agressiva. Este estudo aborda uma questão central: o que permite que as células de CPPC “mudem de personalidade” e se tornem resistentes aos medicamentos, e é possível retardar ou bloquear essa metamorfose?
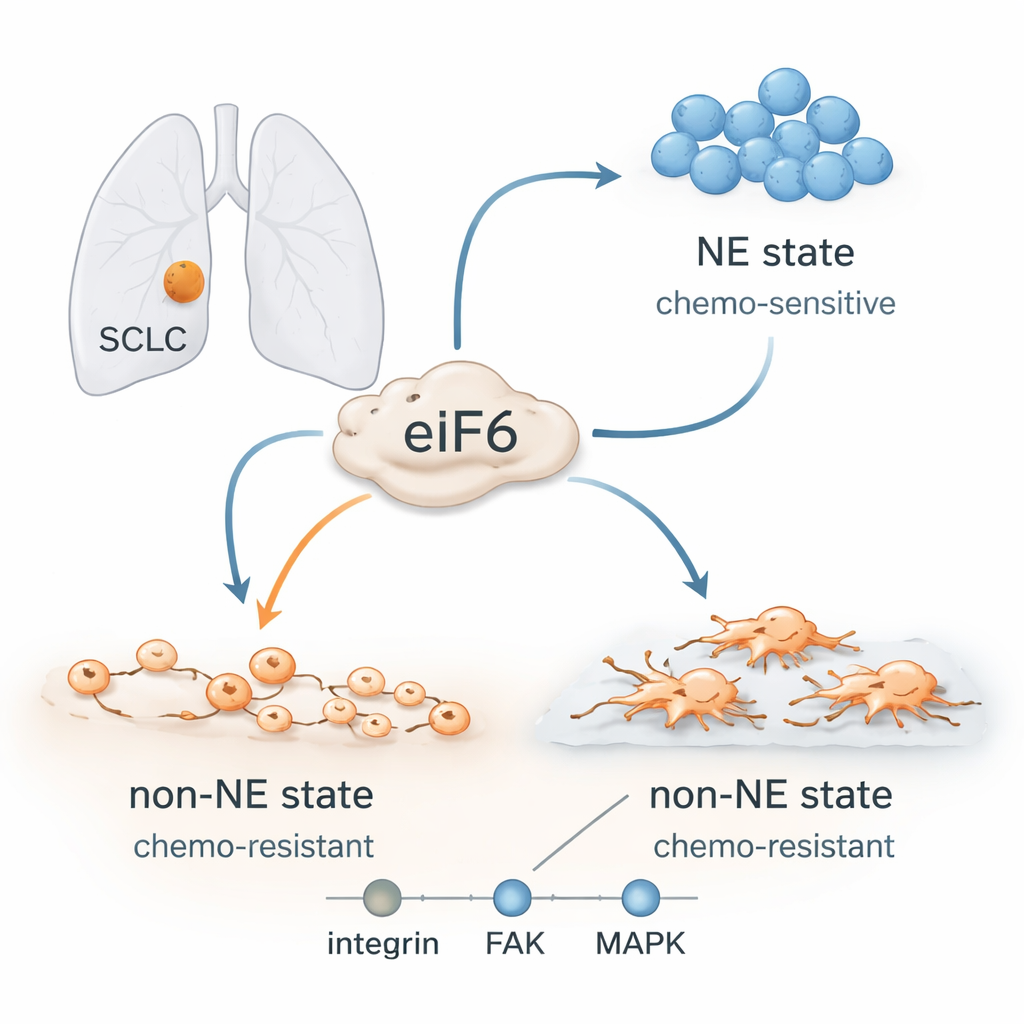
Células cancerígenas que mudam de forma
Os médicos costumavam considerar o CPPC uma doença uniforme, mas agora está claro que esses tumores contêm tipos celulares diferentes. Algumas células apresentam uma forte identidade “neuroendócrina”: crescem em aglomerados flutuantes compactos, respondem bem à quimioterapia à base de platina e tendem a ser ricas em certas proteínas de aparência nervosa. Outras perdem essa identidade e adotam um estado “não neuroendócrino”: espalham‑se, aderem ao tecido circundante, exibem características de células mais móveis e invasivas, e são muito mais difíceis de eliminar com drogas. Os tumores dos pacientes frequentemente evoluem do estado sensível para o resistente durante ou após o tratamento, mesmo que o DNA não mude muito. Isso aponta para programas celulares flexíveis, e não novas mutações, como motor da recaída.
Um fator de tradução com dupla vida
Os autores concentraram‑se em uma proteína chamada eIF6, mais conhecida por ajudar a montar ribossomos, as fábricas de proteínas da célula. Ao estudar amostras de pacientes, modelos de camundongo e várias linhagens humanas de CPPC, eles descobriram que os níveis de eIF6 aumentavam consistentemente quando as células mudavam para o estado não neuroendócrino resistente a drogas. Surpreendentemente, esse aumento ocorreu junto com uma queda geral na produção de proteínas em massa, sugerindo que o eIF6 pode estar fazendo mais do que seu papel clássico. Análises detalhadas de como os RNAs mensageiros se ligam aos ribossomos mostraram que as partes básicas do ribossomo não mudaram muito. Em vez disso, a seleção e o processamento das mensagens para tradução foram reconfigurados quando as células trocavam de identidade.
Rompendo para se conectar a sinais de sobrevivência
Ao aprofundar, a equipe descobriu que, nas células resistentes, parte do eIF6 se desprende dos ribossomos e se associa a um centro de sinalização na superfície formado por integrinas e uma proteína chamada quinase de adesão focal (FAK). As integrinas ajudam as células a sentir e se prender ao ambiente; a FAK transmite esses sinais para dentro, frequentemente ativando vias que promovem movimento, sobrevivência e tolerância a drogas. Ensaios bioquímicos de captura e testes de proximidade dentro da célula mostraram que o eIF6 interage fisicamente com o parceiro integrina CD104 e com a FAK, e que esses complexos são mais abundantes em células não neuroendócrinas. Esse conjunto eIF6–integrina–FAK, por sua vez, aumenta a atividade da via de sinalização MAPK, um conhecido condutor de crescimento e resistência ao estresse.
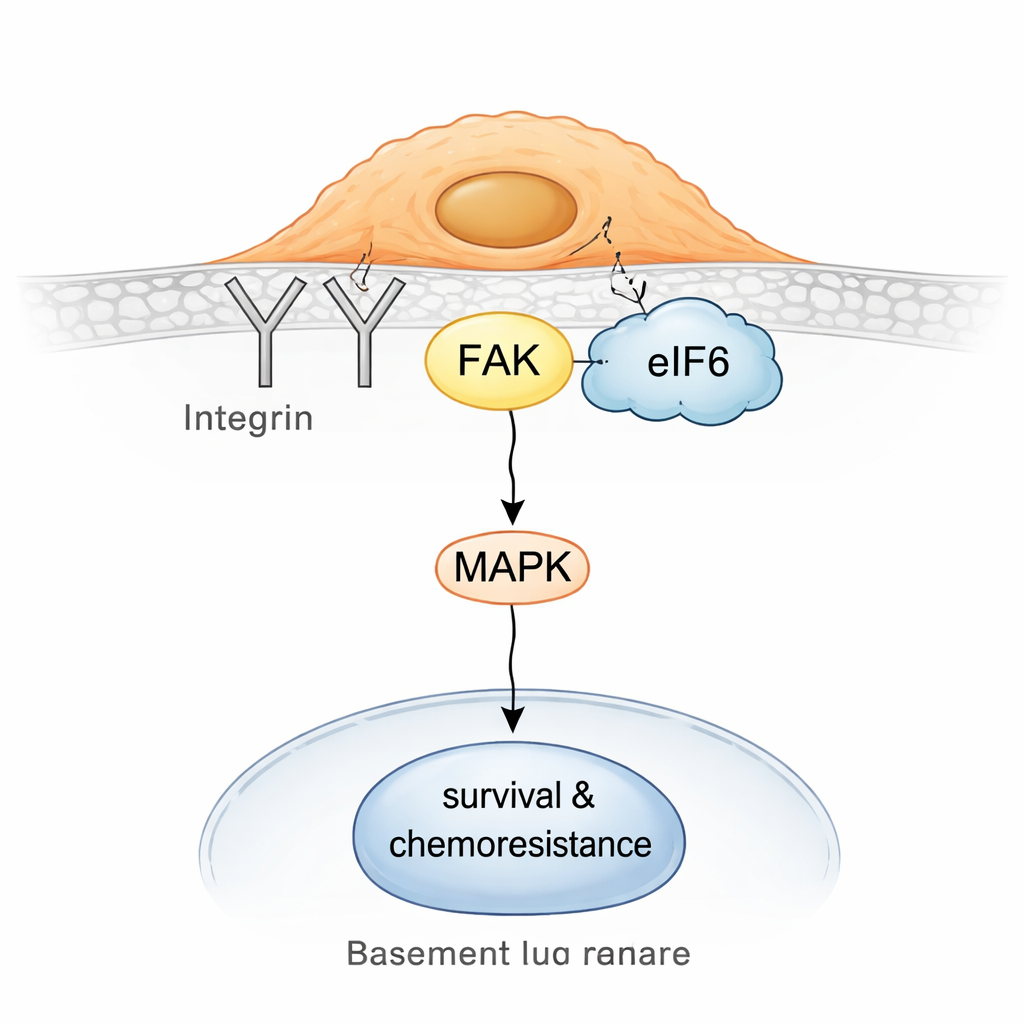
Tornando tumores resistentes vulneráveis novamente
Os pesquisadores então perguntaram se manipular o eIF6 poderia mudar o comportamento do CPPC. Quando reduziram os níveis de eIF6 em células resistentes, genes ligados a um programa móvel e formador de cicatriz (epitélio–mesênquima) foram diminuídos, enquanto genes neuroendócrinos clássicos foram parcialmente restabelecidos. Essas mudanças não reverteram completamente o processo, mas retardaram a transição para o estado resistente. Crucialmente, células com menos eIF6 tornaram‑se mais sensíveis à quimioterapia padrão carboplatina–etoposídeo em cultura e em tumores de camundongo, resultando em menos colônias sobreviventes e em uma redução tumoral mais duradoura. Como o eIF6 em si ainda não dispõe de fármacos específicos, a equipe testou inibidores de FAK já em desenvolvimento clínico. Bloquear a sinalização FAK re‑sensibilizou as células resistentes à quimioterapia e, em camundongos, o tratamento combinado produziu o melhor controle tumoral.
Do insight em laboratório a ferramentas futuras para pacientes
Por fim, os autores examinaram amostras tumorais de pacientes com CPPC em estágio limitado que haviam passado por cirurgia. Usando um método de coloração sensível que ilumina proteínas apenas quando estão próximas, eles mediram com que frequência o eIF6 forma complexo com CD104 ou FAK dentro das células tumorais. Altos níveis desses complexos—mais do que o eIF6 isolado—foram associados a recidiva mais precoce e menor sobrevida, marcando‑os como potenciais sinais prognósticos. Em conjunto, este trabalho revela que o eIF6 pode “atuar em paralelo” fora dos ribossomos para ajudar a ligar as células cancerígenas a circuitos de sobrevivência poderosos. Ao mapear esse eixo eIF6–integrina–FAK, o estudo sugere maneiras de identificar pacientes com maior risco de recaída e apoia a combinação de inibidores de FAK com quimioterapia para enfrentar a perigosa plasticidade do CPPC.
Citação: Peng, H., Wang, Z., Wang, M. et al. Eukaryote initiation factor 6 modulates small-cell lung carcinoma plasticity via the integrin-FAK signaling axis. Nat Commun 17, 2048 (2026). https://doi.org/10.1038/s41467-026-69899-8
Palavras-chave: câncer de pulmão de pequenas células, resistência a medicamentos, plasticidade celular, eIF6, sinalização integrina FAK