Clear Sky Science · pt
Inibição da tradução dependente do contexto como modalidade terapêutica contra o câncer
Virando as fábricas de proteínas contra o câncer
As células cancerosas sobrevivem produzindo constantemente grandes quantidades de proteínas “motoras” de curta meia‑vida que as mantêm crescendo e se dividindo. Este estudo explora uma nova forma de combater o câncer ao atrapalhar sutilmente as máquinas de síntese de proteínas da célula — os ribossomos — somente quando elas tentam construir sequências proteicas específicas, especialmente as encontradas em oncogenes difíceis de atingir com drogas, como o MYC. Essa interferência seletiva poderia matar células tumorais preservando grande parte da produção proteica normal.
Como as células constroem proteínas — e onde as coisas podem dar errado
Cada célula depende dos ribossomos, pequenas fábricas moleculares que leem mensagens genéticas (mRNAs) e unem aminoácidos em proteínas. A maioria dos fármacos existentes que atingem ribossomos, como antibióticos ou drogas oncológicas antigas, age como ferramentas contundentes: interrompem amplamente a síntese proteica, o que pode prejudicar células saudáveis e causar efeitos colaterais graves. Os autores raciocinaram que, como cada cadeia proteica nascente tem uma sequência e caráter químico únicos, poderia ser possível projetar pequenas moléculas que bloqueiem o ribossomo apenas quando uma sequência específica estiver na máquina, deixando a maior parte da produção proteica da célula praticamente intacta.
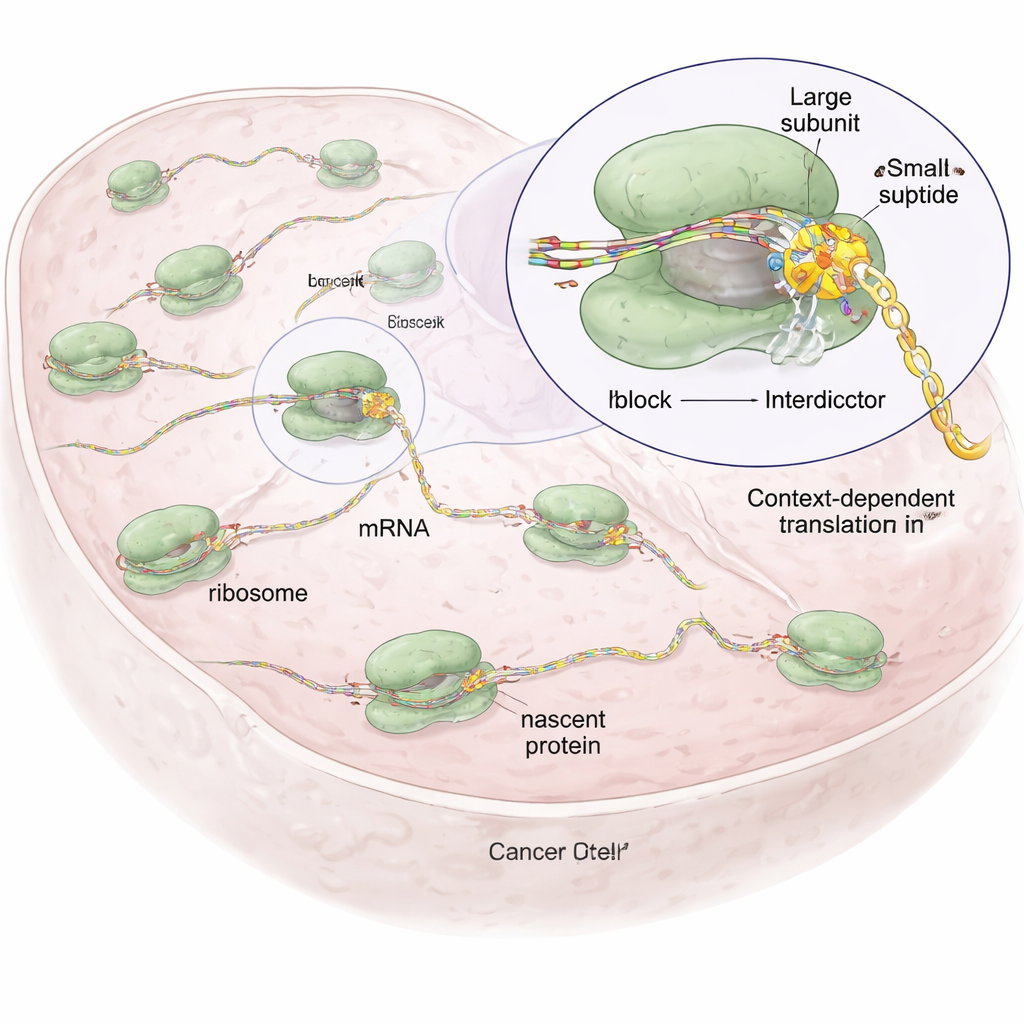
Moléculas desenhadas que interrompem apenas certas sequências proteicas
Partindo de um composto natural chamado anisomicina, que se liga ao coração catalítico do ribossomo onde as ligações peptídicas são formadas, os pesquisadores criaram uma família de moléculas sintéticas que chamam de “interditores”. Todas compartilham um esqueleto central que as ancora dentro do ribossomo, mas diferem em grupos laterais que apontam para a cadeia proteica em crescimento. Esses grupos laterais são ajustados para favorecer tipos particulares de aminoácidos — por exemplo, um interditor (IDB‑001) é atraído por resíduos carregados negativamente, enquanto outro (IDB‑002) prefere resíduos pequenos e oleosos (hidrofóbicos). Usando uma técnica chamada mapeamento de ribossomos (ribosome profiling), que localiza globalmente onde os ribossomos pausam em mRNAs dentro das células, a equipe mostrou que cada composto causa paralisações em motivos curtos e distintos na cadeia nascente, frequentemente no aminoácido penúltimo (−1), demonstrando ação dependente da sequência em vez de um desligamento indiscriminado.
Observando o encontro entre droga e ribossomo átomo a átomo
Para ver como essa seletividade funciona em detalhe físico, os autores congelaram ribossomos humanos no ato de traduzir sequências peptídicas projetadas e os imagearam por criomicroscopia eletrônica em resolução quase atômica. Eles observaram o interditor aninhado no sítio ativo do ribossomo fazendo contatos precisos com os últimos aminoácidos da cadeia nascente. Em uma estrutura, um grupo lateral hidrofóbico do IDB‑002 é acomodado por resíduos peptídicos pequenos e não volumosos, explicando por que cadeias laterais maiores ali são desfavorecidas. Em outra, a cadeia lateral ácida de um resíduo derivado de MYC gira para formar uma ponte salina com um grupo positivamente carregado no IDB‑001. A presença da droga também empurra bases do RNA ribossômico próximas para novas posições que estreitam o sítio ativo e bloqueiam parcialmente a entrada do próximo tRNA, ajudando a congelar a elongação nessas sequências favorecidas.
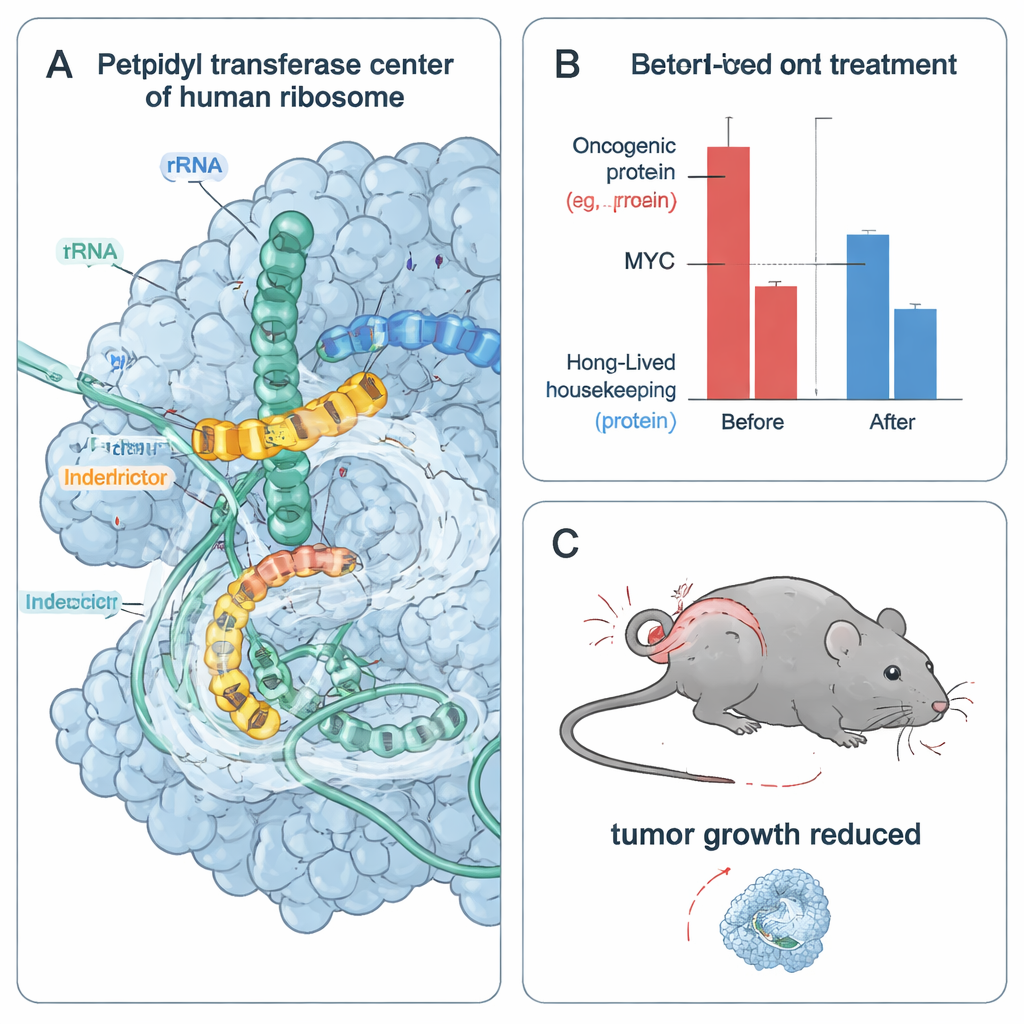
De ribossomos paralisados a células tumorais estressadas e morrendo
Como células cancerosas em rápido crescimento dependem fortemente de proteínas oncogênicas de curta duração como MYC e CCND1, a equipe testou como os interditores afetam a sobrevivência celular tumoral. Em várias linhas celulares cancerosas dependentes de MYC, IDB‑001 e IDB‑002 reduziram a viabilidade celular em concentrações nanomolares a micromolares baixas. Um análogo posteriormente otimizado, IDB‑003, foi ainda mais potente e adequado para administração oral. Nas células, esses compostos esgotaram rapidamente MYC e outras oncoproteínas de alta rotatividade, enquanto deixavam proteínas de manutenção de vida mais duradouras relativamente estáveis no mesmo período. As drogas também desencadearam respostas de estresse celular ligadas a colisões de ribossomos, mas bloquear essas vias de sinalização de estresse não eliminou a perda de viabilidade, sugerindo que a privação direta de proteínas oncogênicas essenciais é um motor importante da morte das células tumorais.
Prova de conceito em um modelo difícil de câncer de mama
Para testar se essa abordagem funciona em animais, os autores trataram camundongos com tumores humanos de câncer de mama triplo‑negativo com IDB‑003 administrado por via oral. Ao longo de 28 dias, os tumores dos animais tratados cresceram muito mais lentamente que os dos controles, com até 80% de inibição do crescimento tumoral nas doses mais altas e nenhuma toxicidade grave relatada neste estudo. A análise da expressão gênica dos tumores mostrou forte regulação negativa de programas de genes alvo do MYC, consistente com atividade reduzida de MYC in vivo. Juntos, esses resultados indicam que paralisar seletivamente ribossomos em sequências proteicas específicas pode enfraquecer tumores que dependem de drivers oncogênicos instáveis, enquanto potencialmente evita a toxicidade ampla de bloqueadores clássicos da tradução.
Por que isso importa para tratamentos futuros do câncer
Este trabalho introduz um novo tipo de droga de pequena molécula: uma que age não por se ligar a uma proteína pronta, mas por interceptá‑la enquanto está sendo feita e apenas quando uma curta “etiqueta de endereço” está presente. Como muitas proteínas promotoras do câncer são flexíveis, de curta duração ou carecem de cavidades óbvias para drogas convencionais, mirar diretamente sua síntese no ribossomo pode abrir caminho para tratar tumores impulsionados por genes hoje “intratáveis”, como o MYC. O estudo também sugere que, ao ajustar a química dos interditores, futuros medicamentos poderiam ser desenhados para focalizar diferentes motivos de sequência e alvos de doença, estendendo essa estratégia além da oncologia para outras condições em que reduzir proteínas específicas pode restaurar a saúde.
Citação: Diamond, P.D., Sauer, P.V., Holm, M. et al. Context-dependent translation inhibition as a cancer therapeutic modality. Nat Commun 17, 1963 (2026). https://doi.org/10.1038/s41467-026-69891-2
Palavras-chave: terapia contra o câncer direcionada ao ribossomo, inibição da tradução, tumores acionados por MYC, pequenas moléculas dependentes do contexto, câncer de mama triplo‑negativo