Clear Sky Science · pt
Engenharia in situ de TRIM13 aumenta a capacidade anti‑inflamatória de CAR‑Ms para terapia da fibrose hepática
Reprogramando a equipe de limpeza do fígado
A fibrose hepática, um processo de cicatrização que pode evoluir para cirrose e insuficiência hepática, afeta milhões de pessoas e hoje conta com poucas opções de tratamento eficazes. Este estudo explora uma forma de aproveitar e reprogramar as próprias células imunes do fígado para que elas não só removam as células que formam a cicatriz, como também acalmem a inflamação prejudicial, potencialmente oferecendo uma terapia mais segura e potente para doenças hepáticas crônicas.
Por que a cicatrização do fígado é tão difícil de deter
Quando o fígado é lesionado repetidamente — por vírus, álcool ou doenças metabólicas — ele tenta se curar depositando tecido cicatricial. Células especializadas chamadas células estreladas hepáticas passam a um estado “ativado” e produzem fibras resistentes, como se estivéssemos despejando concreto. Com o tempo, essa fibrose distorce o órgão e prejudica sua função. Células imunes chamadas macrófagos ocupam o centro desse processo. Num fígado lesionado, eles podem agir como uma espada de dois gumes: num modo, promovem inflamação e ativam as células estreladas; em outro, mais reparador, ajudam a degradar a cicatriz e restaurar o equilíbrio.
Transformando sinais prejudiciais em úteis
Os pesquisadores focaram num sinal de perigo chave em fígados danificados: DNA mitocondrial que vaza de células lesionadas. Os macrófagos detectam esse DNA por meio da via cGAS‑STING, que os empurra para um estado pró‑inflamatório e pró‑fibrose. Uma proteína chamada TRIM13 normalmente ajuda a conter a STING marcando‑a para destruição. A equipe supôs que aumentar TRIM13 dentro dos macrófagos do fígado poderia reorientá‑los para um modo calmante e reparador do tecido. Ao mesmo tempo, queriam que essas células caçassem e removessem diretamente as células estreladas formadoras de cicatriz. Para isso, usaram o conceito do receptor quimérico de antígeno, ou CAR, emprestado da terapia contra o câncer: um receptor sintético que permite às células imunes reconhecer um alvo escolhido — neste caso, uma proteína chamada FAP, abundante nas células estreladas ativadas.
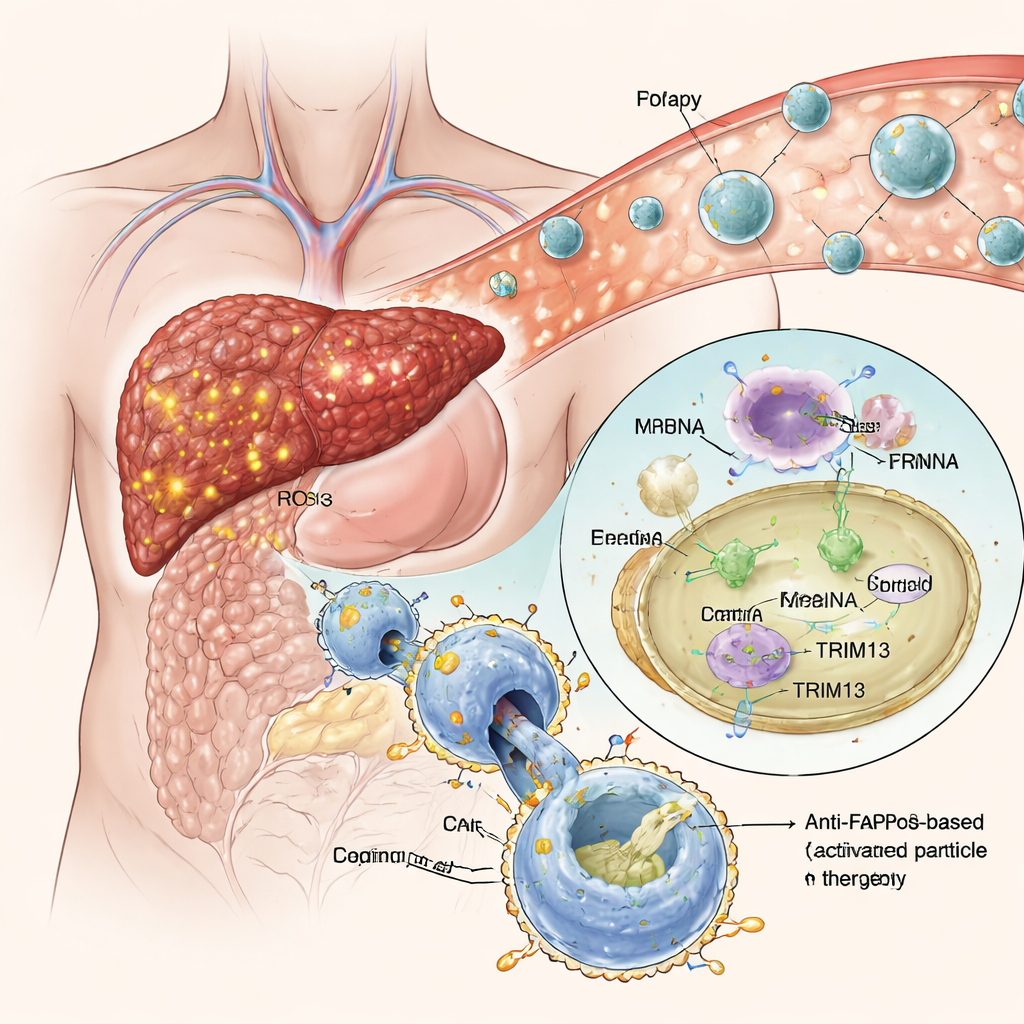
Nanopartículas inteligentes que se dirigem ao tecido doente
Em vez de modificar macrófagos fora do corpo, a equipe construiu nanopartículas lipídicas “desencadeadas por eferocitose” — minúsculas esferas à base de gordura que carregam instruções genéticas na forma de RNA mensageiro (mRNA). Essas partículas são recobertas com uma forma disfarçada de fosfatidilserina, um sinal natural de “coma‑me” que células moribundas exibem para atrair macrófagos. No ambiente altamente oxidativo do tecido hepático fibrótico, o disfarce é removido e o sinal é revelado, induzindo os macrófagos próximos a engolir as nanopartículas. Uma vez no interior, o mRNA é liberado e lido pela célula, levando à produção tanto de TRIM13 quanto do CAR anti‑FAP. Em culturas celulares, essa abordagem inclinou com sucesso os macrófagos para um estado anti‑inflamatório ao mesmo tempo em que lhes conferiu um apetite forte e seletivo por células formadoras de cicatriz FAP‑positivas, sem prejudicar sua habilidade normal de limpar outros detritos.
De fígados doentes a regenerativos em camundongos
A equipe então testou essa estratégia em modelos murinos de fibrose hepática causados por um agente químico tóxico ou por uma dieta deficiente e gordurosa. Nanopartículas injetadas sistemicamente alcançaram eficientemente o fígado e, especialmente em animais fibróticos, foram captadas principalmente por macrófagos. Lá, as células modificadas mostraram redução da atividade da via STING e menor produção de moléculas inflamatórias, além de maior capacidade de matar células estreladas ativadas. Análises de tecido revelaram quedas marcantes em colágeno e outros marcadores de cicatriz, matriz extracelular mais fina e com estrutura mais normal, e exames sanguíneos de função hepática melhorados. Os fígados dos animais tratados apresentaram mais células proliferando e recuperaram uma arquitetura mais saudável, sugerindo reparo genuíno do órgão em vez de apenas um abafamento temporário da inflamação.
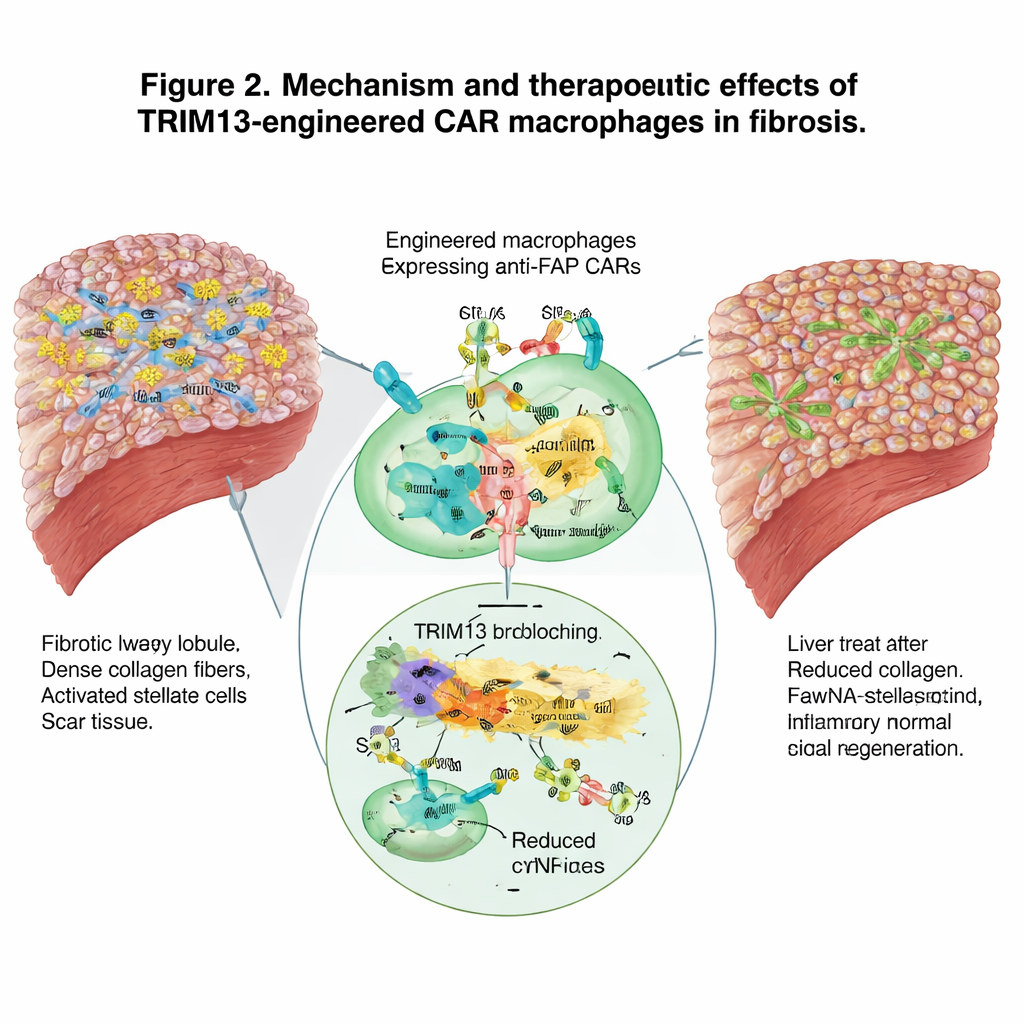
Recrutando o sistema imunológico mais amplo
Além da remoção direta da cicatriz, os macrófagos modificados remodelaram o panorama imune mais amplo. Eles mudaram de um perfil agressivo e promotor de dano para um mais resolutivo e reparador e reduziram sinais inflamatórios no sangue. Ao mesmo tempo, ao devorar as células que formam a cicatriz, pareceram atuar como instrutores para o sistema imune adaptativo, atraindo neutrófilos, células dendríticas e células T e incentivando uma resposta coordenada contra o tecido fibrótico. Sequenciamento de RNA de célula única das células imunes do fígado confirmou uma migração de programas gênicos pró‑inflamatórios para uma maior capacidade de englobar e limpar células e detritos nocivos.
O que isso pode significar para pacientes
Para um leitor leigo, a conclusão é que este trabalho aponta uma forma de “reeducar” as próprias células coletores de lixo do fígado para que desmontem o tecido cicatricial e desliguem os sinais de alarme crônicos que mantêm o dano. Ao usar instruções de mRNA de curta duração empacotadas em nanopartículas inteligentes, a terapia evita alterar permanentemente as células e limita a atividade às regiões doentes, o que pode reduzir efeitos colaterais. Embora sejam necessários muitos testes adicionais antes de tentar em humanos, essa estratégia delineia um plano promissor para tratar a fibrose hepática — e potencialmente outras doenças fibróticas — transformando o próprio sistema imunológico do corpo de um motor de cicatrização em um parceiro ativo na reparação.
Citação: Gao, J., Yang, Z., Song, Y. et al. TRIM13 in situ engineering boosts anti-inflammatory capacity of CAR-Ms for liver fibrosis therapy. Nat Commun 17, 2077 (2026). https://doi.org/10.1038/s41467-026-69858-3
Palavras-chave: fibrose hepática, terapia com macrófagos, entrega de mRNA por nanopartículas, receptor quimérico de antígeno, via TRIM13 STING