Clear Sky Science · pt
Radiomarcação de oligopeptídeos por troca seletiva de isótopos de hidrogênio com deutério e trítio em tampões aquosos
Rastreando medicamentos no nível atômico
Medicamentos modernos incluem cada vez mais moléculas biológicas complexas, como peptídeos e pequenas proteínas. Para entender para onde esses fármacos vão no corpo e por quanto tempo permanecem, os cientistas frequentemente substituem alguns átomos comuns por outros raros ou radioativos que podem ser rastreados. Este artigo apresenta uma forma de “marcar” fármacos peptídicos com esses átomos rastreáveis diretamente em soluções aquosas, muito mais próxima das condições biológicas reais do que a maioria dos métodos anteriores.
Por que trocas atômicas mínimas importam
Substituir o hidrogênio normal por formas mais pesadas, como deutério ou trítio, transforma moléculas comuns em poderosos traçadores científicos. Essas versões marcadas comportam-se quase da mesma forma que o fármaco original, mas podem ser seguidas por instrumentos sensíveis que detectam massa ou radiação. Para pequenas moléculas farmacêuticas, os químicos desenvolveram um vasto conjunto de ferramentas para preparar esses compostos marcados. Em contraste, os métodos para marcar biologicos maiores e frágeis — como peptídeos e proteínas — são escassos, frequentemente complicados e pouco adequados a ambientes aquosos semelhantes ao sangue ou fluidos celulares. Os autores buscaram preencher essa lacuna: uma maneira simples e seletiva de inserir deutério ou trítio em blocos de construção peptídicos diretamente em tampões aquosos.
Uma estratégia de marcação em uma única etapa em água
A equipe concentrou-se em um tipo de reação chamada troca de isótopos de hidrogênio, na qual um átomo de hidrogênio em uma molécula é trocado por seu primo mais pesado a partir de um gás como deutério (D2) ou trítio (T2). Eles montaram um catalisador in situ baseado em irídio e uma molécula auxiliar de fósforo (fósfina) especialmente escolhida. Quando misturado em um tampão levemente básico e aquecido, esse sistema ativa ligações carbono–hidrogênio específicas em aminoácidos e pequenos peptídeos e substitui esses hidrogênios por deutério ou trítio vindos do gás. O ponto crucial é que isso ocorre em uma única etapa, em meio rico em água, e com quantidades muito baixas de metal — condições mais compatíveis com peptídeos delicados e com fluxos de trabalho práticos de laboratório. 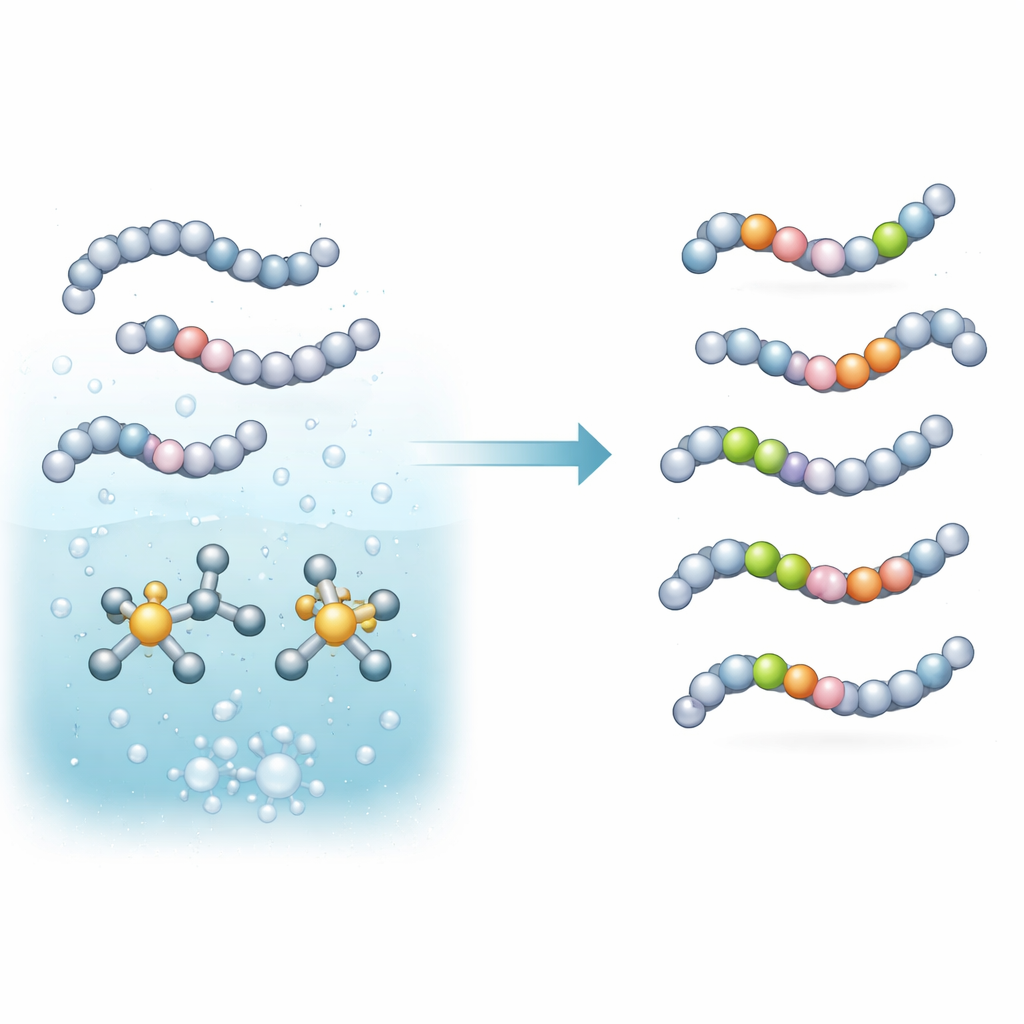
Escolhendo os pontos certos nos peptídeos
Nem todo átomo de hidrogênio em um peptídeo é igualmente útil como marcador. Alguns são facilmente perdidos durante o metabolismo, o que apagaria a etiqueta radioativa. Os autores exploraram cuidadosamente onde seu catalisador prefere agir. Descobriram que aminoácidos não protegidos, como lisina e arginina, são particularmente bem adequados. Na lisina, o método marca seletivamente um carbono na cadeia lateral (a chamada posição gama), um sítio considerado “não ativado” e mais propenso a permanecer estável no organismo. A arginina apresenta comportamento semelhante em posições próximas na sua cadeia lateral. Ao testar uma série de moléculas relacionadas, incluindo cadeias curtas com dois grupos amino, a equipe encontrou que ter dois sítios de nitrogênio posicionados adequadamente ajuda o catalisador metálico a se prender à molécula e alcançar a ligação carbono–hidrogênio alvo.
Examinando o mecanismo do catalisador
Para compreender por que essa seletividade surge, os pesquisadores combinaram experimentos com simulações computacionais detalhadas usando teoria do funcional da densidade. Esses cálculos mapeiam a paisagem energética conforme o complexo de irídio se forma a partir de um material dimérico inicial, se liga à água, depois ao aminoácido e, finalmente, insere-se em uma ligação carbono–hidrogênio específica. Os modelos mostram que romper o dímero de irídio original é energeticamente factível em água para um tipo de precursor, mas não para outro estreitamente relacionado, explicando por que apenas certos complexos iniciais são eficazes. Eles também revelam que o próprio substrato ajuda a estabilizar o centro metálico ativo e a evitar que ele agregue em partículas inativas. A via mais favorável envolve o aminoácido ligando-se através de dois átomos de nitrogênio, formando uma espécie de “pinça” que posiciona uma única ligação carbono–hidrogênio para troca com deutério ou trítio.
De blocos de construção simples a fármacos peptídicos reais
Com o mecanismo em mãos, a equipe estendeu o método de aminoácidos isolados para peptídeos curtos contendo até sete resíduos e, em seguida, para sequências terapêuticas mais complexas com até 13 aminoácidos. Em todos os casos, a marcação ocorreu nas cadeias laterais de lisina ou arginina na extremidade do peptídeo, e os peptídeos permaneceram majoritariamente intactos nas condições de reação. Para o trítio, eles otimizaram a reação em baixas pressões de gás para alcançar com segurança altas atividades específicas, significando que uma grande fração das moléculas carrega ao menos um átomo de trítio. Esses peptídeos marcados com trítio foram produzidos em uma única etapa e estão prontos para uso como traçadores em estudos in vitro e, potencialmente, in vivo. 
O que isso significa para medicamentos futuros
Este trabalho demonstra que é possível ligar seletivamente deutério ou trítio a fármacos peptídicos realistas em uma etapa simples em meio aquoso, enquanto se mira posições metabolicamente robustas em aminoácidos-chave. Para desenvolvedores de fármacos, isso significa acesso facilitado a versões de traçadores precisamente marcadas de terapias peptídicas, vitais para medir absorção, distribuição e metabolismo. Além da produção de traçadores, os insights mecanísticos sobre como o catalisador de irídio interage com aminoácidos podem inspirar novas maneiras de ajustar onde e como biomoléculas complexas são modificadas, abrindo portas para um controle químico mais preciso sobre medicamentos biológicos futuros.
Citação: Martinelli, E., Weck, R., Güssregen, S. et al. Radiolabeling of oligopeptides by selective hydrogen isotope exchange with deuterium and tritium in aqueous buffers. Nat Commun 17, 2317 (2026). https://doi.org/10.1038/s41467-026-69850-x
Palavras-chave: peptídeos radiomarcados, troca de isótopos de hidrogênio, marcação com deutério e trítio, terapêuticos peptídicos, catálise por irídio