Clear Sky Science · pt
Maximizando a utilização de energia e a eficiência de lixiviação de lítio via dupla oxidação eletroquímica sequencial e imersão-relaxamento
Por que baterias de carro antigas ainda importam
As baterias de íon-lítio alimentam nossos telefones, laptops e, cada vez mais, nossos carros. Mas à medida que milhões de módulos de veículos elétricos chegam ao fim de sua vida útil, eles geram um novo tipo de resíduo — e uma nova oportunidade. O lítio e outros metais presos dentro de baterias gastas são valiosos, mas exigem muita energia para serem recuperados. Este estudo explora uma maneira mais inteligente de extrair o lítio usando eletricidade de forma mais eficiente, reduzindo custos e impacto ambiental enquanto atende ao apetite mundial crescente por materiais para baterias.
Transformando baterias descartadas em recurso
Hoje, a maior parte da reciclagem industrial de baterias de íon-lítio depende de produtos químicos agressivos ou fornos de alta temperatura. Esses métodos podem recuperar metais, mas frequentemente desperdiçam energia e dificultam a separação limpa do lítio do níquel, cobalto e manganês nas chamadas baterias NCM. Os pesquisadores focaram em uma rota mais nova e mais limpa: usar uma corrente elétrica em água salgada para extrair o lítio do material do cátodo usado. Fizeram uma pergunta simples, porém crucial: podemos reorganizar quando e como usamos eletricidade para que quase cada watt ajude a remover o lítio, em vez de ser perdido em reações secundárias?
Uma dança em dois passos: potência, depois silêncio
A equipe desenhou um processo em duas etapas que combina um “empurrão” ativo com uma “imersão” silenciosa. Na primeira etapa, chamada dupla oxidação eletroquímica, uma tensão constante é aplicada através de uma célula contendo um cátodo NCM gasto e uma solução de cloreto de sódio. A corrente puxa íons de lítio do sólido para o líquido enquanto também gera espécies oxidantes poderosas na solução. Os cientistas descobriram que a maior parte do trabalho útil acontece na primeira hora: o lítio sai da estrutura cristalina rapidamente no início, mas depois grande parte da energia é desperdiçada em reações secundárias, como a formação de bolhas de oxigênio.
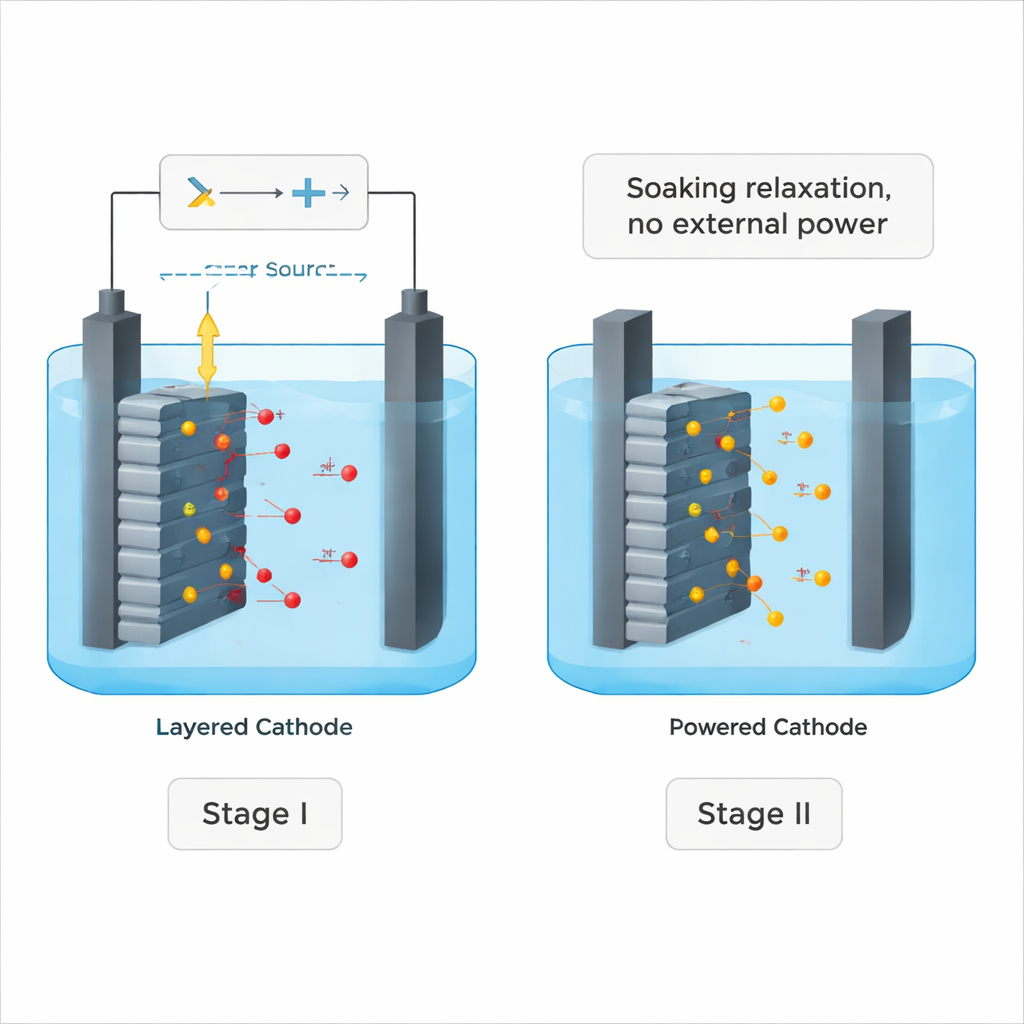
Deixando a química terminar o trabalho
Em vez de manter a energia por mais e mais tempo, os pesquisadores simplesmente desligaram e deixaram o eletrodo imerso na solução salina agora oxidante. Surpreendentemente, o lítio continuou a lixiviar até quase todo ser removido — atingindo cerca de 99% de recuperação para material NCM novo e aproximadamente 98% para cátodos realmente usados. Medições detalhadas mostraram que átomos de oxigênio dentro do cristal, temporariamente levados a um estado mais reativo durante a etapa com energia, tornaram-se o motor oculto nessa segunda etapa silenciosa. Essas espécies de oxigênio “ativadas” promoveram uma troca lenta: íons de lítio difundiram para o líquido enquanto íons de sódio (ou potássio) da solução ocupavam os espaços vazios, tudo sem entrada elétrica adicional.
Como a estrutura cristalina se rearranja
Usando microscópios eletrônicos, difração de raios X e espectroscopia, a equipe observou as partículas do cátodo racharem, afinarem e mudarem seu empilhamento interno à medida que o lítio partia. O material passou por várias arranjos em camadas conhecidos ao ir de rico em lítio para pobre em lítio, terminando em uma forma rica em sódio que manteve a estrutura, mas não continha mais muito lítio. Ao longo desse processo, átomos de níquel e cobalto mudaram seus estados de carga para manter o equilíbrio elétrico geral do material, enquanto o manganês permaneceu majoritariamente inalterado, ajudando a estabilizar a estrutura. Os pesquisadores também mostraram que íons de potássio, que perdem suas moléculas de água mais facilmente que o sódio, podem acelerar ainda mais a etapa de troca de íons.
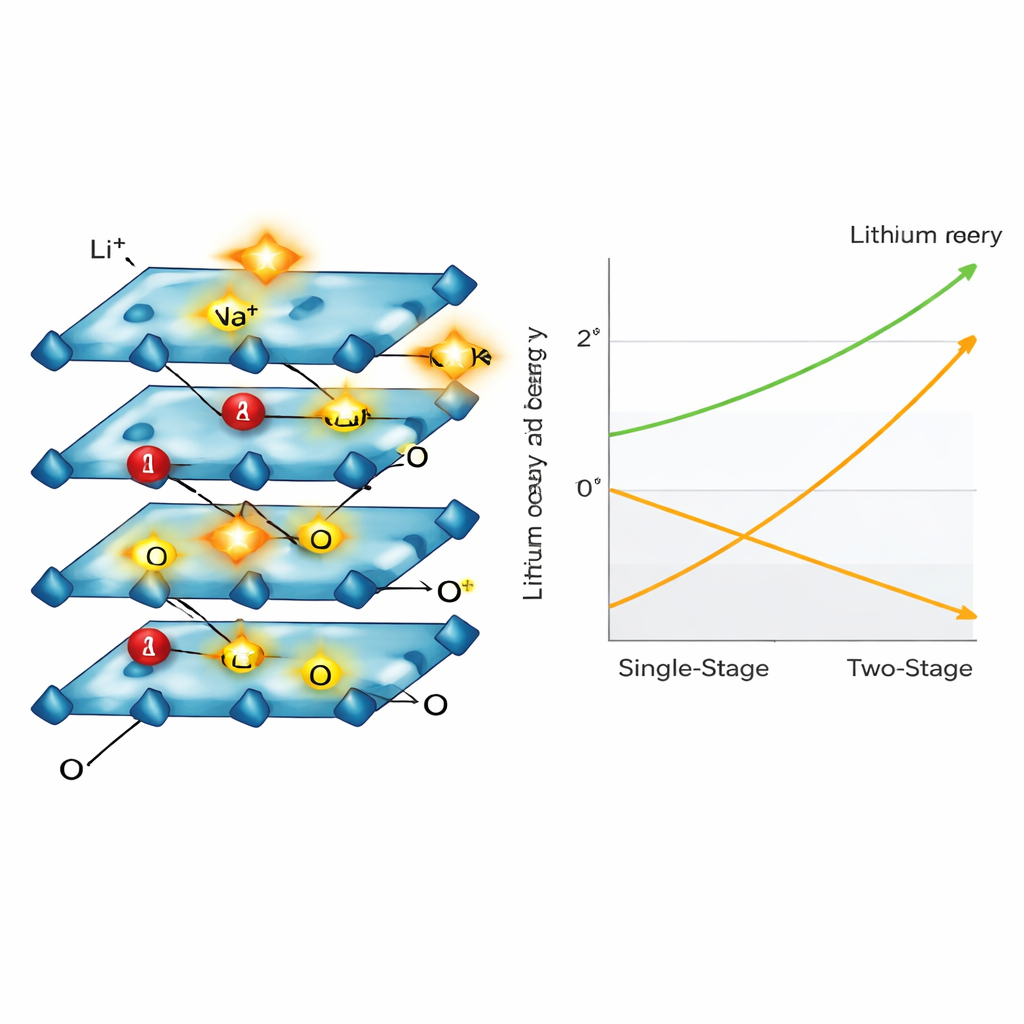
Do banco de laboratório ao chão da indústria
Para testar se a ideia funcionaria fora do laboratório, a equipe construiu um sistema piloto capaz de tratar meio quilo de resíduos reais de bateria por lote. Usando seu método em duas etapas, recuperaram mais de 98% do lítio como carbonato de lítio de alta pureza, adequado para fabricar novas baterias. Crucialmente, porque a energia é desligada assim que a “química inteligente” é ativada, o processo usou cerca de metade da energia elétrica de um método eletroquímico padrão de etapa única, economizando mais de um quinto do lucro operacional total por tonelada de material de cátodo reciclado.
O que isso significa para baterias futuras
Em termos simples, o estudo mostra que nem sempre precisamos continuar injetando eletricidade para recuperar materiais valiosos de baterias antigas. Uma rajada de energia bem temporizada pode preparar o material e a solução para que o restante do trabalho ocorra por si só, impulsionado por forças químicas internas. Se adotada em escala, essa abordagem em duas etapas pode tornar a reciclagem de lítio de baterias NCM gastas mais barata, mais limpa e mais atraente para a indústria, ajudando a fechar o ciclo de vida das baterias e reduzindo a pressão sobre a mineração de lítio nova.
Citação: Zhong, W., Gu, X., Feng, X. et al. Maximizing energy utilization and lithium leaching efficiency via sequential electrochemical dual-oxidation and soaking-relaxation. Nat Commun 17, 2050 (2026). https://doi.org/10.1038/s41467-026-69834-x
Palavras-chave: reciclagem de lítio, resíduos de baterias, lixiviação energeticamente eficiente, cátodos NCM, recuperação eletroquímica