Clear Sky Science · pt
Sobrevivência de cianobactérias e mitigação dos efeitos tóxicos do Fe(II) em um oceano Arqueano rico em sílica
Mares antigos e o ar que respiramos
Bilhões de anos antes do aparecimento de animais ou plantas, minúsculos microrganismos fotossintéticos chamados cianobactérias começaram a liberar oxigênio nos oceanos da Terra. Ainda assim, levou centenas de milhões de anos até que o oxigênio se acumulasse na atmosfera. Este estudo investiga por que esse atraso foi tão longo e se a química dos mares primitivos — ricos em ferro dissolvido e sílica — ajudou ou atrapalhou os micróbios que, em última instância, tornaram nosso planeta respirável.

Mares ricos em ferro e um efeito colateral tóxico
Os oceanos primitivos continham grandes quantidades de ferro dissolvido, especialmente em regiões costeiras onde águas profundas afloravam à superfície. Quando esse ferro encontrava o oxigênio liberado pelas cianobactérias, ele oxida-va, formando minerais de ferro que mais tarde deram origem às formações ferríferas laminadas — rochas estriadas que constituem alguns de nossos arquivos geológicos mais antigos. Mas as mesmas reações também podem gerar “espécies reativas de oxigênio”, formas altamente agressivas de oxigênio que podem danificar DNA, proteínas e membranas celulares. Trabalhos anteriores sugeriram que essa reação química impulsionada pelo ferro poderia ter envenenado as cianobactérias, retardando sua expansão e adiando a elevação do oxigênio na atmosfera.
Sílica como uma guarda-costas inesperada
Os autores concentraram-se em outro ingrediente abundante da água do mar antiga: a sílica dissolvida, o mesmo material básico encontrado no vidro. Evidências geológicas indicam que os oceanos primitivos continham sílica em concentrações muito superiores às atuais. Em experimentos de laboratório, eles cultivaram uma cianobactéria marinha (Synechococcus sp. PCC 7002) sob condições cuidadosamente controladas com diferentes quantidades de ferro e sílica dissolvidos. Monitoraram a velocidade de crescimento das células, quanto oxigênio produziam, quão rápido o ferro era oxidado e quanto de oxigênio reativo se formava. Em níveis baixos de ferro, as células prosperaram independentemente da sílica. Mas quando o ferro era muito alto — semelhante às condições esperadas em algumas águas costeiras do Arqueano — culturas sem sílica adicionada enfraqueceram, enquanto aquelas com alta sílica permaneceram ativas, produziram mais oxigênio e alcançaram maiores números de células.
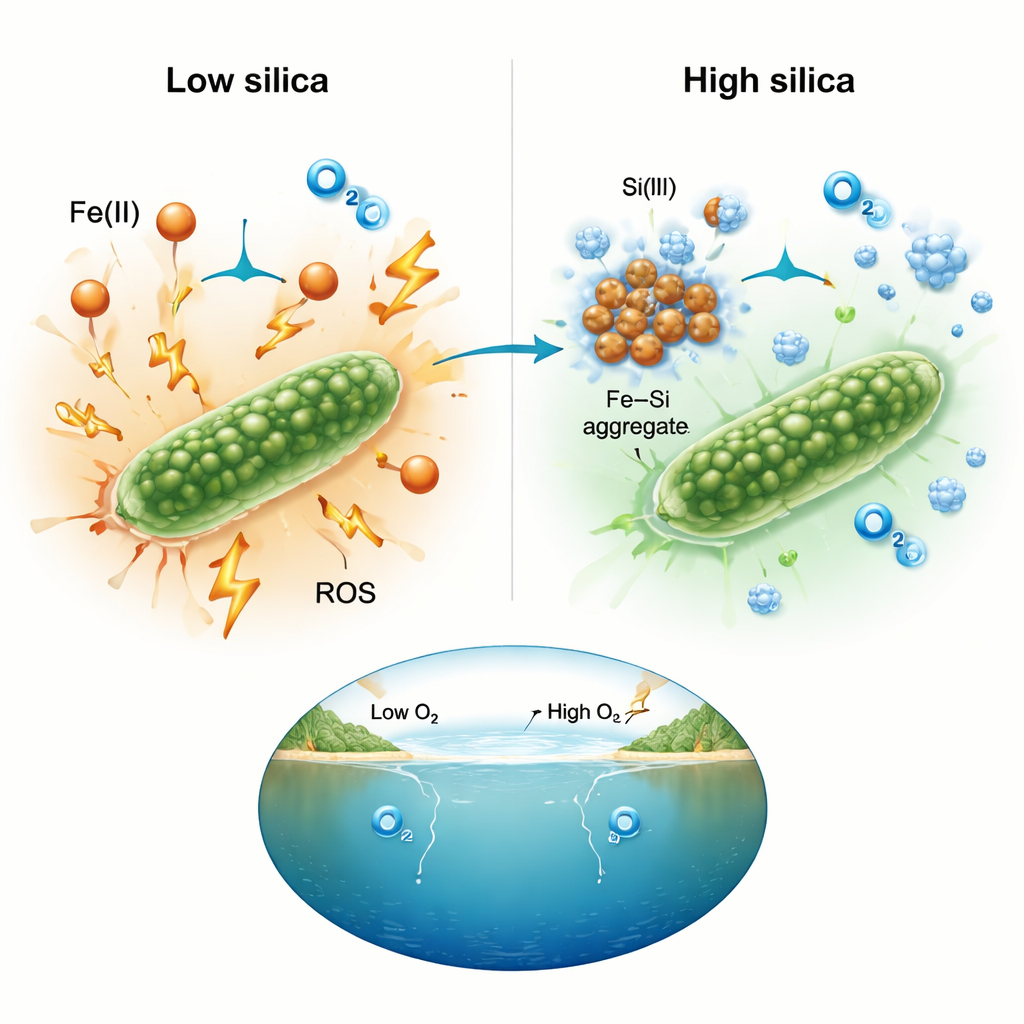
Trabalho químico conjunto que domou reações prejudiciais
Para entender por que a sílica fez tanta diferença, a equipe mediu diretamente o oxigênio reativo usando corantes fluorescentes. Em níveis altos de ferro, culturas sem sílica mostraram sinais fortes de oxigênio reativo, compatíveis com uma química estressante ao redor das células. Em arranjos ricos em sílica, esses sinais permaneceram próximos ao nível de fundo mesmo quando as concentrações de ferro eram extremas. Os pesquisadores interpretam isso como resultado da ligação da sílica ao ferro dissolvido e da formação de agregados ferro–sílica. Uma vez aprisionado nesses aglomerados, o ferro fica menos disponível para alimentar as reações em cadeia que geram oxidantes danosos. O efeito líquido é suavizar o ambiente químico, permitindo que as cianobactérias continuem a fotossintetizar em vez de serem incapacitas pelo estresse oxidativo.
Ritmos dia–noite e impactos em escala oceânica
Os experimentos também foram conduzidos sob ciclos realistas de luz dia–noite, em vez de iluminação constante. Nessas condições alternadas, as cianobactérias oxidaram o ferro mais rapidamente e toleraram melhor águas com alto teor de ferro, sugerindo que os períodos noturnos de “descanso” reduzem o estresse de longo prazo. Usando taxas de produção de oxigênio medidas em laboratório, os autores então construíram um modelo numérico simples de uma coluna de água do oceano primitivo. Para abundâncias plausíveis de cianobactérias e taxas realistas de ressurgência de águas profundas, eles verificaram que as águas superficiais podiam se tornar ricas em oxigênio enquanto camadas mais profundas permaneciam carregadas de ferro. Em muitos cenários, as concentrações de oxigênio na zona iluminada alcançaram ou excederam os níveis de saturação da água do mar modernos, o que implica que “oásis” locais de oxigênio acima de profundidades ricas em ferro poderiam ter sido comuns.
Repensando por que o oxigênio demorou tanto
Em conjunto, os resultados indicam que o oxigênio reativo formado a partir do ferro e do oxigênio provavelmente não foi um problema insuperável para as primeiras cianobactérias, desde que a sílica fosse abundante e os ciclos naturais dia–noite prevalecessem. Em vez de serem envenenados cronicamente, esses microrganismos provavelmente encontraram muitos ambientes costeiros onde a sílica amortecia os efeitos nocivos do ferro, permitindo-lhes crescer, oxidar enormes quantidades de ferro e liberar oxigênio excedente para a atmosfera. O mistério persistente de por que a atmosfera da Terra se oxigenou tão tardiamente deve, portanto, residir mais em fatores de grande escala — como a rapidez com que o oxigênio foi consumido por gases vulcânicos e rochas — do que na química local ao redor de células microbianas individuais.
Citação: Dreher, C.L., Cirpka, O.A., Schad, M. et al. Survival of cyanobacteria and mitigation of Fe(II) toxicity effects in a silica-rich Archean ocean. Nat Commun 17, 1987 (2026). https://doi.org/10.1038/s41467-026-69826-x
Palavras-chave: oxigênio na Terra primitiva, cianobactérias, formações ferríferas laminadas, espécies reativas de oxigênio, oceanos ricos em sílica